Química
Química
CUESTIONARIO DE QUÍMICA
¿Qué es la química?
Es un intento de descripción y explicación sistemática de la materia y de la materia y de los cambios que sufre.
¿Qué es ciencia?
Es el conocimiento de las cosas por sus causas.
¿Cuáles son los dos tipos de Ciencias Naturales que existen?
Ciencias Físicas y Ciencias Biológicas.
Menciona el nombre de algunas ciencias físicas.
-
Física
-
Geología
-
Química
-
Astronomía
-
Menciona el nombre de algunas ciencias biológicas
-
Botánica
-
Fisiología
-
Genética
-
Ecología
-
¿Cuál es el objeto de estudio de la Química?
-
¿Cuántos tipos de cambios hay?
-
¿Cuáles son los cambios físicos?
-
¿Cuáles son los cambios químicos?
-
Menciona algunas ramas de la química.
-
Química farmacéutica
-
Bioquímica
-
Fisicoquímica
-
Química agrícola
-
Química analítica
-
Química inorgánica
-
Química orgánica
-
Menciona el objeto de estudio de la química farmacéutica
-
Objeto de estudio de la bioquímica.
-
¿Cuál es el objeto de estudio de la fisicoquímica?
-
¿Qué estudia la química agrícola?
-
¿Cuál es el objeto de estudio de la química analítica?
-
¿A qué se llama química orgánica?
-
¿A qué se le llama química inorgánica?
-
¿Qué es materia?
-
¿Qué es energía?
-
¿Qué es sustancia?
-
¿Cuáles son los dos tipos de sustancias que existen?
-
¿Quiénes componen a las sustancias puras?
-
Da el ejemplo de un elemento.
-
Da un ejemplo de un compuesto.
-
Menciona algunas características de las sustancias puras (elementos y compuestos)
-
Tienen propiedades químicas
-
Propiedades físicas
-
Clasificación
-
¿Quiénes componen a las sustancias impuras?
-
Da el ejemplo de una mezcla.
-
¿Cómo pueden ser las mezclas?
-
Característica de las mezclas homogéneas.
-
Características de las mezclas heterogéneas
-
A los siguientes tipos de materia anota si son elementos, compuestos, o mezclas
-
Agua: Compuesto
-
Oro: Elemento
-
Aire: Mezcla Homogénea
-
Alcohol: Compuesto
-
Tequila: Mezcla homogénea
-
Aluminio: Elemento
-
Ozono: Compuesto
-
Agua de mar: Mezcla homogénea
-
Ensalada: Mezcla heterogénea
-
Leche: Mezcla homogénea
-
Bauxita: Mezcla heterogénea
-
¿Qué es un metal?
-
¿Qué es un mineral?
-
¿Qué es la tabla periódica?
-
¿Qué es la triada de Döbereiner?
-
¿Qué es la ley de las octavas de Newlands?
-
¿Cuál es el sistema periódico de Mendeleiev-Meyer?
-
¿Cuál es el sistema periódico?
-
¿Cuál es el anatema periódico moderno?
-
¿Cómo se divide la tabla periódica para su estudio?
-
¿Qué es una familia?
-
¿Qué es un grupo?
-
¿Qué es un periodo?
-
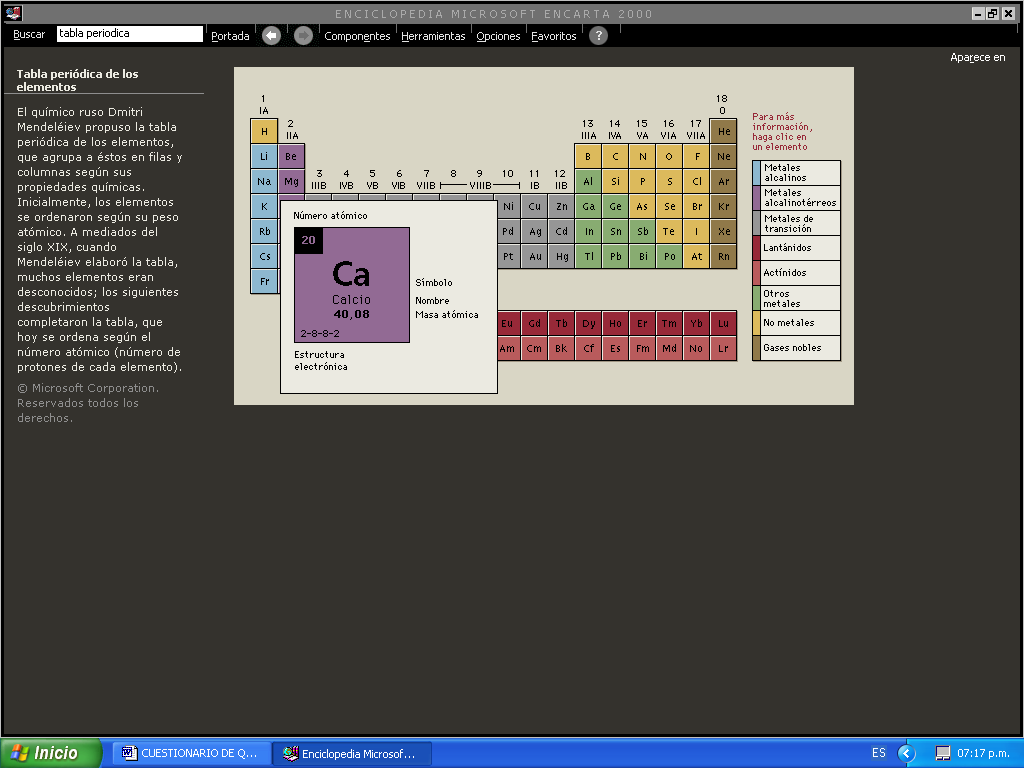
¿Qué es un símbolo químico?
-
¿Qué es el número atómico?
-
¿Qué es la serie de los lantánidos?
-
¿Cuál es la serie de los actínidos?
-
¿Qué elementos son conocidos desde la antigüedad?
-
¿Quién es el padre de la Tabla Periódica?
-
¿Con cuántos elementos metálicos contó Mendeleiev (1869) para elaborar su Tabla?
-
¿Cuál fue el primer elemento descubierto científicamente, quién fue su descubridor y en qué año lo hizo?
-
Dibuja una tabla periódica y escribe sus partes
-
Escribe el metal correspondiente a cada mineral dado
-
Calcopirita (CuFeS2): Cobre
-
Casiterita (SnO2): Estaño
-
Bauxita (Al2O3.7H2O): Cromo y Aluminio
-
Esfalerita (ZnS): Zinc
-
Hematina (Fe2O3): Fierro
-
Halita (NaCl): Sodio
-
¿Cuáles son las diferencias entre un metal y un mineral?
-
¿Cuál es el estado físico de un elemento metálico?
-
¿Qué es la maleabilidad?
-
¿Qué son las propiedades?
-
De acuerdo a la propiedad del aluminio escribe su aplicación
-
Escribe las propiedades físicas de la bauxita.
-
Es terrosa
-
Forma de arcilla o roca
-
Es blanca, gris o crea (si es baja en hierro)
-
Color rosado, amarillo, café claro (si es alta en hierro)
-
Escribe ejemplos de procesos químicos.
-
Fundición
-
Refinación
-
Purificación
-
Baño de criolita
-
Fabricación
-
Escribe en que proporción integran a cada compuesto.
-
Al2O3: por cada 2 átomos de Aluminio hay 3 átomos de Oxígeno
-
Al2O3.7h2O: por cada 2 átomos de Aluminio hay 3 de oxígeno, y por 14 de Hidrógeno hay 7 de Oxígeno.
-
CaO: por cada átomo de Calcio hay uno de Oxígeno
-
NaOH: por cada átomo de Sodio hay uno de Oxígeno y otro de Hidrógeno
-
Fe2O3: por cada 2 átomos de fierro hay 3 de Oxígeno
-
A las siguientes fórmulas escribe su nombre común y su nombre químico
-
¿A qué se le llama fórmula?
-
¿A qué se le llama composición?
-
En una muestra de bauxita que pesa 5 kilos, se extraen 450 gramos de Aluminio. ¿Qué porcentaje de Aluminio había originalmente?
-
El porcentaje de una muestra de Aluminio en una muestra de bauxita es de 48%, ¿qué cantidad podría extraerse de 300 gramos de bauxita?
-
¿Qué es una aleación?
-
¿Qué cantidad de silicio se necesita adicionar para obtener 6kg. de aleación 4000 al 8%?
-
Una muestra de 1800g. de aleación 8000 contienen 120g. de berilio, ¿qué porcentaje de berilio contiene la aleación?
-
Si se desean obtener 0.4 toneladas de aleación serie 3000, ¿qué cantidad de manganeso deberá agregarse?
-
Desde que siglo en México se hacían aleaciones, sobre todo de cobre y oro?
-
¿Qué es una propiedad química?
-
Menciona algunas propiedades químicas del aluminio.
-
Oxidación
-
Corrosión
-
¿Qué es el proceso electrolítico?
-
¿Qué es una reacción química?
-
¿Qué es corrosión?
-
¿Qué es un óxido?
-
Haz una representación gráfica de la reacción química.
-
Valencia con la que siempre actúa el oxígeno
-
¿A qué familia pertenecen los elementos que siempre actúan con número de oxidación uno?
-
¿Con qué valencia actúan los elementos de la familia 2 A?
-
¿Con que valencia actúan los elementos de la familia B?
-
¿Cuál es el número de oxidación de un elemento?
-
¿Cómo se clasifican los compuestos de acuerdo al número de elementos que lo forman?
-
Compuestos binarios: con 2 elementos diferentes
-
Compuestos pernarios: con tres elementos ternarios
-
Compuestos cuaternarios: con cuatro elementos diferentes
-
¿Qué es un Ion?
-
¿Qué es un cation?
-
¿Qué es un anion?
-
¿Cómo se les denomina a los iones formados un solo átomo?
-
Da un ejemplo de un Ion monoatómico.
-
¿Cómo se les llama a los iones formados por más de un átomo?
-
Balancea las siguientes ecuaciones.
-
¿Qué es una ecuación química?
-
Escribe el nombre químico de cada sustancia.
-
LiO: Oxido de Litio
-
Cu2O: Oxido de Cobre II
-
Mn2O3: Oxido de Manganeso III
-
CrO: Oxido de Cromo
-
Rb2O: Oxido de Rubidio
-
¿Cómo se clasifican las reacciones químicas?
-
¿Cuál es la reacción de síntesis?
-
¿Cuál es la reacción de descomposición?
-
¿Quién propuso la Ley de la Conservación de la Materia?
-
¿Qué dice la Ley de la Conservación de la Materia?
-
NaCl: Cloruro de Sodio
-
KBr: Bromuro de Potasio
-
MgF2: Fluoruro de Manganeso.
El estudio de la materia, su estructura molecular, composición origen y cambios.
Físicos y químicos.
Elasticidad, cambio de estado, etc.
Mezclas, oxidación, cambio de color.
Fármacos y efectos sobre el cuerpo, análisis de sangre y orina.
Se relaciona con la química de los procesos de los seres vivos
La aplicación de los métodos y teorías de la física a cambios químicos y de las propiedades de la materia.
Hace los fertilizantes, pesticidas, estudia la nutrición de animales, crecimiento de plantas y el cultivo de tierra.
Trata sobre la detección o identificación de las sustancias presentes en un material y cuanto de estas esta presente.
A la química de los compuestos formados de carbono e hidrógeno.
A la rama de la química que estudia las sustancias que no contienen carbono combinado con hidrógeno.
Es todo aquello que ocupa un lugar en el espacio.
Capacidad para realizar un trabajo.
Un elemento o un compuesto químico.
La pura y la impura.
Los elementos y los compuestos.
Un metal.
Los óxidos.
Las mezclas.
Minerales.
Homogéneas y heterogéneas.
No se ven a simple vista
Es posible distinguir sus elementos
Material sólido que es buen conductor y se puede aprovechar en la mayoría de los instrumentos de la vida cotidiana. Se encuentra dentro del mineral
Material rocoso del que se pueden extraer varios metales
Es una distribución tabular de elementos basada en las propiedades químicas y físicas de estos.
Es la primera clasificación que se hizo de los elementos químicos. Agrupaba elementos con propiedades semejantes en grupos de tres.
Después de cada siete elementos, en el octavo se repetían propiedades del primero.
Organización de los elementos considerando no sólo sus propiedades físicas y químicas, si no t6ambién su peso atómico. Su tabla posee diez filas horizontales y nueve columnas verticales, incluyendo ya a los gases nobles.
J. Moseley enuncia el concepto de número atómico. La tabla consta de 18 columnas o grupos y siete filas o periodos. En cada grupo se colocan los elementos con propiedades similares, y cada periodo se construye colocando elementos que aumentan en una unidad el numero atómico del elemento precedente.
Seaborg, reconfiguro la tabla periódica poniendo la serie de los actínidos debajo de la serie de los lantánidos.
En grupos, familias y periodos
Es un conjunto de grupos de elementos con propiedades similares, existen dos en la tabla periódica, que son A y B
Es una columna y existen 18 en la tabla
Es una fila en la tabla periódica y existen 7
Es la expresión de una o dos letras para representar a un elemento
Representa en la tabla periódica el número de protones que contiene cada átomo de un elemento.
Es un grupo de elementos que fácilmente forma cationes por tener incompleta la capa 4F
Es un grupo de elementos que tienen completa o incompleta la capa 5F
Oro, plata, estaño, cobre, plata y mercurio
Dimitri Ivanovich Mendeleiev.
Con 52
Fósforo, Henning Brand, en 1669 y era un no metal. Aunque antes se descubrió el arsénico.
El mineral contiene a los metales, para poder ver un metal hay que extraerlo del mineral mediante procesos químicos, el metal se usa en la vida cotidiana, mientras que el mineral debe pasar por varios procesos.
Sólido, líquido y gaseoso
La deformación que pueden sufrir los metales
Son las cualidades o características particulares de las sustancias, que les confieren una identidad exclusiva.
| Propiedad | Aplicación |
| Magnifico reflector de luz | Fabricación de espejos |
| No despide olores | Alimentación, comida |
| Es poco tóxico | Envases, charolas |
| Buen reflector de radio y radar | Antenas satelitales |
| Es muy ligero | Fabricación de aviones carros, construcción de edificios |
| Formula | Nombre Común | Nombre químico |
| Al2O3 | Alúmina | Óxido de Aluminio |
| Al2O3.7h2O | Bauxita | Oxido de Aluminio heptahidratado |
| CaO | Cal viva | Oxido de Calcio |
| NaOH | Sosa Cáustica | Hidróxido de sodio |
| Fe2O3 | Herrumbre | Oxido de hierro |
A la representación gráfica de un compuesto químico, e indica qué elementos y en que proporción se encuentran en dicho compuesto.
A la relación de integrantes que tiene una sustancia, y que puede determinarse mediante un análisis químico .
Sustancia impura de características metálicas obtenida por la incorporación de otros elementos a un metal.
71.¿Qué Estado de la República Mexicana es el mayor productor de metales?
Zacatecas
Desde el siglo XIV, y se le conocía a esta aleación como tumbaga.
Son aquellas que se determinan por la alteración (reacción química) de la estructura interna de la materia.
Es aquel que utiliza electricidad para efectuar cambios químicos en la materia.
Es la transformación de una o mas sustancias en otras diferentes y se compone por reactivos y productos.
Destrucción por la acción del agua.
Compuesto que resulta de la combinación de oxígeno con otro elemento.
Con la valencia 2
De la familia 1 A
Con 2
Por lo general sus elementos tienen mas de una valencia.
Es el numero e cargas que adquiere un átomo al reaccionar con otro, por la transferencia de electrones entre ellos para formar un compuesto.
Es un átomo o un grupo de átomos que posee carga eléctrica, se clasifican en aniones y cationes.
Es un átomo o grupo de átomos que tienen carga positiva, lo cuales se forman por la perdida de electrones.
Es un átomo o grupo de átomos con carga eléctrica negativa, el cual se forma cuando gana electrones.
Monoatómicos.
Na, Cl., Ag, Pb.
Poliatómicos.
Na + O2
Mg + O2
Sn + O2
Es la representación química de cambios y reacciones.
De síntesis, de descomposición, de sustitución y de oxido reducción.
Aquella que se efectúa cuando 2 o mas sustancias se combinan para formar una sola, un ejemplo de esta reacción es la formación de óxidos.
Es aquella que se efectúa cuando una sustancia se transforma en otra más simple, es inversa a la de síntesis.
Lavoisier
“La materia no se crea ni se destruye, solo se transforma”
100. ¿Qué tipo de carga tienen los protones?
Carga positiva
101. ¿Qué tipo de carga tienen los electrones?
Negativa
102. ¿Qué es el número atómico?
El número de protones que tiene un átomo.
103. ¿Qué tipo de carga tiene el neutrón?
No tiene ninguna
104. ¿Quiénes forman al átomo?
El núcleo y la corteza.
105. ¿Quién propuso la Teoría de la Estructura Atómica
Niels Bohr.
106. ¿Cuál fue la regla propuesta por Bohr que debieran seguir los electrones?
Cada electrón solo puede estar en una órbita de energía específica: los electrones sólo pueden moverse entre una y otra órbita absorbiendo o emitiendo energía: cuando un electrón salta de una capa superior a otra inferior , desprende energía radiante.
107. ¿Qué es un electrón de valencia?
Son los electrones que se encuentran en el ultimo nivel de energía de un átomo.
108. ¿A qué se llama regla de octeto?
La tendencia de los átomos a contar con ocho electrones de valencia.
109. ¿Cómo se les llama a los átomos con tendencia a perder electrones?
Metales.
110. ¿Cómo se les llama a los átomos con tendencia a ganar electrones?
No metales.
111. ¿Qué es un enlace iónico?
Cuando un elemento cede su electrón de valencia a otro elemento, ambos adquieren configuración estable 8, y al hacer esto uno de los elementos se convierte en cation (+) y el otro en un anion (-) se mantienen unidos por diferencia de cargas, a través del enlace químico llamado enlace iónico.
112. ¿Cómo se obtienen las sales binarias?
Al combinar un metal con un no metal
113. Escribe el nombre de las siguientes sales binarias
A + B C + D
Reactivos Productos
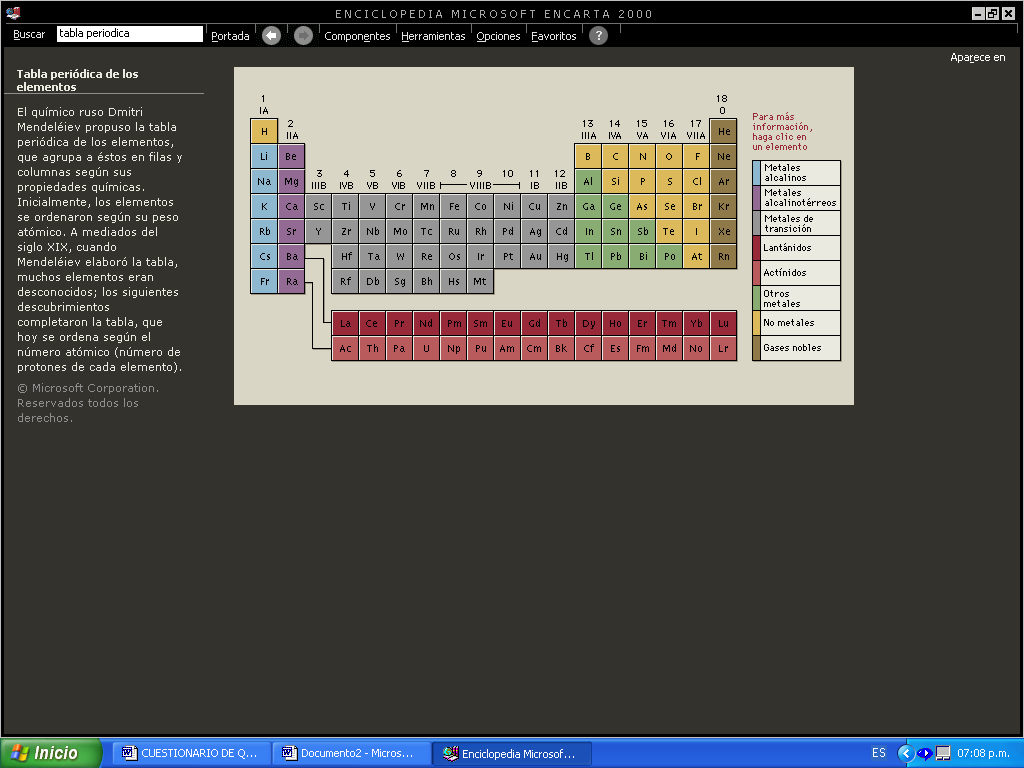
FAMILIA
PERIODO
G
R
U
P
O
4F SERIE DE LOS LANTÁNIDOS
5F SERIE DE LOS ACTÍNIDOS
Nº ATÓMICO
Descargar
| Enviado por: | Marcy |
| Idioma: | castellano |
| País: | México |
