Química
Separación de mezclas
“Técnicas de Separación de Mezclas”
Práctica 3
Química Inorgánica 1:00 PM
26 de febrero del 2003
Grupo 5
Objetivo: Experimentar algunas técnicas de separación de mezclas más comunes.
Introducción:
La materia, de acuerdo a su pureza, se clasifica en: sustancias puras, elementos y compuestos, y Mezclas; Homogéneas, heterogéneas y coloides.
Las sustancias puras son aquellas que no se pueden separar por métodos físicos no químicos comunes, los coloides son mezclas con moléculas de tamaño intermedio, tienen aspecto lechoso y presentan el efecto Tindal, las mezclas heterogéneas son a las que se les pueden observar 2 o más fases (una fase es la parte de una mezcla con las mismas propiedades físicas y químicas), las mezclas homogéneas son aquellas que sólo se les observa una fase, las dos anteriores estas unidas sólo físicamente, por lo cual se les puede separar por métodos físicos en los elementos que las componen. La técnicas más comunes son: La decantación sirve para separar dos líquidos inmiscibles (que no se mezclan), como por ejemplo agua y aceite. Se usa un embudo de decantación donde se dejan reposar los líquidos para después vaciar el que está debajo al abrir la llave. La cristalización sirve para separar un sólido disuelto en un líquido. En un recipiente llamado cristalizador se deja evaporar el líquido para separarlo del sólido. Tamización, cuando hay una mezcla heterogénea de sólidos si estos tienen distintos tamaños de partículas se pueden separar con un colador o harnero. Magnetismo Cuando una mezcla contiene un componente magnético, se puede separar de otro componente utilizando un imán.
En esta práctica utilizaremos algunos de los métodos más usados para separar mezclas. Utilizaremos, la filtración que es una técnica para separar mezclas heterogéneas de fases sólidas y líquidas, en esta se coloca un papel de filtro para retener él o los sólidos en éste y dejar fluir los líquidos a algún recipiente debajo del papel, claro que después de hacer esto todavía se tendría, en algunas ocasiones, volver a separar los líquidos y los sólidos en sus compuestos. La segunda técnica que usaremos será la destilación, ésta se utiliza para separar líquidos, en un matras de destilación se coloca las sustancia que se quiere separa, después se calienta y se espera a que los líquidos se evaporen, cada líquido de un compuesto diferente destila a diferente temperatura, se debe de tomar la temperatura cuando se observe que empieza a destilar algo en el matraz de destilación para poder identificar la sustancia que destiló. La tercera técnica es la sublimación que se una para separar sólidos.
Resultados:
En la primera parte de la práctica, tratamos de separar una mezcla de arena y agua con la técnica de la filtración, después de mezclarlas perfectamente vertimos la mezcla en un papel filtro y esperamos a que el agua fluyera al vaso que pusimos debajo de éste, cuando toda el agua que pudo, se encontraba en el vaso medimos la cantidad e agua recuperada, 17 ml de agua fue lo que había en el vaso, por su parte, la arena fue recuperada en su totalidad, 5 gr.
En la segunda parte de la práctica utilizamos la técnica de la destilación para tratar de separar una mezcla compuesta de 25 ml de etanol, 25 ml de agua y 5 gr de sal común (cloruro de sodio). Después de armar el equipo de destilación, vertimos la antes mencionada mezcla en el matraz de destilación, y la calentamos con el mechero, a los 12 minutos de estar calentando al se observó que la mezcla burbujeaba, este fenómeno ocurrió a una temperatura de 78°C, un liquido transparente comenzó a fluir desde el tubo de destilación al vaso de precipitados que colocamos para contener los líquidos destilados. Este liquido siguió cayendo al vaso y la temperatura de la mezcla se mantenía estable, cuando la temperatura comenzó a subir el líquido dejó de fluir poco a poco. La cantidad de liquido que recuperamos fue de 20 ml, éste tenía un olor muy penetrante y algo aturdidor. Esperamos pocos minutos más y cuando la temperatura de la mezcla alcanzó los 94 °C ésta entró de nuevo en un estado de ebullición, el liquido que fluyó hacia el vaso de precipitados era transparente y no tenía olor. Cuanto el antes mencionado líquido ya terminaba de fluir y de evaporarse dentro del matraz de destilación el tiempo de laboratorio terminó y no pudimos terminar de observar los resultados.
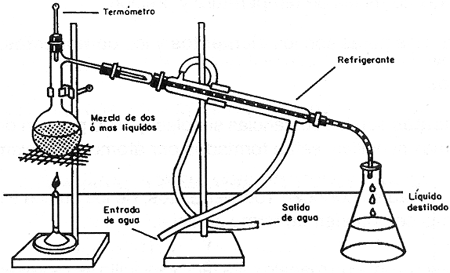
Ilustración 1: Fuente: http://biblioteca.itesm.mx/cgi-bin/nav/salta?cual=www:48835
En la tercera parte de la práctica utilizamos la técnica de la sublimación que consistió en mezclar 2 sólidos, la sal y yodo metálico, esta parte de la práctica se debe realizar en la campana de extracción de gases ya que los emitidos por esta reacción son tóxicos, colocamos estos dos compuestos en una cápsula de porcelana y la colocamos en la llama del mechero de Buncen y esperamos a que se calentara. Después de poco tiempo de calentamiento, el yodo comenzó a sublimarse poco a poco, en forma de un gas color morado denso, la sal quedó en la cápsula de porcelana adquirió un color morado muy tenue. En el vidrio de reloj vertimos agua para que lo enfriara, esto dio como resultado que se observaban unos pequeños cristales morados.
Análisis de Resultados:
Como ya se mencionó en la primera parte de la práctica, en el que usamos la técnica de la filtración, el agua que fluyó al vaso después de ser filtrada por el papel, era de color café claro, esto sucede por que el agua solvató parte de la arena y fue a caer agua y arena solvatada en el vaso, el volumen de agua que recuperamos en el vaso fue de 17 ml de estos una pequeña proporción era de arena, el agua restante para completar los 25 ml originales estuvo en el papel filtro y el arena, lo cual pesaba unos cuantos gramos más que los 5 gr. que teníamos de arena al agregarle la masa del agua, no pudimos registrar el peso de la arena mojada en el papel pero debió suceder lo antes dicho.
En la parte de la práctica que implicaba utilizar la técnica de la destilación obtuvimos como resultado dos líquidos que destilaron a diferentes temperaturas, a los 78°C el primer líquido destiló y según conocimientos previos supimos que era el etanol, ya que tenía un olor igual y tenía las mismas características físicas(incoloro, olor penetrante, líquido, etc.), otro dato que nos ayudo a saber que éste líquido era etanol es la ecuación descrita en la ecuación. El 2° líquido en destilar fue el agua ay que destiló a 98°C, no tenía olor y gozaba de las características físicas del agua. (incolora, inodora, líquida, etc.). Aemás de que utilizamos la formula descrita en la ecuación para saber que era agua y como sólo colocamos 2 líquidos también pudimos deducir que el primer líquido en destilar era el etanol.
En la técnica de la sublimación los 2 compuestos involucrados eran sólidos, al mezclarlos se produjo una mezcla heterogénea ya que podíamos distinguir 2 fases, la de la sal y la del yodo, al calentarlos el yodo pasó de estado sólido a estado gaseoso, un poco de éste se mantuvo en la cápsula mezclado con la sal lo que le dio a ésta ese color morado pálido. Los cristales del vidrio de reloj se produjeron porque al enfriarse el yodo se condensó en el virio, estaba en estado sólido ya que no pasa por el estado líquido, sólo se sublima en ambos sentidos. No tomamos masa de los instrumentos pero sabemos que la sal se recuperó por completo, con un ligero aumento de volumen ya que estaba mezclada con yodo, por lógica podemos deducir que el volumen del vidrio con los cristales de yodo aumentó en proporción de la masa de los cristales, no hubiéramos recuperado todo el yodo ya que una parte de éste se liberó al aire en forma de gas.
Conclusiones:
Concluimos que en todos los experimentos utilizamos mezclas ya que las pudimos separar con método físicos,
Cuestionario:
Investigue cuando menos otras tres técnicas de separación de mezclas, explique cada una de ellas.
La decantación: Esta técnica sólo sirve para separar líquidos inmiscibles (que no se mezclan) como el agua y el aceite, esto se hace en una probeta y se deja que los líquidos se asienten, cuando esto sucede se abre la llave y se jeja fluir el líquido que está hasta el fondo.
La Cristalización: Esta técnica se usa para separar un sólido disuelto en un líquido, la mezcla se coloca en un recipiente llamado cristalizador y se deja que le liquido se evapore.
La Tamización: Se usa para separar dos sólidos que tienen partículas de diferente tamaño, por medio de un colador o harnero, cayendo las más pequeñas y reteniendo las más grandes
Investigue una técnica de separación de mezclas que utilice un equipo eléctrico, explique.
Cromatografía: En esta técnica se utiliza un aparato que se llama cromatógrafo de gases. Este instrumento separa a la muestra en todos sus componentes, fundiéndola y registrando que temperatura ese componente se quemó, es aparato lógicamente funciona con electricidad.
Investigue dos tipos de destilación y explique cada uno de ellos.
Destilación simple: cuando se separa una sustancia muy volátil de unas no tan volátiles.
Destilación compuesta o fraccionada: Cuando las sustancias no son muy volátiles.
Destilación seca: cuando los productos volátiles se obtienen de cuerpos sólidos en recipientes cerrados y bajo la acción del calor, como ocurre con el gas del alumbrado.
Investigue el término “azeótropo”
Azeótropo: Mezcla Azeotrópica; Azeotrópica: Dicese de una mezcla de dos líquidos que destila a temperatura constante produciendo, a determinada presión, un vapor de composición fija.
Investigue Los términos “aleación” y “amalgama”
Aleación: Combinación de metales; puede ser una mezcla o un compuesto de estos.
Amalgama:
Aleación en la cual uno de los componentes es mercurio.
Bibliografía:
http://biblioteca.itesm.mx/cgi-bin/nav/salta?cual=www:48835
http://www.ula.ve/admision/Boletin_NutricionDietetica.htm
http://biblioteca.itesm.mx/cgi-bin/nav/salta?cual=www:48034
Tec de Monterrey Campus Qro.
Preparatoria
Química Inorgánica-1:00 PM
26 de marzo del 2003
- 5 -
Descargar
| Enviado por: | Moe |
| Idioma: | castellano |
| País: | México |
