Química
Cristalización
INTRODUCCIÓN TEÓRICA
¿Qué es un cristal? Un cristal es un cuerpo sólido que debido a su estructura interna adopta naturalmente una configuración geométrica, limitada por caras planas.
¿Cómo se puede conseguir un cristal? Mediante la cristalización, que consiste en separar una substancia en forma sólida a partir de su disolución, debido a sobrepasar la concentración de saturación de la misma.
HIPÓTESIS
*Tras un disolución hay que aumentarle la concentración evaporando el agua. Esta operación será la que permitirá la aparición de cristales, tras una saturación, como se dice en la introducción.
*A más cantidad de soluto, mayor serán los cristales.
*Los cristales se unirán mediante una estructura que tendrá una forma.
MATERIALES Y PRODUCTOS
*Erlenmeyer
*Trípode
*Rejilla de amianto
*Mechero
*Embudo
*Papel de filtro
*Lupa
*Sulfato de cobre
*Dicromato potásico
PASOS A SEGUIR PARA REALIZAR LA PRÁCTICA.
Montamos el trípode y el aro, y colocamos el mechero debajo.
En un erlenmeyer, vertemos 15gr. del producto y disolvemos con agua. (de 125ml. a 150ml. si es sulfato de cobre y de 200ml. a 225ml. si es dicromato potásico).
Se enchufa el mechero y se pone a calentar la disolución.
Esperar hasta que el agua se evapore hasta unos 45 ml. y empiece a saltar el producto del interior.
Enfriamiento rápido: Enfriamiento lento: _
Se saca el producto y se Se saca el producto y se
coloca a chorro de agua coloca en algún lugar fresco
fresca continua varios con el fin de que cristalice
minutos hasta que el con un cambio de temperatura
producto cristalice. Natural en un par de días.
Una vez cristalizado, observar los cristales por la lupa, filtrándolo con anterioridad para que no se pierda ningún cristal
TABLA
| | gr. producto | ml. agua | Tamaño cris.(mm) | Forma cris. |
| Sulfato de cobre (lenta) | 15 | 125 | 12 | Rombo |
| Sulfato de cobre(rápida) | 15 | 150 | 0.8 | Rombo |
| Sulfato de cobre(lenta) | 15 | 125 | 7 | Rombo |
| Dicromato potásico(lenta) | 15 | 200 | 0.5 | Rectángulo |
| Dicromato potásico(rápida) | 15 | 225 | 0.2 | Rectángulo |
| Sulfato de cobre y Dicromato potásico(lenta) |
7.5 y 7.5 |
180 |
1 | Irregular, en su mayoría, rectángulo con puntas de rombo |
GRÁFICA
OBSERVACIONES
Hemos observado que el sulfato de cobre, hace los cristales con más facilidad que el dicromato potásico.
El resultado obtenido respecto al tamaño de los cristales en sulfato de cobre, ha dependido del aumento de la concentración cuando la disolución hecha con anterioridad, estaba a una temperatura superior a la inicial. Realizada la evaporación de casi en su totalidad del agua, se enfría de algunas de las dos formas nombradas en los pasos a seguir para realizar la práctica. Una vez enfriado, sus partículas se agrupan en formas de rombo de color azul, de distintos tamaños según el aumento de la concentración.
(forma del cristal)
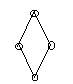
En el dicromato potásico, se realizan las mismas operaciones. Una de las cosas que más nos ha llamado la atención, ha sido que no es tan soluble, puesto que la cantidad puesta de agua, siempre ha sido muy superior (de 200 a 225ml.). Al observarlo en la lupa, vemos que sus partículas se agrupan en forma de rectángulo de color naranja. El aumento de su concentración, no se aprecia a simple vista en el tamaño de los cristales, éstos muy pequeños, y con la lupa es prácticamente inapreciable.
(forma del cristal)
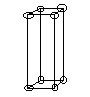
La mezcla del sulfato de cobre y el dicromato potásico resultó muy curiosa. Las agrupaciones de sus partículas hizo formas muy irregulares, había en su mayoría rectángulos con puntas de rombo, pero también habían rectángulos. Eran de color marrón oscuro
(forma de cristal
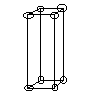
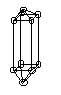
El enfriamiento lento logra unos cristales más grandes que el rápido.
CONCLUSIONES
Esta práctica nos ha llevado a saber que un cristal se forma por una saturación del producto en el agua, y que así, cuando llega a su temperatura natural, las partículas se ven obligadas a juntarse. Si se enfría naturalmente, los cristales son de mayor tamaño porque se juntan poco a poco; el hacerla rápida, le obligas al producto a juntarse en escaso tiempo y por eso los cristales son más pequeños.
También hemos llegado a la conclusión de que la forma depende del producto, porque al juntar los dos productos, la forma era una mezcla de los dos.
Hemos comprobado que los cristales se obtienen por saturación de un producto en agua, porque cuando más le hemos aumentado su concentración, los cristales tenían mayor tamaño.
Podemos decir, también, que un cristal no es solo un rombo (en el caso del sulfato de cobre) o un rectángulo (en el caso del dicromato potásico), sino que son muchas agregaciones de éstas, puesto que dentro de una figura de éstas, hay más de las mismas. Dicho esto, solo queda decir que cuando rompes un trozo de cristal, se hace en muchos pedazos de la forma que formen sus partículas, puesto que el contorno de su forma es lo más débil del cristal.
Descargar
| Enviado por: | RAFAEL |
| Idioma: | castellano |
| País: | España |
