Ingeniero Químico
Análisis de aguas
Instituto Politécnico Nacional
Escuela Superior de Ingeniería Química e Industrias Extractivas
Laboratorio de Química Analítica II
Práctica #1:”Análisis de aguas: determinación de cloruros, alcalinidad, dureza total, dureza de calcio, dureza de magnesio, sulfatos y sílice”
Fecha de entrega: 24 de septiembre de 2009
“Análisis de Aguas”
Determinación de Cloruros, Alcalinidad, Durezas, Sulfatos y Sílice
Objetivos generales:
-
Determinar el contenido de iones presentes en muestras de agua, que son considerados como sustancias indeseables o impurezas y a partir de los resultados de estos análisis se tendrá la pauta para seleccionar los tratamientos requeridos para su purificación.
-
Determinar los parámetros principales requeridos para establecer la calidad del agua para alimentación a generadores de vapor (calderas), que sirve como ejemplo a los análisis que se llevan a cabo en diferentes tipos de agua. El resultado de estos análisis sirve de base para la selección de equipos y procesos de tratamiento.
-
Efectuar las determinaciones de dureza total, parcial, alcalinidad, cloruros, sílice y sulfatos utilizando las técnicas analíticas correspondientes.
Cloruros
Nota: Datos y resultados tomados de 6A
Reacciones de valoración de la disolución titulante:
Blanco
Rojo Ladrillo
Reacciones de la muestra problema:
Alcalinidad
Reacciones de valoración de la disolución titulante:
Reacciones de la muestra problema:
Dureza
Reacciones de valoración de la disolución titulante:
![]()
Complejo inestable incoloro complejo estable azul
Reacciones de la muestra problema:
[Ca-Mg--ENT] + EDTA ------------->[Ca-Mg--EDTA] + ENT
Complejo inestable incoloro complejo estable azul
[Ca--ENT] + EDTA ------------->[Ca--EDTA] + ENT
Complejo inestable incoloro complejo estable purpura
[Mg--ENT] + EDTA ------------->[ Mg--EDTA] + ENT
Complejo inestable incoloro complejo estable azul
Sulfatos
Reacción de la muestra problema:
![]()
Sílice
Nota: Datos y resultados tomados de 6B ÚNICAMENTE PARA SÍLICE
Reacciones de la muestra problema:
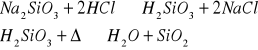
Tabla de preparación de disoluciones utilizadas en el análisis de cloruros
| Soluto | Solvente | Concentración | Volumen | Tipo de solución |
| AgNO3 | Agua | 0.02 N | 1000 ml | Sólido líquido |
| K2CrO4 | Agua | 0.5% | 100 ml | Sólido líquido |
Tabla de preparación de disoluciones utilizadas en el análisis de alcalinidad
| Soluto | Solvente | Concentración | Volumen | Tipo de solución |
| HCl | Agua | 0.02 N | 1000 ml | liqudo líquido |
| AM | Agua | 100ml | liquido líquido | |
| K2CrO4 | Agua | 0.5% | 100 ml | Sólido líquido |
Tabla de preparación de disoluciones utilizadas en el análisis de dureza
| Soluto | Solvente | Concentración | Volumen | Tipo de solución |
| EDTA | Agua | 0.02 N | 1000 ml | Liquido-solido |
| ENT | Etanol y aforar con trietanolamina | 0.5% | 100ml | Liquido-líquido |
| NaOH | Agua destilada | 0.1 N | 100 ml | Sólido-líquido |
| Buffer(NH4Cl/(NH4)OH) | Agua destilada | pH 10 | 250 ml | Solido-solido |
| Murexida | Cloruro de potasio | 0.2 % | 100 g | Solido/solido |
Tabla de preparación de disoluciones utilizadas en el análisis de sulfatos
| Soluto | Solvente | Concentración | Tipo de solución |
| Na2SO4 | Agua | 0.1 mg SO4/ml sol´n | Sólido líquido |
| BaCl2 2H2O | Agua | 2.5%w | Sólido líquido |
| Glicerina | Etanol | (1:1) | Líquido líquido |
| NaCl | HCl/H2O | ………… | Sólido líquido |
Tabla de preparación de disoluciones utilizadas en el análisis de Sílice
| Soluto | Solvente | Concentración | Tipo de solución |
| HR Silica molibdate | Agua | 10% | Sólido líquido |
| HR silica acid RCT | Agua | Sólido líquido | |
| Silica citric acid | Agua | 10% | Sólido líquido |
Procedimiento de preparación de disoluciones utilizadas
PROCEDIMIENTO GENERAL PARA UNA SOLUCIÓN SOLIDO LÍQUIDO
PROCEDIMIENTO GENERAL PARA UNA SOLUCIÓN LIQUDO LÍQUIDO
Procedimiento de valoración
PREPARACIÓN DEL SÍLICE
Tabla de datos experimentales
| Análisis de cloruros | ||||
| Volumen de AgNO3 | Normalidad promedio | Volumen de muestra | ||
| 6.6 ml | 0.0193 | 20 ml | ||
| Análisis de Alcalinidad | ||||
| Volumen de HCl | Normalidad promedio | Volumen de muestra | ||
| 7.5 ml | 0.0184 | 20 ml | ||
| Carbonatos y Bicarbonatos | ||||
| Volumen de la fenoftaleina | Volumen del anaranjado de metilo | |||
| 0.4ml | 7.2ml | |||
| Análisis de Durezas | ||||
| Normalidad promedio | Titulo promedio | Volumen de muestra | ||
| 0.0197 | 0.9476 | 20 ml | ||
| Volumen de EDTA dureza total | Volumen de EDTA dureza calcio | Volumen de EDTA dureza magnesio | ||
| 7.5 ml | 6.6 ml | 4.6 ml | ||
| Análisis de sulfatos | ||
| Absorbancia leída | Concentración | Volumen de muestra |
| 0.035 | 0.75 | 20 ml |
| Análisis de sílice | ||
| Absorbancia leída | Concentración | Volumen de muestra |
| 0.462 | 53 | 20 ml |
Tabla de absorbancia para sulfatos
| Patrón | A | Concentración SO42- | Mg SO42- |
| Blanco | 0 | 0 | 0 |
| 1 | 0.024 | 0.5 | 0.5 |
| 2 | 0.049 | 1 | 1 |
| 3 | 0.075 | 2 | 2 |
| 4 | 0.081 | 3 | 3 |
| 5 | 0.106 | 4 | 4 |
| 6 | 0.196 | 5 | 5 |
Tabla de absorbancia para sílice
| Patrón | A | Concentración |
| Blanco | 0 | 0 |
| 1 | 0.267 | 29.5 |
| 2 | 0.37 | 40.9 |
| 3 | 0.385 | 42.5 |
| 4 | 0.4 | 43.3 |
| 5 | 0.429 | 47.4 |
| 6 | 0.549 | 60.7 |
Curvas de calibración para sulfatos y sílice
SULFATOS
SILICE
Tabla de resultados por cada integrante del equipo
4A
| ANÁLISIS | PEq | ppm | epm |
| pH aproximado | Básico | ||
| Tipo de dureza | TEMPORAL Y PERMANENTE | ||
| Dureza total como CaCO3 | 100/2 | 409.36 | 8.1872 |
| Alcalinidad total como CaCO3 | 100/2 | 430.99 | 8.6198 |
| Calcio, Ca2+ | 40/2 | 111.20 | 5.56 |
| Magnesio. Mg2+ | 24.31/2 | 31.79 | 2.6154 |
| Sodio, Na1+ | 23/1 | 206.885 | 8.995 |
| Hidróxidos, OH- | ----- | ----- | ----- |
| Carbonatos, CO32- | 60/2 | 39.74 | 1.3247 |
| Bicarbonatos, HCO3- | 61/1 | 222.23 | 3.6431 |
| Cloruros, Cl- | 35.5/1 | 166.941 | 4.7026 |
| Sulfatos, SO42- | 96/2 | 360 | 7.5 |
| Sílice como SiO2 | 60/2 | 47.6 | 1.5867 |
| Sólidos totales disueltos | 1186.381 | ||
4B
| ANÁLISIS | PEq | ppm | epm |
| pH aproximado | Básico | ||
| Tipo de dureza | TEMPORAL Y PERMANENTE | ||
| Dureza total como CaCO3 | 100/2 | 236.9 | 4.738 |
| Alcalinidad total como CaCO3 | 100/2 | 487.6 | 9.752 |
| Calcio, Ca2+ | 40/2 | 64.44 | 3.222 |
| Magnesio. Mg2+ | 24.31/2 | 18.42 | 1.5154 |
| Sodio, Na1+ | 23/1 | 312.15 | 13.572 |
| Hidróxidos, OH- | ----- | ----- | ----- |
| Carbonatos, CO32- | 60/2 | 33.12 | 1.104 |
| Bicarbonatos, HCO3- | 61/1 | 230.1 | 3.7721 |
| Cloruros, Cl- | 35.5/1 | 99.34 | 2.7983 |
| Sulfatos, SO42- | 96/2 | 475.00 | 9.8962 |
| Sílice como SiO2 | 60/2 | 65.100 | 2.1685 |
| Sólidos totales disueltos | 1063.1 | ||
6A
| ANÁLISIS | PEq | ppm | epm |
| pH aproximado | Básico | ||
| Tipo de dureza | TEMPORAL Y PERMANENTE | ||
| Dureza total como CaCO3 | 100/2 | 502.22 | 10.044 |
| Alcalinidad total como CaCO3 | 100/2 | 349.92 | 6.9984 |
| Calcio, Ca2+ | 40/2 | 125.08 | 6.254 |
| Magnesio. Mg2+ | 24.31/2 | 52.95 | 4.3562 |
| Sodio, Na1+ | 23/1 | 140.109 | 6.0917 |
| Hidróxidos, OH- | ----- | ----- | ----- |
| Carbonatos, CO32- | 60/2 | 22.08 | 0.736 |
| Bicarbonatos, HCO3- | 61/1 | 381.61 | 6.2559 |
| Cloruros, Cl- | 35.5/1 | 225.78 | 6.36 |
| Sulfatos, SO42- | 96/2 | 162.5 | 3.38 |
| Sílice como SiO2 | 60/2 | 52.5 | 1.0938 |
| Sólidos totales disueltos | 1162.609 | ||
6B
| ANÁLISIS | PEq | ppm | epm |
| pH aproximado | Básico | ||
| Tipo de dureza | TEMPORAL Y PERMANENTE | ||
| Dureza total como CaCO3 | 100/2 | 530.65 | 10.613 |
| Alcalinidad total como CaCO3 | 100/2 | 358.8 | 7.176 |
| Calcio, Ca2+ | 40/2 | 113.71 | 5.6855 |
| Magnesio. Mg2+ | 24.31/2 | 87.50 | 7.1987 |
| Sodio, Na1+ | 23/1 | 449.63 | 19.549 |
| Hidróxidos, OH- | ----- | ----- | ----- |
| Carbonatos, CO32- | 60/2 | 44.16 | 1.472 |
| Bicarbonatos, HCO3- | 61/1 | 488.24 | 8.0039 |
| Cloruros, Cl- | 35.5/1 | 167.86 | 4.7285 |
| Sulfatos, SO42- | 96/2 | 875 | 18.229 |
| Sílice como SiO2 | 60/2 | 53 | 1.767 |
| Sólidos totales disueltos | 2279.1 | ||
Conclusiones
Evaluando los datos obtenidos en el análisis de la muestra de agua proporcionada, se pueden obtener las siguientes conclusiones:
El agua contiene simultáneamente dureza temporal y permanente, NO ES UTIL COMO AGUA POTABLE.
Las aguas con dureza temporal se pueden ablandar hirviéndolas o calentándolas lo suficiente. Con este método de purificación el CO2 es liberado, formándose precipitados relativamente insolubles de calcio y magnesio (CaCO3, MgCO3).
Si esta agua se utiliza para equipos como generadores de vapor o intercambiadores de calor, las incrustaciones que se obtendrán, si no se trata, son más blandas y porosas que con dureza permanente.
El pH del agua es mayor a 7, es decir, tiene un pH alcalino, por lo cual se puede utilizar como agua de alimentación en una caldera, ya que si el agua es alcalina se obtendrá menor corrosión.
Cuando el agua tiene simultáneamente dureza temporal y permanente, como en este caso, se utiliza para tratarla: cal (absorbe el CO2) y sosa, esta produce la descomposición de los sulfatos, la precipitación de carbonato cálcico insoluble, y la formación de sulfato sódico soluble:
CaSO4 + Na2CO3 CaCO3 + Na2SO4
CaCl2 + Na2CO3 CaCO3 + 2NaCl
Guardar en un frasco reactivo y etiquetar
Disolver con parte del solvente
Aforar y homogeneizar
Pesar el soluto en un vaso de precipitados.
Tomar con una pipeta graduada el acido
Agregar el acido a un vaso de pp con parte del disolvente
Verter un poco de acido en un vaso de precipitados
Guardar en un frasco reactivo y etiquetar
Aforar y homogeneizar
Titular con la solución de titulante hasta el vire acordado
Agregar indicador.
Pesar Xg de solución patrón. Disolver con agua destilada.
Por último, agregar el silica acid citric y leer la absorbancia en el espectofotómetro
Agregar a la muestra HR Silica Molibdate y dejar reposar por 2 minutos
Agregar a la muestra HR Silica Acid RCT, agitar cada dos minutos y dejar reposar, hasta completar 10 minutos
Descargar
| Enviado por: | El remitente no desea revelar su nombre |
| Idioma: | castellano |
| País: | México |
