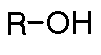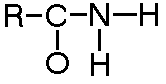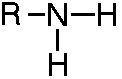Laboratorio
Química orgánica
Química Orgánica
La química orgánica es el estudio de los compuestos que en su estructura contienen carbono. El termino lo debemos a una clasificación muy antigua dada según la procedencia del compuesto, según ésta clasificación los compuestos inorgánicos eran aquellos que provenían de los minerales y por el contrario los compuestos orgánicos son los que provienen de fuentes vegetales y animales, de hecho hasta 1850 los químicos creían que los compuestos orgánicos provenían de los organismos vivos.
Hasta la fecha no se creía que las sustancias orgánicas se pudieran sintetizar a partir de sustancias inorgánicas, sin embargo en el año 1882, el químico Friedrich Wohler (1800-1882), logro sintetizar el primer compuesto orgánico calentando casualmente cianato amónico, considerado un compuesto inorgánico, descubrió sorprendido que este se había transformado en urea, producto de excreción de los seres vivos.
Entre las diferencias que podemos establecer entre las moléculas orgánicas de las inorgánicas es la cantidad de átomos que la están formando (3 ó 4 átomos) en el caso de las inorgánicas y las orgánicas por un gran conglomerado de estos, los cuales se comportan de acuerdo con sus características físicas y químicas para establecer sus relaciones con otros átomos. Existe una gran variedad de Compuestos Orgánicos, tanto así que se contabilizan más de diez millones de ellos, dadas las circunstancias debe haber una denominación para cada uno de ellos para estos los clasificaremos de la siguiente manera
Nomenclatura Orgánica
Alcanos
Están constituidos por H y C , a su vez unidos por enlaces covalentes polares, se consideran hidrocarburos saturados, ya que estos no poseen en su estructura enlaces múltiples.
Para nombrar los alcanos debemos primero tener en claro que utilizaremos sufijos y prefijo los cuales se en el caso de los prefijos serán utilizados de acuerdo a la cantidad de átomos de carbono que posea la molécula:
Sufijo: ano
Prefijo:
Cantidad de (C)
Met: 1
Et:2
Prop:3
But:4
Pent: 5
Hex: 6
Hept: 7
Oct: 8
Nona: 9
Deca: 10
Dentro de los alcanos están también los alcanos ramificados; estos pueden estar constituidos por cadenas cortas. Con menos de 5 átomos de Carbono se encuentran en estado gaseoso, entre 5 a 17 átomos de carbono en estado liquido y con más de 17 carbonos en su estructura son generalmente compuestos sólidos. Los alcanos se pueden ramificar con grupos sustituyentes como por ejemplo:
-CH3 : Metil
-CH2-CH3 : Etil
-CH2-CH2-CH3 : Propil
-CH2-CH2-CH2-CH3 : Butil.....
Alquenos
Son hidratos de carbono insaturados que en su estructura poseen enlaces múltiples (dobles enlaces) se definen mediante la siguiente estructura:
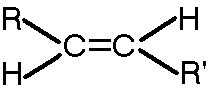
Para nombrar estos compuestos utilizaremos los mismos prefijos nombrados con anterioridad dependiendo de la cantidad de carbonos e incluiremos en vez de la terminación ano vamos a usar el sufijo ENO.
Alquinos
Son Hidratos de Carbono insaturados, poseen enlaces múltiples (enlaces triples) se define mediante la siguiente estructura:
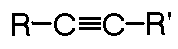
Para nombrar estos compuestos utilizaremos los mismos prefijos que los dos anteriores pero el sufijo en este caso serán INO.
Funciones orgánicas
Son las siguientes:
Nombre Estructuras
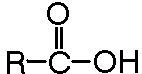
| Ácido Carboxílico |
| Fórmula: R-COOH | Sufijo: -oico |
| Alcohol |
| Fórmula: R-OH | Sufijo: -ol |
| Aldehído | Fórmula: R-CHO | Sufijo: -al | |
| Cetonas | Fórmula: R-CO-R' | Sufíjo: -ona | |
| Eter |
| Fórmula: R-O-R' | Sufijo: Eter |
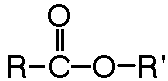
| Ester |
| Fórmula: R-COO-R' | Sufijo: -oato de R' |
| Amida |
| Fórmula: R-CO-NH2 | Sufíjo: -amida |
| Amina |
| Fórmula: R-NH2 | Sufíjo: -amina |
Isomería
Reciben este nombre aquellos compuestos químicos que, poseyendo la misma fórmula molecular (el mismo número de cada tipo de átomos), tienen éstos distribuidos de distinta manera en la estructura de sus respectivas moléculas.
Isómeros de función
Son aquellos que tienen igual formula global paro distinto grupo funcional.
Isómeros de esqueletos
Tienen igual numero global pero diferente estructura carbonada.
Datos importantes del Carbono
Configuración electrónica: 1s2 2s2 2p2
Electronegatividad: 2.55
Estructura cristalina: Hexagonal
Usos: El acero es una aleación de acero y carbono; en todos los combustibles fósiles (petróleo, carbón, gas natural); grafito (lápices, filtros, lubricantes).
Hidrocarburos (CH)
Alifáticos
Aromáticos
Alcanos
Ciclo alcanos
Alquenos
Alquinos

Descargar
| Enviado por: | Alexanders Pizarro |
| Idioma: | castellano |
| País: | Chile |