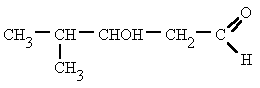Química
Alcoholes
INSTITUTO CULTURAL SUCRE, A.C.
SECCIÓN PREPARATORIA
ALCOHOLES
PRÁCTICA No. 17
Objetivo:
Reconocer las propiedades físicas y químicas de los alcoholes.
Investigación.
¿Cuál es y como se llama el grupo funcional que caracteriza a los alcoholes?
¿Cómo se clasifican los alcoholes monovalentes saturados?
Nomenclatura de los alcoholes
Se nombran como los hidrocarburos de los que proceden, pero con la terminación "-ol", e indicando con un número localizador, el más bajo posible, la posición del grupo alcohólico. Según la posición del carbono que sustenta el grupo -OH, los alcoholes se denominan primarios, secundarios o terciarios.
|
|
| 2-butanol |
Si en la molécula hay más de un grupo -OH se utiliza la terminación "-diol", "-triol", etc., indicando con números las posiciones donde se encuentran esos grupos. Hay importantes polialcoholes como la glicerina "propanotriol", la glucosa y otros hidratos de carbono.
|
|
| 1,2,3-propanotriol ou glicerina |
Cuando el alcohol non es la función principal, se nombra como "hidroxi-", indicando el número localizador correspondiente.
|
|
| 3-hidroxi-4-metil-pentanal |
Escribe la formula semi-desarrollada y el nombre común de los siguientes alcoholes:
-
Metanol
| CH3OH | Metanol | Alcohol metílico |
-
Etanol
-
Propanol
-
Butanol
-
Pentanol
-
Pentanol II
-
propiedades físicas en general de los alcoholes
-
reacción del etanol con:
-
acido yodhídrico
-
deshidratación de dos moléculas de etanol
-
deshidratación de una molécula de etanol
-
reacción con el sodio
-
reacción con el acido acético
-
reacciones de oxidación de:
-
alcoholes primarios
-
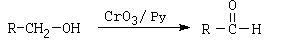
-
alcoholes secundarios
-
alcoholes terciarios
-
oxidación avanzada de los alcoholes
-
métodos de identificación de los alcoholes primarios, secundarios y terciarios.
-
Solubilidad: Coloca 1ml de cada alcohol en los tubos y agrega a c/u 1ml de agua. Anota tu observación.
-
Formación de alcoholato: Agrega un trocito de sodio a 1ml de etanol y observa la reacción. Acerca un cerillo encendido a la boca del tubo y anota lo que observes.
-
Oxidación moderada: Agrega 1ml de etanol a 5ml de solución de dicromato de potasio, acidificada con HSO4. Calienta con cuidado ligeramente y aprecia el olor de la sustancia formada. Anótalo.
-
Esterificacion: Agrega a 1ml de etanol 1ml de acido acético y 1ml de HSO4. Calienta con cuidado ligeramente y aprecia el olor de la sustancia formada. Anótalo.
-
Oxidación avanzada: En dos capsulas coloca etanol y alcohol isoamílico, respectivamente. Enciéndelas y anota lo que observes.
-
Identificación de etanol: a 2ml de etanol añade 2ml de solución yodo yodurada hasta formar un precipitado amarillo que se reconoce por su olor. Anótalo.
-
¿Cuál es la solubilidad de cada alcohol en el agua?
-
¿Por qué ocurre el cambio de color en el experimento “c”?
-
Escribe la ecuación de la reacción que se produjo en el experimento “c”
-
Escribe la ecuación de la reacción del experimento “b”
-
“ “ “ “ esterificación (exp. “d”).
-
Escribe las características de las flamas de los alcoholes utilizados y las ecuaciones respectivas
-
Escribe la ecuación por lo cual identificaste al etanol
| CH3CH2OH | Etanol | Alcohol etílico |
| CH3CH2CH3 | Propano | - No hay - |
| CH3(CH2)3OH | 1-Butanol | Alcohol butílico |
| CH3(CH2)4OH | 1-Pentanol | Alcohol pentílico |
Los alcoholes pueden formar enlaces mediante puentes de hidrógeno ,lo que causa que estos compuestos tengan puntos de ebullición más altos que los correspondientes haloalcanos.
Se utiliza la Piridina (Py) para detener la reacción en el aldehído
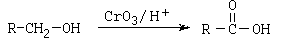
Cr03 / H+ se denomina reactivo de Jones
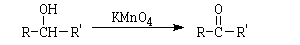
No se oxidan
| MATERIALES | SUSTANCIAS |
| Gradilla | Etanol |
| Tubos | Metanol |
| 2 capsulas de porcelana | Alcohol anílico |
| Pipetas | Alcohol isoamílico |
| Solución de hidróxido de sodio al 10% | |
| Solución yodo yodurada | |
| Solución de dicromato de potasio | |
| Sodio metálico | |
| Acido sulfúrico |
Desarrollo:
Reporte:
Conclusión:
Bibliografía:
Química Orgánica, Lee Summerlin y Lynn Jackson. Publicaciones Cultural, SA de CV 24ta ed. México 1986
Descargar
| Enviado por: | Krloz Hdt |
| Idioma: | castellano |
| País: | México |