Biología, Botánica, Genética y Zoología
Priones
Introducción
El presente trabajo es el resumen de los contenidos del panel de biología celular. Este busca explicar y responder si los priones agentes patógenos formados solo por una proteína poseen un medio de propagación convencional (multipliación) o un método nuevo y exclusivo como la reclutación.
Todos estos estudios apuntan a comprender el mecanismo de enfermedades mortales que afectan tanto a los animales como al ser humano, para nosotros este estudio es importante para comprender los medios moleculares que esto implica y las relaciones que podemos establecer con la cátedra.
Es por eso que siguiendo la metodología guiamos nuestro panel a través del método cientifico y plantamos como hipotesis que los priones se reclutan,nuestro principal objetivo es contrarrestar y probar la hipotesis, ya sea demostrando las diferencias proteicas existentes o las diferencias marcadas con otros agentes patógenos estudiados como lo son los virus y las bacterias.
Desarrollo
En la decada de 1950, el doctor Carleton Gajdusek estudiaba en Nueva Guinea una enfermedad fatal del sistema nervioso que se conoce como “Kuru” (escalofrio) esta enfermedad afectaba a una tribu canibal llamada Fore, lo interesante de todo esto era que la enfermedad no correspondia con ningun modelo anteriormente estudiado (ya sea virus, bacteria) especialmente en la transmisión de la enfermedad.
Al paso del tiempo en 1959 el veterinario Wj. Hadlow puso de manifiesto las similitudes entre el “Kuru” y el “Scrapie” (tembladera) de los ovinos, y más interesante aun estas enfermedades tenian similitudes con la enfermedad de “Creutzfeldt-Jakob” CJD (Creutzfeldt-Jakob dissease) una curiosa demencia presenil que se presentaba en la población humana a principios del siglo XX. De manera más importante en el reino unido estaba ocurriendo un extraño mal al ganado Bovino , al parecer los animales estaban sufriendo daños de tipo nervioso por un agente infeccioso no convencional (Encefalopatia espongiforme) “vacas locas”. Todas estas patologías convergen en un mismo ente infeccioso “EL PRION”.
Estos agentes patógenos formados por una proteína ( proteína del prión o PPr ) Producen entre otras, la enfermedad de las "vacas locas" o encefalopatía bovina espongiforme. Esta proteína se acumula en el cerebro de animales enfermos , dando lugar a la estructura esponjosa de la corteza cerebral que da nombre a la enfermedad.
El Prión, proteína codificada por un gen celular, presenta dos isoformas: normal (PrP) y anormal (PrPcs) o infecciosa. La proteína del prión normal tiene una secuencia de aminoácidos (estructura primaria) idéntica a la proteína de prión patógena. La diferencia entre las dos recae en la estructura secundaria y terciaria, o sea, en su plegamiento.
En humanos, el gen que codifica para PrP se ha localizado en el brazo corto del cromosoma 20. Schnittger determinó que dentro de la región 20p12-pter, el locus es pter-PRP-SCG1. El gen completo ha sido secuenciado y se ha visto la secuenciación para la proteina Prp.
La forma de propagación del carácter infeccioso se debe a una reacción en cadena cuando una proteina patogena (PrpCs) (rica en estructura 2ria láminas beta) induce a una cambio configuracional a una proteina sana Prp.
Este cambio de configuración es crucial, ya que las proteínas con láminas beta son muy resistentes a las enzimas proteolíticas, al calor y no se disuelven en agua. Pero sobre todo, la proteína alterada tiene una característica única: interacciona con una molécula de proteína normal, le cambia la conformación y la hace capaz de convertir las estructuras de más proteínas normales. Ahí radica el poder infectivo de los priones.
Ya producida la proteína anómala, su contacto con las cadena PrP, modifica a estas últimas y el proceso se amplifica de manera exponencial. PrPsc se combina con Prp y produce dos moléculas PrPsc, en un segundo ciclo las dos moléculas de PrPsc de combinan con PrP y producen cuatro moléculas de PrPsc, y así sucesivamente. La presencia de PrP parece ser indispensable, y de hecho, modelos carentes o nulos de PrP ( ratones transgénicos knockout) inoculados con material cerebral infectado con scrapie no desarrollan la enfermedad.

Proteina sana PrP ;Proteina patógena PrPsc ; Inducción al cambio de estructura
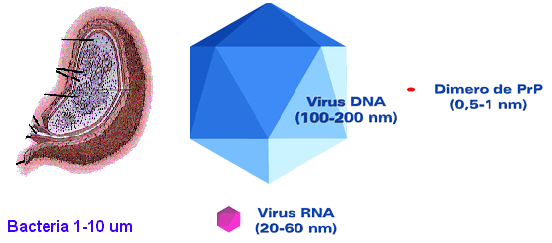
Es importante esclarecer las diferencias entre los patogenos conocidos y los priones para darnos cuenta que estos carecen de acidos nucleicos (DNA y RNA) macromolecula fundamental en la replicación en donde todas las formas de vida incluida los virus desde bacterias plantas y animales transmiten sus caracteres a las siguientes generaciones a través de algun acido nucleico.
| Bacterias | Virus | PRIONES |
| Poseen un genoma de DNA que sirve de base para la herencia genetica | Poseen un genoma formado por un acido nucleico que sirve de molde para la replicación. | Carece de acidos nucleicos, en la particula infecciosa. |
| Estan compuestos de acidos nucleicos, ribosomas, membranas y macromoleculas. | Estan compuestos por acidos nucleicos ,proteinas y generalmente otros componentes | El unico componente es la proteina PrPsc |
| Induce una respuesta inmune | Induce una respuesta inmune | No inducen una respuesta inmune |
| Puede replicarse por fisión u otros metodos. | Trnscribe e inserta el genoma en una celula huesped para poder ocupar la maquinaria enzimatica de esta y reproducirse. | Induce una cambio conformacional para reclutar mas proteinas patogenas y asi propagarse |
Grandes cantidades de péptidos anormales se acumulan dentro de las estructuras que forman parte del mecanismo endocítico de las neuronas (lisosomas) y ello es lo que desencadena la vacuolización y la muerte de dichas células.
El cambio característico en estas encefalopatías es la degeneración espongiforme, difusa o relativamente focal. En ella, la vacuolización ocurre en el citoplasma de neuronas y células gliales.
Conclusión
Como lo expresa el dasarrollo queda claro que es el reclutamiento la forma en la cual los priones se propagan y que es un sistema muy diferentes a lo de otros seres patógenos, la diferencia queda marcada por una diferencia en la forma de las proteinas .Esto para nosotros es importante a nivel de estudio en biología celular ya que se refiere directamente a configuraciones proteicas como lo son alfa hélice y beta hoja plegada y nos demuestra lo importante y crucial que son las formas que adquieren los aminoacidos.
A medida que nuestro conocimiento avanza podremos entender los fenómenos básicos que engloban enfermedades mortales como lo son las encefalopatias espongiformes (mal de las vacas locas) e ir formandonos una idea de lo que vendra en un futuro proximo con los cimientos que nos entrega la biología celular.
Entonces debido a la investigación biblográfica y al estudio correspondiente los principales objetivos se han cumplido a cabalidad de manera óptima.
Biblografía
Stanley B. Prusiner. Prions. Proceedings of the National Academy of Sciece of the USA. Vol. 95 - issue 23 - . 13363-13384 pp.
http://recol.es/comunidades/veterinaria/eeb/priones/priones.htm#bio (31 de octubre)

Descargar
| Enviado por: | Hugo González |
| Idioma: | castellano |
| País: | Chile |
