Química
Preparación de soluciones
PRÁCTICA #1
PREPARACIÓN DE SOLUCIONES
OBJETIVO: Preparar soluciones normales, molares y porcentuales
INTRODUCCIÓN:
La composición de una solución se debe medir en términos de volumen y masa, por lo tanto es indispensable conocer la cantidad de soluto disuelto por unidad de volumen o masa de disolvente, es decir su concentración. Durante cualquier trabajo experimental, el uso de soluciones se hace indispensable, por lo que es necesario conocer los procedimientos para su elaboración. En la presente práctica se realizarán soluciones utilizando como concentración la molaridad, la normalidad y las relaciones porcentuales.
MARCO TEÓRICO
Solución
Una solución es una mezcla homogénea cuyas partículas son menores a 10 ángstrom. Estas soluciones esta conformadas por soluto y por solvente. El soluto es el que esta en menor proporción y por el contrario el solvente esta en mayor proporción. Tosas las soluciones son ejemplos de mezclas homogéneas.
Solución diluida es cuando la cantidad de soluto es muy pequeña.
Solución concentrada es cuando la cantidad de soluto es muy grande.
Solución saturada es cuando se aumento mas soluto en un solvente a mayor temperatura de la normal (esto es porque cuando ya no se puede diluir, se calienta el solvente y se separan sus partículas para aceptar mas soluto)
Solución sobresaturada es cuando tiene más soluto que disolvente
Soluto y Disolvente
La sustancias que está presente en la mayor cantidad se denomina disolvente, que se define como las sustancia en la cual se disuelve otra. Ésta última, que es la que disuelve en la primera, se denomina soluto.
Soluto + Disolvente = Solución
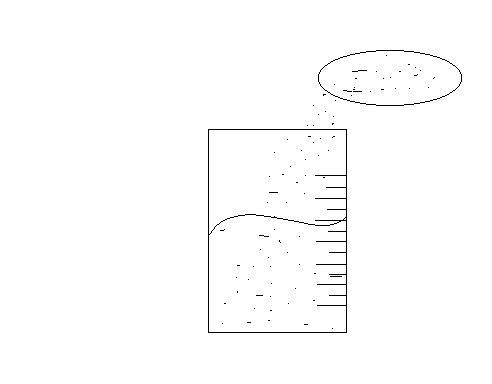
Dilución de soluciones y solución stock
Para diluir una solución es preciso agregar más % de disolvente a dicha solución y éste procedimiento nos da por resultado la dilución de la solución, y por lo tanto el volumen y concentración cambian, aunque el soluto no.
Una solución stock es la cual a partir de ella se puede hacer una disolución:
Solución Stock Nueva Solución
Solubilidad
La solubilidad de un soluto en un disolvente es la concentración que presenta una disolución saturada, o sea, que está en equilibrio con el soluto sin disolver porque siempre habrá algunas moléculas o iones que pasen a la disolución. las sustancias se clasifican en:
Solubles: si su solubilidad es 0,1 M o >.
Poco Solubles: si su solubilidad se sitúa entre 0,1 M y 0,001 M
Insolubles: si su solubilidad no llega a 0,001 M
Factores que afectan a la solubilidad
1.) La temperatura: la mayoría de las disoluciones de sustancias sólidas son procesos endotérmicos y con un aumento de entalpía. Al disolver una sustancia sólida se produce la ruptura de enlaces (energía reticular)que casi nunca se compensa por la energía de solvatación. Por otra parte la destrucción de la estructura ordenada del sólido y la nueva disposición de las moléculas de disolvente alrededor del soluto conllevan un aumento de entropía. Como, unos valores negativos de H y de S positivos favorecen la espontaneidad del sistema por tanto la solubilidad de la mayoría de sustancias aumenta con la temperatura.
En cambio en la disolución de líquidos o gases en líquidos no supone la destrucción de estructuras demasiado estables ni un aumento del desorden ni en muchos casos ruptura de enlaces. La mayoría de los gases son más solubles a bajas temperaturas.
2.)Momento Dipolar: Mayor solubilidad cuanto más parecido sea el momento dipolar del soluto y del disolvente.
3.)Constante Dieléctrica del Disolvente: de acuerdo con la ley de Couland las fuerzas de atracción entre dos iones son más débiles cuanto mayor sea la constante dieléctrica.
4.) Tamaño del Ion y densidad de Carga: si el tamaño de los iones positivo y negativo es muy diferente los iones mayores estarán más próximos. La repulsión desestabilizará la red cristalina y se facilitara la disolución. La densidad de carga representa la carga del ión dividido por su volumen. Cuanto mayor sea la densidad de carga más intensas serán las atracciones eléctricas y más difícil la disolución.
Producto de la Solubilidad
Incluso en las sustancias más insolubles hay siempre una pequeña proporción de partículas que pasan a la disolución. Esto se puede indicar en un campo iónico como un equilibrio entre la forma sólida y los iones en disolución. Este equilibrio está desplazado claramente hacia la forma iónica no disociada.
A la constante de equilibrio se la denota constante del producto de solubilidad o también producto de solubilidad
Cuanto menor sea el producto de solubilidad menor solubilidad tendrá la sustancia.
Efecto Salino
Si no existe efecto de ion común la adicción de otras sales a la disolución aumenta ligeramente la solubilidad.
La presencia en la disolución de iones extraños que no reaccionan ni con el precipitado produce un aumento de la solubilidad
Ej: la solubilidad del Cloruro de talio aumenta en presencia de nitrato potásico o sulfato potásico
Cambio de Disolvente
La solubilidad de una sustancia determinada depende del disolvente utilizado.
Ej: Si a una disolución acuosa de sulfuro de calcio de le añade etanol el sulfuro precipita.
Precipitación fraccionada
A veces se encuentra en una disolución diferentes iones que precipitan con la adicción de un mismo reactivo. Si los productos de solubilidad de los respectivos compuestos insolubles son suficientemente diferentes se puede conseguir precipitar iones de una clase y dejar los otros en disolución. Este principio se denomina precipitación fraccionada.
Influencia sobre el equilibrio de precipitación. Redisolución de precipitados
Efecto del ión común
Si en la disolución de un compuesto iónico poco soluble o insoluble se añade un segundo compuesto que tenga en común alguno de los iones del primer compuesto disminuye la solubilidad de este.
Molaridad
La molalidad se define como el numero de moles de soluto disueltos en 1 kg de disolvente, esto es:
M = [ ( numero de moles de soluto ) / ( peso del disolvente en kg ) ]
La unidad de porcentaje peso tiene la ventaja de que no se necesita conocer la masa molar del soluto. Además, el porcentaje peso de una solución es independiente a la temperatura, ya que se define en términos de pesos, el termino de fracción molar no se emplea normalmente para expresar la concentración de soluciones. Sin embargo es de utilidad para calcular las presiones parciales de los gases y en el estudio de concentración que se emplean con frecuencia, la ventaja del empleo de la molaridad es de que por lo general resulta mas sencillo medir el volumen de una solución utilizando matraces volumétricos calibrados con precisión, que pesar al disolvente. Su principal inconveniente es que depende de la temperatura, ya que el volumen de una solución suele aumentar con el incremento de la temperatura. Otro inconveniente es que la molaridad no especifica la cantidad de disolvente presente. Por otra parte, la molalidad es independiente de la temperatura, ya que se define como una relación del numero de moles de soluto y el peso del disolvente. Por esta razón, la molalidad es la unidad de concentración de empleo preferente en los estudios que involucran cambios de temperatura, al igual que en aquellos de las propiedades negativas de las soluciones.
El termino equivalente-gramo no se puede definir de manera a que sea aplicable a cualquier reacción, es decir, depende de la reacción en la que interviene la sustancia. Esto se debe a que en un mismo compuesto puede tener distintos pesos equivalentes en diferentes reacciones químicas. Por esto, una misma solución puede tener distintas normalidad según sea la reacción en que se emplee. El equivalente gramo de:
| Un ácido | Es el peso del mismo que contiene un átomo de hidrogeno reemplazare, es decir, 1.008 g |
| Una base | Es el peso de la misma que contiene 17.008 de grupo hidróxido ionizable |
| Una sal | Es el mol de la sal dividido por la valencia total del ion reaccionante, en una reacción de precipitación |
| Reacciones en precipitación | Es el peso de la sustancia que contiene o reacciona con un átomo gramo de un cation monovalente (equivalente a 1.008 g de hidrogeno o con medio átomo gramo de un cation bivalente) |
| Reacciones en oxido reducción | Para un oxidante es le peso que contiene o reacciona con 1.008 g de hidrogeno y es el equivalente a la molécula gramo de dicha sustancia, dividida por el cambio total que experimenta el numero de oxidación del elemento que se reduce. |
Al determinar la concentración de una solución, se usa habitualmente el método de titulacion, que consiste en agregar una solución de concentración conocida (solución valorada), hasta que la reacción sea cuantitativa, con un volumen de solución de la sustancia en análisis.
El punto final de la titulacion coincide con el punto de equivalencia, se reconoce visualmente, como regla general, por algún cambio característico, dado por un reactivo auxiliar llamado indicador. El indicador es una sustancia que tiene un color intenso en solución ácida o básica y otro color en soluciones de otro tipo. Los indicadores se emplean para determinar el punto de titulación.
En el punto de equivalencia, el numero de equivalentes gramo de la sustancia que se titula, es igual al numero de equivalentes gramo de la solución valorada que se emplea. Si los volúmenes de las soluciones de dos sustancias a y b que corresponden al punto de equivalencia, son va y vb respectivamente, entonces, dichos volúmenes contienen el mismo numero de equivalentes gramo.
A diferencia de los gases que son completamente solubles unos en otros en todos los casos, las parejas de líquidos muestran todas las variaciones de solubilidad o miscibilidad, desde ser completamente miscibles, como los gases, hasta ser casi completamente inmiscibles. Para objeto de estudio se han clasificado las parejas de líquidos en tres clases:
1) líquidos completamente inmisibles
2) líquidos parcialmente inmisicbles
3) líquidos completamente miscibles.
Los sistemas completamente inmiscibles, se ponen en contacto dos líquidos inmisibles, de forma que ninguno de ellos cubra al otro por completo, cada uno de ellos continuara ejerciendo su presión individual. Es mas, la presión de vapor de cada liquido varia en función de la temperatura como si estuviese presente por si solo. Por consiguiente, a una cierta temperatura, la presión total sobre los dos líquidos será igual a la suma de las dos presiones de vapor individuales.
Los sistemas parcialmente miscibles. Los ejemplos mejor conocidos de líquidos parcialmente miscibles son el fenol, el cresol o sustancias similares en agua.
Normalidad
Se define como el numero de equivalentes químicos de sustancia disuelta por litro de solución.
# de equivalentes = peso molecular del soluto
# de partículas intercambiadas
Concentraciones porcentuales
% peso: se define como el peso del componente entre el peso de la solución por 100
% mol: es el numero de moles de cada uno de los componentes entre el numero total de moles de solución por 100
METODOLOGÍA
Material por equipo
1 frasco de 50ml
1 probeta de 50ml
1 espátula
1 agitador de vidrio
1 vidrio de reloj
1 vaso de precipitados de 50ml
1 matráz aforado de 100ml
Material por grupo
Reactivos por equipo
1. cloruro de sodio
hidróxido de sodio
Procedimiento
Realiza previamente los cálculos necesarios para determinar los gramos necesarios de NaCl para preparar 40ml de una solución al 3%
Pasa en un vidrio de reloj los gramos de NaCl que obtuviste en el punto anterior
Vierte el NaCl en un vaso de precipitados y vierte los 40ml de agua para completar la solución. Mezcla perfectamente de manera que la solución quede homogénea
Guarda la solución obtenida en el punto anterior en un frasco perfectamente etiquetado y sellado
Realiza previamente los cálculos para determinar los gramos necesarios que debes pesar de NaOH para preparar 100ml de una solución 0.1 Molar.
Pesa en un vidrio de NaOH requeridos para la solución
Vierte el NaOH en un vaso de precipitados. Agrega un poco de agua (20ml aprox.) y agita hasta disolver
Pasa la solución anterior a un matraz aforado y adiciona agua hasta completar el volumen de 100ml. Etiqueta tu solución.
PRECAUCIÓN: El NaOH es cáustico, usar espátula y no tocarlo con las manos. Lavarse las manos después de haber utilizado éste reactivo.
RESULTADOS Y ESQUEMAS
1. Después de revolver un largo rato con él agitador, logramos que se formara una mezcla homogénea, con NaCl como soluto y agua como disolvente, mezcla que, a simple vista, se veía como si no estuviera muy concentrada, y aunque fuera así, puede ser peligrosa.

Primero el vidrio de reloj peso sin el NaCl 30.5g y al agregarle 1.2g nos dio como resultado: 31.7. El NaCl se cogió con una cuchara larga.
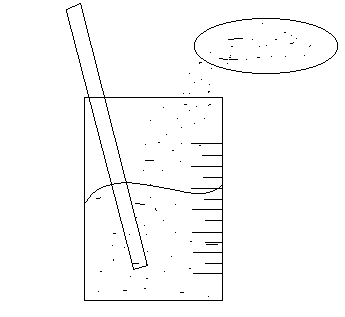
Luego de agregar el NaCl pesado al vaso de precipitados con 40ml, se revolvió con el agitador hasta formar la mezcla homogénea
2. Después de revolver un largo rato con él agitador, logramos que se formara una mezcla homogénea, con NaOH como soluto y agua como disolvente.

Primero el vidrio de reloj peso sin el NaOH 30.5g y al agregarle 0.4 g nos dio como resultado: 30.9. El NaOH se cogió con espátula.
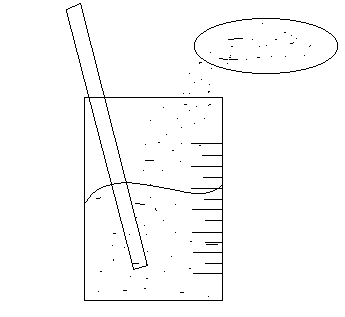
Luego de agregar el NaOH pesado al vaso de precipitados con 20ml, se revolvió con el agitador hasta formar la mezcla homogénea
pasamos la solución que teníamos en el vaso de precipitados a una probeta graduada hasta completar los 100ml.
Martaz Aforado:
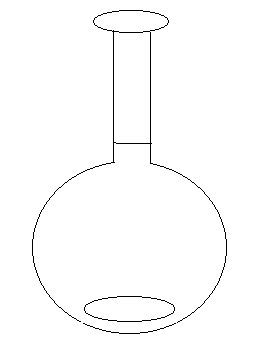
El líquido que contenga la martaz aforada tiene que estar el nivel a la panza, si este es claro, de ser oscuro tiene que estar a los extremos, para ser más preciso podría usarse una pipeta.
![]()
ANÁLISIS DE RESULTADOS
Calcula la normalidad de la solución NaOH que preparaste
Determina la cantidad de NaOH que se requiere para preparar 500ml de una solución 0.2M
¿Cuáles son los cuidados que debes tener en la preparación de soluciones?
-
saber con que estamos trabajando
-
cuando vayas a abrir un frasco hacer lo con cuidado
-
si éste tiene otro tapón por dentro no sacarlo directamente, sino mediante unas tijeras y al final ayudándote con una franela húmeda
-
colocar las tapas de los recipientes boca arriba
-
no invertir tapas ni cucharas porque puedes contaminar las sustancias
-
tratar de no tener contacto con la sustancia
-
tener siempre visible la etiqueta para ver de que sustancia se trata y de que concentración consta.
-
Cerrar muy bien los frascos de dichas soluciones
-
Tener siempre una franela
-
Lavar muy bien el material para evitar contaminar sustancias
CONCLUSIONES
Al terminar la practica denominada SOLUCIONES podemos concluir que con el desarrollo experimental de la presente practica nos pudimos percatar de que la concentración de una solución depende directamente de los factores de molaridad y normalidad, las cuales son propiedades que determinan las características de una solución, con lo cual se puede saber que tan básicas o ácidas pueden ser estas soluciones.
Con lo anterior se puede llegar a la conclusión de que es muy importante tener presente el conocimiento de las expresiones que nos ayudan a conocer lagunas de las características básicas de una solución, con las cuales se pueden calcular soluciones de diferentes grados de concentración.
Además el estudio de las soluciones posee una gran importancia, ya que se puede decir que es la base de la industria química, por un sin numero de procesos y productos provienen de los compuestos entre solutos y disolventes, como en el caso de la industria de los alimentos, perfumes, farmacéuticos, pinturas, etc. Un gran economía o perdida en la industria, la representa el correcto estudio y manejo de los reactivos de una solución, dado que al optimizar estos, depende el ahorro o el desperdicio de los mismos.
BIBLIOGRAFÍA
Bloomfield Molly M. QUÍMICA DE LOS ORGANISMOS VIVOS México DF
ED. Limusa 1997, pp. 87 - 97
Choppin Gregory R. QUÍMICA, México
Ed. Publicaciones Cultural, 1985, pp. 156, 247-349, 19-20
Hill - Kolb, QUÍMICA PARA EL NUEVO MILENIO, México
Ed. Prentice Hall, 1998, pp. 132-133,
PERRY. Biblioteca del ingeniero Químico
McGraw - Hill
BABOR. Química General moderna
Ensa
CROCKFORD. Fundamentos de Fisicoquimica
EDIT. Continental México
Disolvente
Solvente
agitador
1.2g de NaCl
40ml de agua
NaCl 3%
Lo etiqutamos
Lo cerramos
0.4g de NaOH
agitador
20ml de agua
100ml
NaOH 0.1 molar molar
Lo etiqutamos
Lo cerramos
Aforo
Descargar
| Enviado por: | Weepshid |
| Idioma: | castellano |
| País: | México |
