Biología, Botánica y Zoología
Biología
2ªEvaluación
T.6 Sistema endocrino:
Sistema endocrino - Glándulas endocrinas - Hormonas(sust. químicas) - Son vertidas a la sangre - Son acogidas por la célula diana - Cambian el metabolismo.
*Cuando hay más hormonas en la sangre se segrega menos hormonas en la glándula endocrina, y cuando hay menos hormonas la glándula segrega más.
Glándulas Endocrinas:
_Hipófisis:
_Tiroides: - Tiroxina - Las células consumen más oxígeno.
_Cápsulas suprarrenales:
_ Corteza: Adrenalina: Favorece la actividad muscular.
_ Médula: _Aldosterona: impide la eliminación de iones.
_ Cortisona: antiflamatoria y antidolor.
_Gónadas:
_Hombres: testosterona: produce los caracteres 2º en los hombres.
_Mujeres: estrógenos: produce los caracteres 2º en las mujeres.
_Páncreas:
_ Insulina: disminuye el nivel de glucosa en la sangre.
_ Glucagón: lo contrario de la insulina.
Hipófisis:
Adenohipófisis Neurohipófisis Oxitocina Antidiurético
SMH TSH ACTH Estimulantes
de las gónadas
Smh: hormona del crecimiento/Tsh: estimulante del tiroides/Acth: estimulante de la corteza suprarrenal.
| Smh | Tsh | Acth | E. de las gónadas | Antidi- urética | Oxito- cina | |
| Célula diana | A todas | Al Tiroides | A la corteza suprarr.. | A las gónadas | A los riñones | Al útero |
| Provoca | Mitosis | Hombre- Mujer | Retención de orina | Contrac- ciones | ||
T.7 Reproducción sexual.
¿Qué es la reproducción? : Es formar seres semejantes a los que lo origina.
_Asexual - Un individuo - Todos los descendientes iguales.
Reproducción
_ Sexual - Dos individuos - Todos los descendientes diferentes.
| Aparato reproductor Femenino | Aparato reproductor Masculino |
| Óvulos | Gametos: Células con la mitad de información. | Espermatozoide |
| Fecundación |
| Cigoto |
| Embrión |
| Feto |
| Recién nacido |
*Tras la fecundación se crea la célula huevo o cigoto que contiene 46cromosomas (23 y 23) siempre, ya que en el caso de que no fuera así habría malformaciones en el ser.
Cambios en la pubertad:
Hombres: musculatura más desarrollada, cambio de la voz, desarrollo y maduración de los órganos sexuales.
Mujeres: desarrollo de las glándulas mamarias, acumulación de grasa en algunas zonas, y desarrollo y maduración de los órganos sexuales.
La pubertad es la época de nuestra vida en que se producen todos los cambios.
Órganos Sexuales:
Aparato reproductor femenino:
· Los Ovarios: del tamaño de una almendra. Dentro de ellos madura un óvulo y se libera cada mes. También producen las HSF.
· Trompas de Falopio: dos conductos que unen los ovarios con el útero. Es donde se produce la fecundación.
· Útero: cavidad preparada para acoger el óvulo fecundado y desarrollar el embrión.
· Vagina: conducto flexible que comunica el útero con el exterior. Se abre por el orificio vaginal detrás del meato de la orina, ambos rodeados por los labios menores y otros externos: labios mayores. En la parte superior de éstos se encuentra el clítoris, una pequeña protuberancia especialmente sensible.
Aparato reproductor masculino:
· Testículos: fabrican los espermatozoides y HSM. Se encuentran en el escroto(el saco).
· Epimídos: estructuras sobre los testículos. Completan la maduración espermatozoides.
· Conductos deferentes: por donde los espermas van hasta las vesículas seminales.
· Vesículas seminales: almacenan espermas y unen líquido sirviente de vehículo y alm.
· Próstata: órgano que fabrica el líquido prostático que junto el seminal forma el semen.
· La uretra: conducto que atraviesa el pene y finaliza en el meato urinario.
· El pene: órgano con la misión de depositar los espermas en la vagina. La parte final se llama glande, recubierta por una porción de piel llamada prepucio.
Células sexuales.
El óvulo: es el gameto femenino. Es una célula muy grande y con dificultad de movi-
miento. Su capacidad reproductora es de 24 horas, una vez liberado del ovario. Llega a la Trompa de Falopio, donde puede permanecer un corto periodo de tiempo en el que podrá ser fecundado o morir. A éste lo rodean células acompañantes y la zona pellúcida.
Los espermatozoides: son los gametos masculinos. Más pequeños y móviles quel óvulo y están formados por una cabeza, una parte intermedia y la cola.
Las hormonas sexuales: las producen los testículos y los ovarios. Causan los cambios fisiológicos responsables de la aparición de los caracteres sexuales que diferencian a los dos sexos, además de regular la sexualidad y la reproducción. Pueden ser los estrógenos que son las HSF y los andrógenos; HSM.
El ciclo menstrual.
Tras la pubertad el hombre y la mujer son capaces de reproducirse. En las mujeres se produce una actividad cíclica de los ovarios con la maduración de un óvulo cada 28 días aprox. A partir de los 50 años aprox. se hacen más irregulares y acaban por desaparecer. A este último periodo se le llama menopausia o climaterio.
Durante la maduración del óvulo el útero se prepara para un posible embarazo cubriéndose en su interior de una gran cantidad de vasos sanguíneos. A esta capa se denomina endometrio. Una vez transcurrido ese tiempo (24 h.), el óvulo muere. Entonces se inicia otro ciclo.
| Día 1-5: menstruación. Día 6-13: endometrio. Día 14-15: madura el óvulo y se le expulsa a las trompas. Día 16-28: Reposo o expulsión. |
La fecundación.
Es la unión de un óvulo y un espermatozoide para formar el cigoto. Se produce en la Trompa de Falopio. Estos, que se introducen en la vagina en el coito, si no encuentran ningún óvulo, mueren al cabo de tres días. Si no, lo rodearán, pero sólo uno podrá penetrar en él. Más tarde se produce la unión de los núc de los gametos.
El embarazo.
Tras la fecundación, el cigoto empieza a dividirse continuamente. A esta estructura se denomina embrión, que termina instalándose en las paredes del útero con la formación de la placenta. A este hecho se denomina nidación, ocurre unos 7 días después de la fecundación. El embrión está rodeado de una membrana denominada corión. Endometrio y corión quedan entrelazados y unidos entre sí formando la placenta, donde se une el embrión y la madre, por medio del cordón umbilical. Así el bebé recibe… de la madre y expulsa a ésta…A partir del 3º mes recibe el nombre de feto.
El parto.
Finalizado el embarazo, tiene lugar el parto, que consta de 3 periodos:
· Dilatación del cuello uterino. Comienza con las contracciones de las paredes del útero y la dilatación del cuello. Las contracciones producen la ruptura de la bolsa amniótica (donde se desarrolla el feto) y la salida del líquido amniótico.
· Expulsión del feto: las contracciones y la presión de los músculos abdominales empujan al feto a través de la vagina hasta el exterior.
· Expulsión de la placenta: una vez nacido, se le corta el cordón umbilical; la cicatriz constituye el ombligo. Luego, la placenta se desprende de las paredes del útero y es expulsada junto con restos de envolturas.
Salud y enfermedad.
La salud.
Podemos definir salud como la ausencia de enfermedad. Pero la salud no es sólo un concepto físico, también es psíquico. Para mantenernos en buena salud es imprescindible observar una serie de hábitos saludables
Hábitos saludables.
Son todos aquellos hábitos que nos ayudan a mantenernos en buena salud y prevenir las enfermedades. Uno de los más importantes es mantener una dieta saludable. Además, que es importante observar una serie de conductas sanas: masticar correctamente, higiene bucal, evitar sust nocivas, etc.
Las enfermedades.
Son un proceso anormal que altera, modifica o impide la actividad de una parte de nuestro cuerpo o del organismo completo.
Las lesiones traumáticas no son enfermedades. Los grupos más importantes son:
· Las enfermedades infecciosas debidas a la acción de microorganismos.
· Las enfermedades congénitas son las existentes al nacer.
· Las enfermedades hereditarias se transmiten de padres a hijos.
· Las enfermedades carenciales se deben al déficit o a la ausencia en la dieta de sustancias importantes.
· Las enfermedades crónicas son las que no tienen curación posible.
Epidemias y pandemias.
En ocasiones, una enfermedad infecciosa, puede extenderse de tal modo que afecte a una población más grande. Entonces hablamos de epidemias o pandemias.
· Una epidemia afecta a una comunidad.
· Una pandemia afecta a un territorio muy grande.
Actualmente es muy difícil que una enfermedad se extienda de tal forma. No obstante, con enfermedades que no son demasiado graves pero se transmiten con mucha facilidad.
Luchando contra las enfermedades.
La medicina dispone de diversos recursos para luchar contra las enfermedades. El tratamiento con fármacos, que permite la curación o, al menos, el alivio. En algunos casos se realizan intervenciones quirúrgicas. La medicina preventiva, vacunación, previene las enfermedades y evita que se produzcan.
Las enfermedades producidas por microbios.
Las enfermedades infecciosas son las producidas por diversos microorganismos. Los que producen enfermedades se llaman patógenos, y pueden ser virus, bacterias, hongos y protozoos. Éstos pueden penetrar en nuestro cuerpo por vía digestiva, respiratoria o cutánea (por una herida), y sexual. Causan diferentes efectos. El más habitual es la fiebre, que en realidad en una defensa de nuestro cuerpo contra la infección.
Prevenir las enfermedades infecciosas.
Es difícil prevenirlas. La única forma de prevención es la vacunación. Consiste en introducir en el organismo un preparado, la vacuna, que contiene los microorganismos que provocan una enfermedad o bien las toxinas que estos microorganismos producen.
Enfermedades producidas por virus.
Algunas de ellas son:
· El catarro común es una enfermedad muy contagiosa. Produce malestar leve, congestión y estornudos. Los virus pasan por contacto; una forma de prevenirlo es lavarse las manos cuando se está con personas enfermas.
· La gripe. Se transmite como el catarro, pero es otro virus. Produce malestar más intenso y dolores en las articulaciones. Es más grave en niños y ancianos.
· El SIDA es producido por un virus que ataca al sistema de defensa del organismo y que se transmite por contacto sanguíneo. Aunque aún no existe vacuna, los enfermos pueden llevar una vida casi normal.
Enfermedades producidas por bacterias.
Las bacterias son más resistentes que los virus y se pueden transmitir de varias maneras.
· La salmonelosis se produce por comer alimentos contaminados por la bacteria Salmonella. Provoca fiebre alta y trastornos digestivos graves.
· El tétanos se produce por la infección por la bacteria Chlostridium tetani. Afecta al sistema nervioso y provoca rigidez muscular.
Existen vacunas para muchas enfermedades producidas por bacterias. Casi todas se pueden tratar con antibióticos.
Enfermedades producidas por hongos.
Los hongos patógenos son muy contagiosos, pero suelen aparecer sólo en personas con higiene deficiente. Las infecciones son muy molestas y de difícil curación. Ej.: la candidiasis y el pie de atleta.
Enfermedades producidas por protozoos.
Son más propias de zonas tropicales. La malaria y la enfermedad del sueño son buen ejemplo. La malaria se produce por la picadura de un mosquito frecuente en zonas pantanosas tropicales. La enfermedad del sueño, que aparece en África, se transmite de forma similar, picadura de la mosca tse-tse.
Trastornos de los aparatos de la función de nutrición.
Los aparatos que desempeñan la función de nutrición, pueden verse afectados por gran nº de enfermedades relacionadas con la dieta o a factores distintos.
Algunas enfermedades del aparato digestivo.
Una de las enfermedades bucales más comunes es la caries, que consiste en una destrucción progresiva de las piezas dentarias. La única forma de prevenirlas es tener buen higiene y revisiones odontológicas.
Entre las más conocidas se encuentran las úlceras. Es una pequeña herida que aparece en la pared del estómago o duodeno. Antes la única solución era la cirugía, pero ahora hay medicamentos que producen mejoría o desaparición.
Menos grave es la gastritis: inflamación de las paredes del estómago, que causa ardores y digestiones pesadas. Se trata con fármacos.
La gastroenteritis se produce por una infección por virus o bacterias o bien por intoxicación alimentaria. Causa malestar, fiebre, vómitos. Se cura con reposo y dieta blanda.
Algunas enfermedades del aparato respiratorio.
Aparte del catarro, podemos citar dos enfermedades imprtantes: la bronquitis y el asma.
La bronquitis es una inflamación de los bronquios debido a la infección de una bacteria. Produce tos y expectoración. Se cura con antibióticos.
El asma se produce por la contracción súbita de los músculos de los bronquiolos, que dificulta la respiración. Es debida, generalmente, a la alergia. Se alivia con aerosoles.
Enfermedades del aparato circulatorio.
Muchas se deben a la obstrucción de los vasos sanguíneos. La aterosclerosis, ocasionada por acumulación de grasa que reduce el flujo de sangre.
La trombosis se debe a la formación de un coágulo de sangre en un vaso sanguíneo. Impide la llegada de sangre a la zona donde se produce.
El infarto y la angina de pecho se deben a la obstrucción de las arterias coronarias.
· La angina de pecho se produce por el estrechamiento o la obstrucción parcial de las coronarias. Causa un dolor intenso en el pecho. No suele tener consecuencias graves.
· El infarto de miocardio, se produce por la muerte de una parte del corazón debido a la obstrucción total de las arterias. Causa un dolor intenso en el pecho. Si la zona afectada es muy grande, el infarto es mortal.
Enfermedades del aparato excretor.
Entre las más comunes está la cistitis, inflamación de la vejiga de la orina. Es molesta y dolorosa.
La inflamación de los riñones, se manifiesta por la presencia de sangre en la orina y dolor en la zona lumbar. El cólico nefrítico también es muy doloroso, y se debe a la acumulación de piedras en un riñón.
El impacto de las enfermedades de los sistemas de coordinación.
Las alteraciones en los órganos de los sentidos, el sistema nervioso o el sistema endocrino, causan importantes trastornos. Siempre tienen un importante impacto en nuestra vida.
Muchas de estas enfermedades son bien conocidas y existen medicamentos para combatirlas. Otras plantean importantes problemas y son un reto para la investigación médica.
Las enfermedades degenerativas del sistema nervioso.
Una enfermedad es degenerativa, si produce el deterioro progresivo de un órgano hasta impedir su función. Las más importantes son el síndrome de Alzheimer y la enfermedad de Parkinson.
Ambas se originan por procesos químicos que destruyen las neuronas de determinadas zonas del cerebro, o impiden su comunicación. El Alzheimer produce una pérdida progresiva de la memoria y la capacidad de razonar. El Parkinson afecta al movimiento, y produce temblores y rigidez. En la actualidad, están tratando de hallar tratamientos eficaces contra ambas enfermedades.
Enfermedades de los órganos de los sentidos.
Son muy variadas, algunas ocasionan molestias, otras importantes alteraciones.
Enfermedades del gusto y del olfato.
La única conocida es el catarro común. Durante el curso perdemos capacidad olfativa, y por tanto, gustativa.
Enfermedades del oído.
Una muy común, es la otitis. Se trata de una inflamación del oído, que causa dolores molestos. Más graves son las que conducen a la sordera. Muchas son degenerativas. En muchos casos, el uso de audífonos resuelve el problema.
Enfermedades de la vista.
Una de las más comunes es una de las más leves. Se tratta de la conjuntivitis, inflamación de la membrana conjuntiva, causa enrojecimiento de los ojos, picores, lagrimeo y legañas. Muchas se deben a infecciones por microorganismos.
Entre las que pueden producir la ceguera, destaca el glaucoma y el desprendimiento de retina. Son alteraciones graves, pero si se detectan en fase temprana, de fácil curación. Las cataratas, consisten en una transformación del cristalino del ojo, que se vuelve translúcido. Sólo dificulta la visión.
Enfermedades del sistema endocrino.
Pequeñas modificaciones en la dosis de una hormona producen grandes trastornosen el funcionamiento de los órganos diana.
La diabetes es una enfermedad muy común que se debe a un problema de funcionamiento del páncreas. El resultado es que las células consumen menos glucosa y, aumenta la cantidad de esta en la sangre. Esto produce alteraciones en el organismo.
Cuando la diabetes es severa, es necesario compensar la deficiencia de insulina mediante la administración periódica de esta hormona.
Las alteraciones en el crecimiento es un problema en la producción de la hormona de crecimiento, que puede provocar el enanismo o el gigantismo. Esta hormona es necesaria en cantidades determinadas. En cantidades menores provoca un crecimiento deficiente, en caso contrario provoca un crecimiento exagerado.
La hormona se puede obtener mediante técnicas de biotecnología. También se puede someter a soluciones quirúrgicas en el caso del gigantismo.
3ª Evaluación
T.1. El lenguaje de la materia.
Formulación y nomenclatura de los compuestos inorgánicos.
-
Formular un compuesto consiste en escribir correctamente su nombre.
-
Nombrar un compuesto consiste en asignarle su nombre correcto atendiendo a las características de su fórmula.
-
La suma de los nº de oxidación de todos los átomos de los elementos que intervienen en un compuesto debe ser cero.
Halogenuros son compuestos binarios formados por dos elementos; un halógeno (elementos 7b) y un metal o Hidrógeno. Los halógenos actúan siempre con valencia 1.
-
Valencia es el nº de electrones que puede ganar o perder un elemento y coincide con el nº de oxidación.
-
Formulación: se escribe primero el metal seguido del no metal (halógeno) y se intercambian las valencias como subíndices.
-
Nomenclatura: puede ser clásica, de Stock o sistemática:
· Clásica: se nombra el no metal terminado en -uro y el metal terminado en -ico, si el metal tiene dos valencias se termina en -ico con la máxima y en -oso con la pequeña.
· N. de Stock: se nombra el halogenuro terminado en -uro seguido del nombre del metal y el numero de valencia en nº romanos.
· Sistemática: primero se añade un prefijo numeral dependiendo del nº del subíndice seguido del halógeno terminado en -uro y luego el nombre del metal.
Calcogenuros, Formulación: se coloca primero el metal seguido del calcógeno (elementos 6b) y se intercambian las valencias, si se puede se simplifica dividiendo los dos subíndices por el menor. Los calcógenos actúan siempre con valencia 2.
-
Nomenclatura: siguen las mismas normas que los halogenuros. Sabiendo que al azufre se le llama sulfuro y excepcionalmente a los que llevan oxígeno se les llama óxidos. Los óxidos también pueden ser no metales.
Hidróxidos son un metal más el ion OH.
-
Formulación: se pone el no metal seguido del OH y se intercambian las valencias sabiendo que el OH actúa de valencia 1.
-
Nomenclatura: se nombra de la misma forma que los anteriores anteponiendo siempre la palabra hidróxido que proviene del ion OH.
| Elementos. | Números de oxidación. |
| H, Li, Na, K, Rb, Cs | +1 |
| Be, Mg, Ca, Sr, Ba | Zn, Cd | +2 |
| B (Boro), Al (Aluminio) | +3 |
| Fe (Hierro), Co (Cobalto), Ni (Níquel) Cu (Cobre), Hg (Mercurio) Cr (Cromo) Mn (Manganesio) | +2 ó +3 +1 ó +2 +3 ó +6 +2, +4 ó +7 |
| C (Carbono), Si (Silicio) Sn (Estaño), Pb (Plomo) | +4 ó - 4 +2 ó +4 |
| N P (fósforo), As (Arsénico), Sb (Antimonio) | +1, +2, +3, +4, +5 ó - 3 +3, +5 ó - 3 |
| O S (Azufre), Se (Selenio), Te (Teluro) | -2 +4, +6 ó -2 |
| F Cl (Cloro), Br (Bromo), I (Yodo) | -1 +1, +3, +5, +7 ó -1 |
-
Anhídridos. Son óxidos de no metales. Se nombran igual que un óxido pero sustituyendo óxido por anhídrido. Los no metales se nombran de forma distinta según sus valencias, que las podemos apreciar en la tabla dabajo.
| Colm 4b | Colm 5b | Colm 6b | Colm 7b | Respectivas nomenclaturas |
| 1 | 2 | 1 | Hipo - oso | |
| 2 | 3 | 4 | 3 | - oso |
| 4 | 5 | 6 | 5 | - ico |
| 7 | Per - ico |
-
Oxoácidos. Se forman con la suma de un anhídrido y el agua.
-
Sales. Se forman con un oxoácido cambiando el H por un metal y cambiando las terminaciones: -oso -ito; -ico -ato.
T.2. Las reacciones químicas.
-
Una reacción química es un proceso en el que unas sustancias iniciales se transforman en otra u otras sustancias finales, distintas de las de partida.
-
Los componentes de dichas reacciones son:
· Los reactivos son las sustancias que inicia la reacción química.
· Los productivos sustancias finales que se obtienen en una reacción.
-
Una reacción química aumenta su velocidad si:
· Aumenta la concentración de los reactivos.
· Aumenta el grado de división de los reactivos sólidos.
· Aumentar la temperatura de la reacción.
-
Se modifica la velocidad de una reacción química si se añaden catalizadores en pequeña cantidad.
-
El porcentaje en masa se halla:
-
El porcentaje en volumen se halla:
-
La moralidad se halla:
Esquema T.7. Átomos y moléculas.
El átomo. La teoría atómica de Dalton resultó muy útil para interpretar el comportamiento de las sustancias. Sin embargo años más tarde se produjeron algunos descubrimientos que demostraron que los átomos no eran indivisibles; se descubrió la existencia de las partículas subatómicas, los electrones, protones y neutrones. Cada uno de estos descubrimientos provocó la aparición de un modelo atómico.
* El físico danés Bohr propuso un modelo atómico en el que los electrones giran entorno al núcleo en niveles energéticos bien definidos. Cada uno de estos sólo puede contener un nº determinado de electrones. Para que un electrón cambie de nivel, es necesario modificar su energía en una cantidad determinada.
-
El modelo atómico actual. Los diferentes modelos atómicos desarrollados a lo largo del s XX pusieron de manifiesto la existencia de dos partes bien diferenciadas: El núcleo y la corteza.
· El núcleo es la parte central del átomo y en él se encuentran los protones y neutrones.
- Los protones son partículas con carga eléctrica positiva.
- Los neutrones son partículas sin carga y de masa aproximadamente igual a la de los protones.
· La corteza es la parte exterior del átomo y contiene los electrones, cuya masa es unas 2000 veces menor a la de los protones. Los primeros s encuentran distribuidos en diferentes niveles energéticos y ocupando orbitales.
- Los niveles energéticos se enumeran del 1 al 7 por orden creciente de energía: el 1 es el menos energético y el 7 el que más.
- Los orbitales son regiones del espacio, en torno al núcleo, donde la probabilidad de encontrar electrones es muy grande.
Masa, carga y volumen de un átomo.
· La masa de un átomo se concentra en el núcleo, la masa de los electrones es insignificante.
· En todos los átomos, el nº de protones es igual al nº de electrones de la corteza, por lo que el átomo carece de carga, es eléctricamente neutro.
· El volumen que ocupa el átomo es aproximadamente 10, elevado a la quince, veces mayor que el volumen del núcleo.
-
Nº atómico y nº másico. Para distinguir los átomos de un elemento de otro hemos de considerar los dos parámetros superiores.
· El nº atómico, Z, es el nº de protones que tienen los núcleos de los átomos de un elemento.
· El nº másico, A, es la suma del nº de protones y el nº de neutrones que tiene el núcleo de un átomo.
El nº atómico y el másico, suelen representarse junto con el símbolo del átomo correspondiente de la siguiente manera:
-
Isótopos y masa atómica. Muchos elementos poseen átomos que teniendo el mismo nº Z tienen distinto nº A.
· Llamamos isótopos a las formas atómicas de un mismo elemento que se diferencian en su nº másico.
Masa atómica. La unidad que se emplea para determinar la masa de un átomo se denomina unidad de masa atómica, u, y se define como la doceava parte de la masa de un átomo de carbono (pues lo ponen como referencia) que es 12. Por tanto esto equivale a la masa de un protón o neutrón. Y la masa atómica de un elemento se define como:
· La masa atómica de un elemento es el número de veces que un átomo de este elemento contiene la unidad de masa atómica.
-
Estructura electrónica. Según la energía de los distintos niveles, éstos pueden contener diferentes tipos de orbitales, denominados s, p, d y f.
La configuración electrónica de un átomo es la distribución de sus electrones es los diferentes niveles y orbitales, ordenados de menor a mayor energía.
-
Agrupaciones de átomos. Distinguimos entre elementos y compuestos.
· Los elementos están formados por átomos iguales y no pueden descomponerse en otros más sencillos. Hierro.
· Los compuestos están formados por moléculas iguales que sí pueden descomponerse en otros materiales más sencillos. Agua.
Tanto los elementos como los compuestos son materiales de composición fija, por ello se denominan sustancias puras.
Los científicos pensaron que las unidades mínimas de los elementos eran los átomos y la de los compuestos las moléculas. Pronto se descubrió que no era exactamente así.
En los elementos; el oxígeno forma moléculas diatómicas, constituidas por dos átomos. En cambio el hierro forma una tupida red cristalina de átomos. Los átomos de las sustancias que están formadas por un único elemento se agrupan en redes cristalinas o moléculas.
En los compuestos; el dióxido de carbono forma moléculas en las que hay un átomo de carbono y dos de oxígeno. La arena o sílice forma una red cristalina en la que hay un átomo de silicio por cada dos de oxígeno. Los átomos de los compuestos también se agrupan entre sí formando moléculas aisladas o redes cristalinas.
· Las moléculas de un elemento están formadas por dos o más átomos de un mismo elemento. Las moléculas de compuestos están formadas por dos o más átomos de diferentes elementos.
· Las redes cristalinas están formadas por un número indeterminado de partículas elementales que se disponen constituyendo una estructura geométricamente ordenada.
-
La regla del octeto. ¿Por qué los átomos presentan tendencia a unirse entre sí? Se unen porque adquieren una situación más estable cuando están separados. Depende de su configuración electrónica relacionada con los gases nobles.
· Los gases nobles. No presentan ninguna tendencia a reaccionar ni a formar agrupaciones de átomos. El análisis de su configuración electrónica muestra que, a excepción del He, todos los gases nobles tienen ocho electrones en su nivel más externo.
Se admite que los átomos de los elementos tienden a rodearse de ocho electrones en su nivel más externo para ganar estabilidad. Este comportamiento recibe el nombre de regla del octeto.
· Los átomos de los elementos tienden a ganar, perder o compartir electrones para conseguir que su nivel más externo adquiera la configuración de gas noble.
-
El enlace químico. Es la unión que se establece entre los átomos o las partículas elementales que constituyen una sustancia.
Pero las sustancias presentan agrupaciones muy diversas. Este diferente comportamiento se debe a la existencia de distintos tipos de enlaces: iónico, covalente o metálico.
-
El enlace iónico. El ion es un átomo o un grupo de estos que ha ganado o perdido uno o más electrones y ha adquirido carga eléctrica positiva o negativa respectivamente. Según si la tendencia de los átomos es perder o ganar electrones distinguiremos entre iones positivos o cationes (cuando un elemento pierde uno o más electrones y estos elemento se denominan elementos metálicos) y iones negativos o aniones (cuando un elemento gana uno o más electrones y dicho elemento se denomina elemento no metálico).
· El enlace iónico es la unión que resulta de la presencia de fuerzas de atracción electrostática entre iones de distinto signo.
-
Enlace covalente. Cuando la tendencia a ganar electrones es similar, los átomos se aproximan bastante, los orbitales de los electrones más externos se solapan entre sí y forman un nuevo orbital (orbital molecular) mediante el cual comparten los electrones que aporta cada átomo.
· El enlace covalente es la unión de dos átomos que comparten uno o más pares de electrones. Así el nivel más externo se ha completado con ocho electrones.
-
El enlace metálico. Los átomos de los metales pueden perder algunos de los electrones de su nivel más externo y convertirse en iones positivos que forman redes cristalinas. Los electrones perdidos forman una nube electrónica que envuelve a la red. Estos electrones pueden desplazarse entre sí.
· El enlace metálico es la unión que existe entre los átomos de los metales, que se encuentran formando una red cristalina.
-
Tipos de sustancias. El tipo de enlace condizoa las prop de las sust que lo presentan.
| Sust iónicas (Sal) | Sust covalentes (Agua) | Metales (Hierro) | |
| Estructura | Red cristalina iónica | Moléculas y red cristalina d´atómo | Red cristalina metálica. |
| Estado nat | Sólidas | Sólidas, líquidas y gaseosas. | Sólidas (- Mercurio). |
| Solubilidad | En agua | Insolubles en agua | Solubles entre sí, fusión. |
| Conduct.dad | Conducen corriente | No conducen | Buenos conductores. |
Esquema T.1.
La materia. La materia es un conjunto de átomos que ocupa un lugar en el espacio.
-
Puede ser:
· Inorgánica (aquella que no tiene vida). En esta encontramos tres tipos:
- Metales. Están formados por un elemento. El Hierro (Fe).
- Minerales. Están formados por más de un elemento. Pirita (SFe)
- Rocas. Son un conjunto de minerales.
· Orgánica (aquella que tiene vida). Está formada por:
- Glúcidos. Carbono, Oxígeno y Hidrógeno.
- Lípidos. Carbono, Oxígeno y Hidrógeno y puede que P, fósforo.
- Proteínas. Carbono, Oxígeno y Hidrógeno y también Nitrógeno.
- Ácidos nucleicos. Carbono, Oxígeno y Hidrógeno y puede que P o N.
- Según la posición de sus átomos puede ser:
· Amorfa. Aquella en la que sus átomos están desordenados.
· Cristalina. Aquella en la que sus átomos están ordenados.
-
Cristal. Material que presenta una estructura interna ordenada en la que los átomos se disponen en el espacio formando una red regular en 3 Dimensiones.
-
Materia mineral. Es la materia inorgánica que forma todo aquello que constituye la corteza terrestre.
Minerales.
- ¿Qué es un mineral? Es una materia formada por la unión de átomos con una
composición fija.
· Son sustancias sólidas. No hay minerales líquidos ni gaseosos.
· Son sustancias naturales. Se encuentran en la naturaleza.
· Su composición es homogénea. Es siempre la misma.
· Son uniformes. Presentan la misma composición en todos sus puntos.
· Son sustancias cristalinas. Sus átomos están ordenados.
- Propiedades de los minerales.
· Propiedades químicas. Se deben a su composición (si se disuelve en agua, el sabor…)
· Propiedades físicas.
- Dureza. Resistencia a ser rayado. Escala de Mohs.
- Aspecto. Color, brillo, transparencia y textura.
- Densidad. Cantidad de masa de un mineral en una unidad de volumen. D=M/V.
- Otras:
· Tenacidad. Resistencia a la fractura.
· Maleabilidad. Capacidad para separarse en láminas.
· Ductilidad. Capacidad para separase en filamentos.
· Si conducen electricidad, magnetismo…
- Clasificación.
· Sedimentarios. Formados a partir de sedimentos.
· Metamórficos. Formados por transformación de otros materiales debido al calor o la presión.
· Magmáticos. Formados por el enfriamiento o solidificación del magma.
Ejemplos de minerales.
-
Sedimentarios.
· Calcita: mineral sedimentario carbonatado. Color blanco. Se utiliza para hacer cemento y cal. Formado por carbonato de calcio.
· Halita: mineral sedimentario del grupo de los haluros. Cristaliza en cubos incoloros y blancos. Formado por cloruro sódico.
· Pirita: Mineral sedimentario del grupo de los sulfuros y sulfatos. Tiene cristales cúbicos de intenso color dorado grisáceo. Formado por sulfuro de hierro.
-
Metamórficos.
· Grafito: mineral metamórfico. De intenso color negro. Utilizado para fabricar minas de lápices. Formado por carbono puro.
· Talco: mineral metamórfico. Muy blando (1 en escala de Mohs). Color blanco. Formado por silicato de magnesio.
-
Magmáticos.
· Mica: mineral magmático del grupo de los silicatos. Tiene aspecto laminar. Formado por silicatos de aluminio y potasio.
· Cuarzo: el más conocido de los silicatos. Transparente. Con cristales hexagonales de diversos colores. Formado por dióxido de silicio.
Esquema T.2.
Las rocas.
-
¿Qué es una roca? Se pueden definir como agregados naturales compuestos por una o más especies de minerales. Son sólidas y rígidas a excepción del petróleo.
-
Diferencia entre rocas y minerales. Un mineral tiene una estructura cristalina. Las rocas no tienen nunca esa uniformidad. Puede tener ciertas variaciones en su composición, dentro de unos márgenes.
-
La diversidad de las rocas. Hay tres rasgos importantes que nos permiten describir las rocas y diferenciarlas:
· La textura es el aspecto superficial de la roca. Puede ser granuda, blanqueada, etc.
· La asociación mineral es el conjunto de minerales que forman la roca y nos informa de su composición química.
· La edad es la antigüedad de la roca. Que se puede calcular mediante análisis o por el fósil, en el caso de que sea una roca fosilífera.
-
Clasificación de las rocas. Según su origen se pueden clasificar en ígneas (granito, basalto), sedimentarias (caliza-arenisca) y metamórficas (mármol, cuarcita).
-
Unidades litológicas de España. Los materiales rocosos que componen el territorio español se pueden clasificar en 4 unidades litológicas:
· Terrenos arcillosos. Formados por rocas graníticas y muy antiguas.
· Terrenos calcáreos. Constituidos por rocas como la caliza, de antigüedad media.
· Terrenos arcillosos. Predominan rocas de grano fino y más modernas.
· Terrenos volcánicos. Muy escasos y form por rocas volcánicas.
Rocas ígneas.
-
El magma. Material a partir se forman las rocas ígneas. Son materiales formados por la fusión de las rocas en la base de la corteza terrestre o manto superior. El enfriamiento, por el cual se forman las `ígneas', puede suceder cerca de la superficie o en la profundidad.
-
Formación de las rocas ígneas. Ocurre por enfriamiento y solidificación del magma. Pero pueden tener las carac distintas debido a:
· Las características del magma. Comp química, temperatura y densidad.
· El proceso de cristalización. Cuando es rápido los cristales son pequeños, si es lento, los cristales de los minerales son grandes.
· El emplazamiento del magma. El lugar de la corteza donde se solidifica. Se utiliza para clasificar las rocas en dif grupos.
-
Tipos de rocas ígneas.
· Rocas extrusivas o volcánicas formadas en la superficie terrestre o muy cerca de ella.
· Rocas intrusivas que se forman en el interior y que pueden ser.
- Plutónicas, granito, formadas por el enfriamiento de grandes masa de magma a gran profundidad, tienen cristales grandes.
- Filonianas, pórfidos, se forman a profundidades medias. Enfriamiento más rápido.
Rocas sedimentarias.
-
Sedimentos y rocas sed. Sedimento es un material suelto que proviene de la erosión de otras rocas, de tamaño variado y que se acumulan en ambientes deposicionales. Como el océano.
-
La formación de las rocas sed. Mediante la transformación de los sed en rocas sólidas y compactas. A este proceso se le llama litificación (transformación en piedra). Hay varios cambios importantes en esta transformación:
· La compactación. Se debe al peso de los materiales que se van depositando sobre los sedimentos. El proceso de acumulación de sedimentos es continuo, los materiales que se encuentran más abajo soportan más peso. Así, se pierde el aire y agua que había entre las partículas.
· La cimentación. Consiste en la precipitación de diversos compuestos minerales entre las partículas de un sedimento. Forma un cemento que une las partículas y disminuye la porosidad del sedimento.
La form de este tipo de rocas puede suceder también por otros procesos, evaporación del agua de entre las part o en las cuevas, la precipitación de sust disueltas en agua.
-
Disposición de rocas sed en el campo. Se encuentran formando capas paralelas denominadas estratos. Si no son paralelas se ha producido un elevamiento.
-
Tipos de rocas sed. La clasificación se realiza en función de los procesos por los que se forman.
· Rocas detríticas. Formadas por la litificación de sed. Conglomerados y areniscas.
· Rocas de precipitación. Formadas por la precipitación de sust que arrastraba el agua. Caliza.
· Rocas orgánicas. Formadas por la litificación de sedimentos de seres vivos. Petróleo.
El cambio de las rocas.
-
Origen de las rocas metamórficas. Se forman a partir de otras rocas mediante procesos que implican profundas transformaciones. Las rocas metamórficas provienen de las ígneas, de las sedimentarias o de otras metamórficas. El metamorfismo es un proceso que hace que una roca se convierta en otra distinta. Este proceso sucede en condiciones de presión y temperatura. Las variaciones que produce el metamorfismo en las rocas son, fundamentalmente, cambios en la composición mineral y alteraciones en la textura.
-
El metamorfismo y sus tipos. En el caso de que en una zona de la corteza terrestre halla ascendido el magma entre dos zonas de metamorfismo, se estaría formando granito. La presencia de ese magma produce importantes cambios en el entorno. La alta temperatura del magma produce un importante ascenso de la temperatura en las rocas de alrededor.
Éste es un claro ejemplo de metamorfismo de contacto, que produce rocas metamórficas como el mármol, a partir de la caliza o la cuarcita a partir de la arenisca. El metamorfismo de contacto es un tipo de met local. Se denomina así a cualquier proceso de met que afecte a una zona no muy extensa. Pero un proceso parecido puede afectar a zonas mucho más extensas. Entonces hablaríamos de met regional.
-
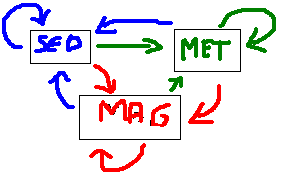
El ciclo de las rocas. Las rocas se forman a partir de otras y este proceso de cambio está sucediendo continuamente. Llamamos ciclo de las rocas al conjunto de procesos y transformaciones que suceden continuamente en la corteza terrestre y hacen que unas rocas se transformen en otras.
· Las flechas azules representan los procesos de destrucción, son los procesos que conducen a la formación de las rocas sedimentarias.
· Las flechas verdes representan los procesos de deformación y recristalización de las rocas debidos a los cambios de temp y pres: son los procesos de metamorfismo, que producen ese tipo de rocas.
· Las flechas rojas indican procesos de fusión de rocas, estos procesos transforman las rocas en magma que, al enfriarse y solidificar, origina rocas ígneas.
Este ciclo se produce continuamente en nuestro planeta, aunque es lento y no observable en la vida humana.
Utilización de las rocas.
-
Las rocas como recurso. Todo aquello que la humanidad obtiene de la naturaleza con el objetivo de utilizarlo se denomina recurso natural. Los recursos naturales se agrupan en dos grandes categorías:
· Los recursos energéticos son aquellos que se utilizan para la obtención de energía.
· Los recursos no energéticos son aquellos cuyo uso no tiene relación con la energía. Se utilizan como materias primas para la fabricación de materiales o la construcción.
-
Las rocas como recurso energético. Cuando hablamos de rocas de interés desde el punto de vista energético, nos referimos al petróleo y al carbón. Estas dos rocas se denominan combustibles fósiles.
· El carbón es una roca orgánica. Su combustión tiene import efectos contaminantes.
· El petróleo es también una roca orgánica. No se utiliza directamente, sino que se somete a una serie de procesos químicos muy complejos. De este proceso de refinado del petróleo se obtienen los combustibles: gasolina, gasóleo o queroseno.
El principal problema de las dos rocas es que son agotables. No sucede así con el uranio, fuente de la energía nuclear. El problema de esta fuente es su almacenamiento y el riesgo que conlleva
-
Los recursos minerales no energéticos. Las rocas y los minerales tienen una gran importancia como materias primas. Normalmente, se clasifican en dos grupos:
· Recursos metálicos, son todos aquellos minerales de los cuales se puede obtener metales (limonita, siderita).
· Recursos no metálicos, son el resto de recursos minerales que tienen alguna aplicación en la industria.
Las rocas se pueden utilizar en la construcción de diversas formas. Muchas de ellas, como el granito y el mármol, se utilizan como rocas ornamentales, o incluso como piedras de construcción en muros y fachadas.
Otro uso de las rocas, de gran importancia constructiva, es como aglomerantes: la cal o yeso. El cemento, probablemente es el más importante de los aglomerantes, se obtiene por calcinación de una mezcla de caliza y arcilla. Este producto se suele utilizar mezclado con arena, grava y piedra triturada, obteniendo el hormigón.
Por último, las rocas son también la materia prima para la elaboración de los materiales cerámicos y del vidrio.
Física y Química.
Esquema Diminuto de T.1.
-
Fenómenos físicos y químicos.
· La física es la ciencia que estudia los fenómenos físicos, aquellos en que las sustancias no modifican su composición ni se transforman en otras nuevas.
· La química es la ciencia que estudia los fenómenos químicos, es decir, la composición, la estructura y las propiedades de las sustancias, así como las transformaciones que pueden experimentar.
· Una magnitud física es toda propiedad de los cuerpos que puede ser medida.
Para medir una magnitud física comparamos su valor con una referencia que llamamos unidad de medida
-
Sistema Internacional de unidades. Para resolver el problema que suponía la utilización de unidades diferentes en distintos lugares del mundo, en la Conferencia General de Pesos y Medidas se estableció el Sistema Internacional (SI). Para ello, se obró de la siguiente manera:
· En primer lugar, se eligieron las magnitudes básicas y la unidad correspondiente a cada magnitud básica.
· A partir de éstas, se definieron las magnitudes derivadas y la unidad correspondiente a cada magnitud derivada.
| Magnitud básica | Unidad | Abreviatura |
| Longitud | Metro | m |
| Masa | Kilogramo | Kg |
| Tiempo | Segundo | S |
| Intensidad de corriente | Amperio | A |
| Temperatura | Kelvin | K |
| Intensidad luminosa | Candela | Cd |
| Cantidad de sustancia | mol | Mol |
-
Transformación de unidades. Un factor de conversión es una fracción igual a uno que expresa la equivalencia entre dos unidades:
1 m = 100 cm 100 cm
1m = 1
Factor de conversión
Al multiplicar la medida inicial por el factor de conversión, su valor no se modifica. Sin embargo, la unidad inicial desaparece y en su lugar aparece una nueva.
-
Notación científica. En muchas ocasiones las medidas tienen un número elevado de cifras. Para operar fácilmente con éstas expresamos las cantidades mediante notación científica, que consiste en escribir cada valor mediante una parte entera de una sola cifra no nula, en una parte decimal y una potencia de exponente entero.
Esquema del T.6.
Estados de agregación de la materia. Los cuerpos materiales presentan diferente forma y tienen distintas propiedades y características. Por ejemplo, el agua, según las condiciones ambientales, podemos encontrarla en forma de hielo, de agua líquida o de vapor de agua. Las demás sustancias que conocemos se presentan en diferentes estados de agregación: sólido, líquido y gaseoso.
· Los sólidos se caracterizan por tener forma y volumen constantes (cobre, mármol)
· Los líquidos tienen volumen constante pero forma variable: se adaptan al recipiente que los contiene. Son incomprensibles pues no puede reducirse su volumen.
· Los gases tienen forma y volumen variables, por eso tienden a ocupar todo el espacio disponible. Pueden comprimirse y expandirse con facilidad.
-
Modelo cinético-molecular de la materia. Para explicar el comportamiento de la materia y las características de los gases, los científicos propusieron la teoría cinética de los gases. Su ampliación a los líquidos y sólidos dio lugar al modelo cinético-molecular de la materia. Se basa en dos postulados:
· La materia es discontinua; está formada por un gran número de partículas separadas entre sí.
· Estas partículas se encuentran en constante movimiento debido a dos tipos de fuerzas: de cohesión y de repulsión.
- Las fuerzas de cohesión tienden a mantener las partículas materiales unidas entre sí.
- Las fuerzas de repulsión tienden a dispersarlas partículas y a alejarlas unas de otras.
Según el predominio de unas u otras fuerzas, la materia se presenta en estado sólido, líquido o gaseoso.
-
Sólido: predominan las fuerzas de cohesión sobre las de repulsión, por tanto, las partículas sólo pueden vibrar alrededor de su posición de equilibrio.
-
Líquidos: las fuerzas de cohesión y repulsión son equilibradas, por tanto, las partículas pueden desplazarse con cierta libertad pero sin alejarse unas de otras.
-
Sólidos: predominan las fuerzas de repulsión frente a las de cohesión, por tanto, las partículas se mueven con total libertad y están muy alejadas unas de otras.
-
Cambios de estado. El estado de agregación de un material puede cambiar si se modifican las condiciones ambientales, es decir, la presión y la temperatura.
Así, un material puede pasar del estado sólido al gaseoso o al líquido, y viceversa. Los procesos que experimenta se denominan cambios de estado. Las características pueden interpretarse a la luz del modelo cinético-molecular.
· Fusión y solidificación. La fusión es el paso de sólido a líquido. Para conseguirla hay que aumentar la temp del sólido. Al calentar un sólido, aumenta la energía de las partículas y, la amplitud de las vibraciones. Esta energía es suficiente para vencer las fuerzas de cohesión y las partículas comienzan a resbalar entre sí. Entonces comienza la fusión.
La forma de fusión de un cuerpo depende de su naturaleza. Así, distinguiremos entre los cuerpos cristalinos y los amorfos. En los cristalinos se produce a una temperatura constante denominada temperatura de fusión, mientras que en los amorfos en un intervalo amplio de temperaturas.
La solidificación es el paso de líquido al sólido. Para conseguirla hay que disminuir la temperatura del cuerpo, por lo que sus características son inversas a la fusión.
· Vaporización y condensación. La vaporización es el paso del estado líquido al gaseoso. Puede conseguirse aumentando la temp del líquido o bien disminuyendo la presión sobre él. Al calentar un líquido, aumenta la velocidad de desplazamiento de las partículas y su energía. Esta energía es suficiente para que las partículas próximas a la superficie del líquido puedan vencer las fuerzas de cohesión y escapar. Entonces se produce la vaporización. Ésta puede ser de dos tipos.
Evaporación es un fenómeno que se produce exclusivamente en la superficie del líquido y aumenta su temperatura. Cuando disminuimos la presión sobre el líquido, la evaporación también aumenta.
Ebullición es un fenómeno que afecta a toda la masa del líquido. Tiene lugar a una temperatura determinada, llamada temp de ebullición.
La condensación es el paso de estado gaseoso al líquido. Puede conseguirse tanto aumentando la temp como disminuyendo la presión sobre él.
· Sublimación y condensación a sólido. La sublimación es el paso del estado sólido al gaseoso, mientras que la condensación a sólido es el paso inverso. Para que se produzca es necesario que los cuerpos se encuentren en unas determinadas condiciones de presión y temp, que varían según la sustancia de que se trate.
Mezclas y sustancias puras. La gran diversidad de sustancias que encontramos en la naturaleza nos obliga a establecer una clasificación. Una forma sencilla se basa en la posibilidad o imposibilidad de poder separar la materia en sustancias más simples y en el método para llevarlo a cabo. Según esto clasificamos:
| La Materia |
Está formada por:
| Mezclas | Sustancias Puras |
· Tienen comp y prop variables. · Tienen composición fija y
· Pueden separase en otras más propiedades constantes y
simples. características.
· No pueden separarse en otras sustancias más simples mediante procesos físicos.
| Mezclas Heterogéneas Mezclas cuyas prop y comp varían de un punto a otro y podemos ver sus componentes. (granito) | Mezclas Homogéneas Mezclas cuyas prop y comp son iguales en todos sus puntos y no podemos ver sus comp (café) | Compuestos Sust puras que pueden descomp en otras más simples. (agua) | Elementos Sust puras que no pueden descomp en otras más simples. (hierro) | |||
-
Técnicas de separación de mezclas. Los componentes de una mezcla pueden separarse utilizando técnicas físicas.
· Para separar mezclas heterogéneas utilizamos filtración y decantación.
· Para separar mezclas homogéneas utilizamos destilación y cristalización.
Filtración. Para separar los componentes de una suspensión fina (mezcla de líquido y sólido en la que las partículas del último se encuentran dispersas en el primero). Consiste en separar las partículas sólidas de las del líquido por medio de un filtro, aprovechando la diferencia de tamaño entre ambas.
Decantación. Para separar dos tipos de mezclas: las emulsiones (dos líquidos inmiscibles que tienden a separarse en dos fases) y las suspensiones gruesas (las partículas del sólido tienden a depo. en el fondo o a sobrenadar el líquido aprovechando la diferencia de densidad).
Para separar las dos fases de una emulsión se emplea un embudo de decantación.
Para separar la fase líquida de la sólida que se encuentra en el fondo, inclinamos el vaso de precipitados y se vierte el líquido.
Para separar la fase sólida que sobrenada un líquido se utiliza una espátula.
Destilación. Se utiliza para separar los componentes de una disolución. Consiste en separar ambos componentes aprovechando la diferencia de punto de ebullición entre ambos. Para ello, se coloca la disolución en el interior del matraz y se calienta hasta que se produce la ebullición de la mezcla. El vapor desprendido es rico en componente de menor punto de ebullición. Cuando pasa a través del refrigerante, se condensa y puede recogerse en el vaso de precipitados.
Cristalización. Se utiliza para separar los componentes de una disolución formada por un sólido y un líquido. Consiste en separar ambos componentes aprovechando la mayor volatilidad del líquido, es decir, la facilidad de este para pasar a estado gaseoso.
Se deposita la disolución en un cristalizador para que el líquido se evapore lentamente: el sólido aparece en el fondo en forma de cristales.
Disoluciones. Es frecuente encontrar mezclas de dos o más sustancias (aire o sangre). Según su comportamiento, distinguimos dos clases de mezclas: las heterogéneas (sus propiedades son diferentes según la porción de mezcla que consideremos) y las homogéneas. Las mezclas homogéneas también se conocen con el nombre de disoluciones.
Una disolución es una mezcla cuyos componentes no pueden distinguirse unos de otros a simple vista ya que tiene una composición uniforme. Está formado por el soluto (sustancia que se disuelve y es el componente que se encuentra en menor cantidad) y el disolvente (sustancia que disuelve al soluto y es el componente que se encuentra en mayor cantidad).
-
Clases de disoluciones. Tanto el soluto como el disolvente pueden presentarse en estado sólido, líquido o gaseoso. Lo que da origen a 9 tipos de disoluciones según el estado físico de sus componentes.
| Tipo de disolución | Estado físico de lo comp | Estado físico de la disolución | Ejemplos | |
| Soluto | Disolvente | |||
| Gas en gas | Gas | Gas | Gaseoso | Aire |
| Gas en líquido | Gas | Líquido | Líquido | Bebida gaseosa |
| Gas en sólido | Gas | Sólido | Sólido | Hidrógeno en paladio |
| Líquido en Líq | Líquido | Líquido | Líquido | Gasolina |
| Líquido en gas | Líquido | Gas | Gaseoso | Aerosoles |
| Líquido en sól. | Líquido | Sólido | Sólido | Arcilla húmeda |
| Sólido en solid | Sólido | Sólido | Sólido | Aleaciones |
| Sólido en líqu. | Sólido | Líquido | Líquido | Azúcar en agua |
| Sólido en gas | Sólido | Gas | Gaseoso | Part de polvo en aire |
Las más habituales en el laboratorio de química son las disoluciones de sólidos en líquidos.
-
El proceso de disolución. Una disolución está saturada cuando a una temperatura determinada no admite más soluto. Para cada temperatura, la cantidad de soluto que hay en una disolución saturada depende de la solubilidad de dicha sustancia.
La solubilidad de una sustancia en un disolvente, a una temperatura determinada, es la máxima cantidad de soluto que puede disolverse en una cantidad fija de disolvente a dicha temperatura.
Cada sustancia tiene una solubilidad característica en un disolvente. También existen otros factores.
-
Comportamiento de una disolución.
Factores que influyen en la solubilidad. La presión y la temperatura. En general, la solubilidad de los gases en líquidos aumenta con la presión y disminuye con la temperatura, al igual que generalmente, la solubilidad de los sólidos en líquidos aumenta con la temperatura.
Factores que influyen en la velocidad de disolución de un sólido. La superficie y la agitación. En general, cuanto mayor sea la superficie de contacto y la agitación de la disolución, más rápida es ésta.
Elementos y compuestos. Los procesos descritos para separar los componentes de una mezcla no alteran las propiedades. Se trata de procesos físicos.
Sin embargo, para distinguir los componentes de una sustancia pura, hay que recurrir a otro tipo de procesos en los que sí se cambia la naturaleza de las sustancias: procesos químicos.
Utilizando estos y otros procedimientos químicos se ha investigado el comportamiento de la materia. De este modo se ha podido distinguir entre elementos y compuestos.
Los elementos son sustancias puras que no pueden descomponerse en otras más sencillas por métodos químicos (hierro).
Los compuestos son sustancias puras que sí pueden descomponerse en otras más sencillas mediante procesos químicos (agua).
El nº de elementos conocidos es de 109. Sin embargo, los compuestos se cuentan por millones.
-
La teoría atómica de Dalton. El desarrollo de la química moderna no se produce hasta el s XVIII cuando el científico británico John Dalton enunció su célebre teoría atómica en 1808. Los principios fundamentales de esta teoría son los siguientes:
· La materia está formada por pequeñas partículas, separadas e indivisibles, llamadas átomos.
· La sustancia que tiene todos sus átomos iguales se denomina elemento.
· Los átomos de elementos distintos pueden unirse en cantidades fijas para originar compuestos.
Tres años más tarde, el químico italiano Avogadro denominó moléculas a los átomos compuestos de Dalton.
-
Los elementos conocidos. La información que poseemos acerca de los elementos es muy diversa según su:
· Descubrimiento. Algunos elementos son conocidos desde la Antigüedad. Otros, han sido producidos artificialmente en los últimos años.
· Abundancia. La presencia de los elementos químicos en nuestro planeta es muy irregular: unos elementos son muy abundantes (oxígeno o silicio) pero otros muy escasos (cadmio o cinc).
· Forma de Presentación. Los elementos conocidos aparecen en su mayoría combinados entre sí en forma de compuestos (glucosa). Otros pueden presentarse no combinados (oxígeno o nitrógeno).
-
Elementos químicos básicos de los seres vivos. Los elementos químicos básicos de los seres vivos son el Carbono, Hidrógeno, Oxígeno y Nitrógeno como primarios, y el Calcio o el Hierro como secundarios. Todos estos se encuentran en los llamados principios inmediatos; que pueden ser orgánicos (Glúcidos, Proteínas, Lípidos y Ácidos nucleicos) e inorgánicos (Agua o Sales minerales).
-
Los símbolos de los elementos químicos. Cuando queremos acortar la escritura de una palabra utilizamos su letra inicial, a esto se la llame abreviatura. Los elementos químicos también se representan mediante abreviaturas que, reciben el nombre de símbolos.
Esquema T.7. Átomos y moléculas.
El átomo. La teoría atómica de Dalton resultó muy útil para interpretar el comportamiento de las sustancias. Sin embargo años más tarde se produjeron algunos descubrimientos que demostraron que los átomos no eran indivisibles; se descubrió la existencia de las partículas subatómicas, los electrones, protones y neutrones. Cada uno de estos descubrimientos provocó la aparición de un modelo atómico.
* El físico danés Bohr propuso un modelo atómico en el que los electrones giran entorno al núcleo en niveles energéticos bien definidos. Cada uno de estos sólo puede contener un nº determinado de electrones. Para que un electrón cambie de nivel, es necesario modificar su energía en una cantidad determinada.
-
El modelo atómico actual. Los diferentes modelos atómicos desarrollados a lo largo del s XX pusieron de manifiesto la existencia de dos partes bien diferenciadas: El núcleo y la corteza.
· El núcleo es la parte central del átomo y en él se encuentran los protones y neutrones.
- Los protones son partículas con carga eléctrica positiva.
- Los neutrones son partículas sin carga y de masa aproximadamente igual a la de los protones.
· La corteza es la parte exterior del átomo y contiene los electrones, cuya masa es unas 2000 veces menor a la de los protones. Los primeros s encuentran distribuidos en diferentes niveles energéticos y ocupando orbitales.
- Los niveles energéticos se enumeran del 1 al 7 por orden creciente de energía: el 1 es el menos energético y el 7 el que más.
- Los orbitales son regiones del espacio, en torno al núcleo, donde la probabilidad de encontrar electrones es muy grande.
Masa, carga y volumen de un átomo.
· La masa de un átomo se concentra en el núcleo, la masa de los electrones es insignificante.
· En todos los átomos, el nº de protones es igual al nº de electrones de la corteza, por lo que el átomo carece de carga, es eléctricamente neutro.
· El volumen que ocupa el átomo es aproximadamente 10, elevado a la quince, veces mayor que el volumen del núcleo.
-
Nº atómico y nº másico. Para distinguir los átomos de un elemento de otro hemos de considerar los dos parámetros superiores.
· El nº atómico, Z, es el nº de protones que tienen los núcleos de los átomos de un elemento.
· El nº másico, A, es la suma del nº de protones y el nº de neutrones que tiene el núcleo de un átomo.
El nº atómico y el másico, suelen representarse junto con el símbolo del átomo correspondiente de la siguiente manera:
-
Isótopos y masa atómica. Muchos elementos poseen átomos que teniendo el mismo nº Z tienen distinto nº A.
· Llamamos isótopos a las formas atómicas de un mismo elemento que se diferencian en su nº másico.
Masa atómica. La unidad que se emplea para determinar la masa de un átomo se denomina unidad de masa atómica, u, y se define como la doceava parte de la masa de un átomo de carbono (pues lo ponen como referencia) que es 12. Por tanto esto equivale a la masa de un protón o neutrón. Y la masa atómica de un elemento se define como:
· La masa atómica de un elemento es el número de veces que un átomo de este elemento contiene la unidad de masa atómica.
-
Estructura electrónica. Según la energía de los distintos niveles, éstos pueden contener diferentes tipos de orbitales, denominados s, p, d y f.
La configuración electrónica de un átomo es la distribución de sus electrones es los diferentes niveles y orbitales, ordenados de menor a mayor energía.
-
Agrupaciones de átomos. Distinguimos entre elementos y compuestos.
· Los elementos están formados por átomos iguales y no pueden descomponerse en otros más sencillos. Hierro.
· Los compuestos están formados por moléculas iguales que sí pueden descomponerse en otros materiales más sencillos. Agua.
Tanto los elementos como los compuestos son materiales de composición fija, por ello se denominan sustancias puras.
Los científicos pensaron que las unidades mínimas de los elementos eran los átomos y la de los compuestos las moléculas. Pronto se descubrió que no era exactamente así.
En los elementos; el oxígeno forma moléculas diatómicas, constituidas por dos átomos. En cambio el hierro forma una tupida red cristalina de átomos. Los átomos de las sustancias que están formadas por un único elemento se agrupan en redes cristalinas o moléculas.
En los compuestos; el dióxido de carbono forma moléculas en las que hay un átomo de carbono y dos de oxígeno. La arena o sílice forma una red cristalina en la que hay un átomo de silicio por cada dos de oxígeno. Los átomos de los compuestos también se agrupan entre sí formando moléculas aisladas o redes cristalinas.
· Las moléculas de un elemento están formadas por dos o más átomos de un mismo elemento. Las moléculas de compuestos están formadas por dos o más átomos de diferentes elementos.
· Las redes cristalinas están formadas por un número indeterminado de partículas elementales que se disponen constituyendo una estructura geométricamente ordenada.
-
La regla del octeto. ¿Por qué los átomos presentan tendencia a unirse entre sí? Se unen porque adquieren una situación más estable cuando están separados. Depende de su configuración electrónica relacionada con los gases nobles.
· Los gases nobles. No presentan ninguna tendencia a reaccionar ni a formar agrupaciones de átomos. El análisis de su configuración electrónica muestra que, a excepción del He, todos los gases nobles tienen ocho electrones en su nivel más externo.
Se admite que los átomos de los elementos tienden a rodearse de ocho electrones en su nivel más externo para ganar estabilidad. Este comportamiento recibe el nombre de regla del octeto.
· Los átomos de los elementos tienden a ganar, perder o compartir electrones para conseguir que su nivel más externo adquiera la configuración de gas noble.
-
El enlace químico. Es la unión que se establece entre los átomos o las partículas elementales que constituyen una sustancia.
Pero las sustancias presentan agrupaciones muy diversas. Este diferente comportamiento se debe a la existencia de distintos tipos de enlaces: iónico, covalente o metálico.
-
El enlace iónico. El ion es un átomo o un grupo de estos que ha ganado o perdido uno o más electrones y ha adquirido carga eléctrica positiva o negativa respectivamente. Según si la tendencia de los átomos es perder o ganar electrones distinguiremos entre iones positivos o cationes (cuando un elemento pierde uno o más electrones y estos elemento se denominan elementos metálicos) y iones negativos o aniones (cuando un elemento gana uno o más electrones y dicho elemento se denomina elemento no metálico).
· El enlace iónico es la unión que resulta de la presencia de fuerzas de atracción electrostática entre iones de distinto signo.
-
Enlace covalente. Cuando la tendencia a ganar electrones es similar, los átomos se aproximan bastante, los orbitales de los electrones más externos se solapan entre sí y forman un nuevo orbital (orbital molecular) mediante el cual comparten los electrones que aporta cada átomo.
· El enlace covalente es la unión de dos átomos que comparten uno o más pares de electrones. Así el nivel más externo se ha completado con ocho electrones.
-
El enlace metálico. Los átomos de los metales pueden perder algunos de los electrones de su nivel más externo y convertirse en iones positivos que forman redes cristalinas. Los electrones perdidos forman una nube electrónica que envuelve a la red. Estos electrones pueden desplazarse entre sí.
· El enlace metálico es la unión que existe entre los átomos de los metales, que se encuentran formando una red cristalina.
-
Tipos de sustancias. El tipo de enlace condizoa las prop de las sust que lo presentan.
| Sust iónicas (Sal) | Sust covalentes (Agua) | Metales (Hierro) | |
| Estructura | Red cristalina iónica | Moléculas y red cristalina d´atómo | Red cristalina metálica. |
| Estado nat | Sólidas | Sólidas, líquidas y gaseosas. | Sólidas (- Mercurio). |
| Solubilidad | En agua | Insolubles en agua | Solubles entre sí, fusión. |
| Conduct.dad | Conducen corriente | No conducen | Buenos conductores. |
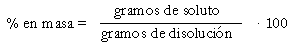
![]()
![]()
![]()
![]()
Descargar
| Enviado por: | Toledano |
| Idioma: | castellano |
| País: | España |
