Química
Modelos atómicos
Modelos atómicos
Modelo atómico de Thomson
Thomson demostró en 1897 la existencia de partículas cargadas negativamente, los electrones; y con los llamados rayos canales o rayos positivos, que pueden observarse como un fino haz de luz detrás de un tubo de descarga con el cátodo perforado, llegó a la conclusión de que el átomo no podía ser una esfera rígida de material característico para cada elemento.
Además determino la relación entre la carga y la masa de los electrones, demostrando que esta relación era constante e independiente del material utilizado.
En 1904, Thomson después de medir las características del electrón, intuyó la existencia de carga positiva en el átomo, dada la neutralidad de la materia. Propuso un modelo de átomo que consistía en una esfera maciza cargada positivamente dentro de la cual estaban embebidos los electrones necesarios para neutralizar la carga. Algo así como si fuera “un pastel esférico, relleno de pasas”, en el que las pasas vendrían a ser los electrones.
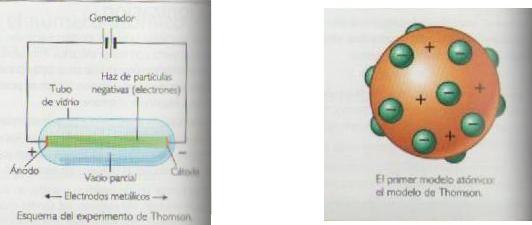
Modelo atómico de Rutherford
Sabiendo ya que en los átomos hay cargas positivas y negativas, y que además, por ser neutros, el número de cargas negativas debe ser igual al de carga positiva, se trató de investigar como se halla distribuidas esas cargas en el interior del átomo.
En 1911, Ernest Ruthenford, profesor de física de Manchester (Inglaterra), realizó experiencias que demostraron que la masa del átomo se halla concentrada en partículas de tamaño muy pequeño en comparación de los átomos del mismo.
Consistía en bombardear con partículas alfa (partículas positivas) una finísima lámina de oro; detrás de la lámina se colocaba una placa fotográfica para estudiar la trayectoria de las partículas: Colocó una sustancia radioactiva, emisora de partículas alfa, cerca de una delgadísima lámina de oro separada de aquella por pantallas con agujeros en sus centros de modo que la difeccion de sus rayos alfa emitidos quedara bien determinada.
Las direcciones de las partículas a se detectaban con una pantalla de sulfuro de cinc. Cuando esta pantalla era alcanzada por las partículas a, producía un destello escintilacíon.
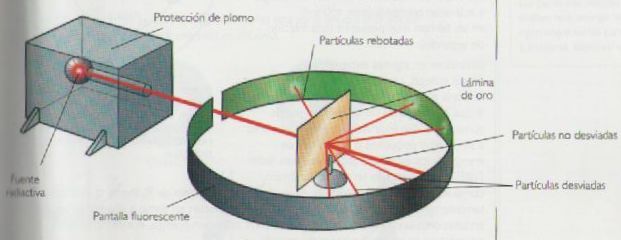
El espesor de la lámina en el experimento era de unos 0,0005mm, es decir, unos 400 átomos de oro seguidos.
La mayor parte de las partículas atravesaban la lámina (espesor de la lámina: 5.000Å; material: oro), algunas no eran desviadas y otras se desviaban con ángulos mayores de 90°.
Ocurría lo siguiente:
*la mayoría de las partículas atravesaban la lámina de oro sin desviarse.
*una pequeña porción atravesaba la lámina con una ligera desviación en su trayectoria.
*solo una de cada 10.000 partículas rebotaba y no atravesaba la lámina.
Esta experiencia reveló que:
-
La mayoría de las partículas atravesaban la lámina sin desviarse. Las partículas a pudieron atravesar las partículas de oro esto era así por que el átomo posee espacios vacíos; solo había algunos electrones girando alrededor del núcleo y la masa de los electrones es muy pequeña.
-
La desviación solo podía ser provocada por masa muy grandes respecto de las partículas a. Las partículas que se desviaban eran las que pasaban cerca del núcleo, se repelían (ambas tiene carga positiva) y sufrían una pequeña desviación.
-
Solo una de cada 10000 partículas rebotaban y no atravesaban la lámina. Las partículas que rebotaban eran las repelidas por el núcleo. El tamaño del núcleo era muy pequeño comparado con el tamaño total de átomo, unas 10.000 veces mas pequeño.
Un poco después, en 1920, Rutherford propuso la existencia de otra partícula en el núcleo .La denominó neutrón, tendría la masa del protón y carecía de carga .La evidencia experimental de esta partícula no se tuvo hasta 1932 con los experimentos de Chadwick.
Este modelo explica la experiencia de Rutherford; sin embargo, sería imposible explicar con el modelo de Thomson por que la mayoría de los protones atraviesan la lámina de oro.
Por cálculos matemáticos y basados en experiencias, Ruthenford dedujo que el átomo tiene un núcleo central cargado positivamente, cuyo diámetro es 10ˉ del diámetro de todo el átomo.
La teoría de Ruthenford se amplió cuando demostró que la masa de las cargas positivas nucleares es aproximadamente igual a la mitad de la masa del átomo.
Basándose en su experimento, Rutherford estableció el siguiente modelo atómico: el átomo está formado por un núcleo y una corteza:
-
El átomo posee un núcleo central cargado positivamente, con un diámetro promedio de 10ˉcm, rodeado de electrones (que ocupan la mayor parte del volumen atómico).
-
El átomo tiene grandes espacios vacíos; su diámetro promedio total es de 10ˉ cm.
-
El núcleo del átomo posee casi toda la masa de éste.
-
Siendo el átomo eléctricamente neutro, la carga negativa total de sus electrones debe compensar la carga positiva de los protones de su núcleo.
-
Como las cargas eléctricas de protones y electrones son iguales en valor absoluto y de signo contrario, el número de protones del átomo es igual al número de sus electrones.
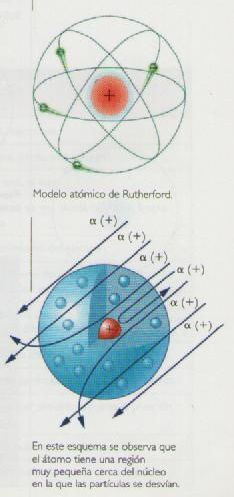
El modelo de Bohr
Cuando Rutherford enunció su modelo, no tuvo en cuenta algunos trabajos publicados por sus contemporáneos y que ponía en evidencia algunos aspectos negativos de su teoría. El principal inconveniente del modelo de Rutherford radica en que si los electrones, que son partículas cargadas, están girando alrededor del núcleo, va perdiendo energía y acabarían precipitándose sobre él en un tiempo muy pequeño (una fracción de segundo).
El físico danés Niels Bohr (1885-1962) propuso, en1913, una reforma fundamental al planetario de Ruthenford, Basándose en algunas experiencias de sus colegas, como el efecto fotoeléctrico, la teoría cuántica de Plack y Einstein (según la cual la energía de un sistema no puede aumentar o disminuir de forma continua, sino a saltos muy pequeños o “cuantos” de energía) y los espectros atómicos; le permitió explicar matemáticamente la discontinuidad de los espectros de los elementos en estado de incandescencia o de excitación eléctrica.
La experiencia de los espectros de raya indica que la energía de los electrones está cuantificada o empaquetada”, hallándose restringida a valores limitados y determinados.
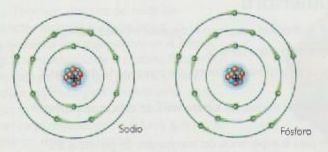
Bohr propuso un modelo atómico, compuesto por un núcleo y corteza. Al igual que el modelo de Rutherford, el átomo también tenía un núcleo positivo y los electrones giraban en torno a él, pero lo hacían en unas órbitas circulares, donde no admiten o absorben energía. A estas “órbitas permitidas” se les llamo niveles de energía.
Los electrones, al pasar de un nivel energético a otro, lo hacen absorbiendo o emitiendo cantidades definidas, “cuantos” o paquetes de energía de manera instantánea, no gradual, que se traducen en forma de luz.
La propuesta sobre la estructura del átomo de nitrógeno de Bohr se resume en estos principios:
-
Un electrón puede girar en órbitas o niveles determinados sin emitir o absorber energía.
-
Estos niveles, en los que el electrón no modifica su energía, se denominan “niveles estacionarios”.
-
Cuando el electrón se halla en “ estado de estabilidad”, gira en el nivel mas próximo al núcleo por ser este el de menor energía
-
Si el electrón, por choque, calor, electricidad, etc., absorbe energía, lo hace en formas de “cuantos de energía” y pasa a un nivel mas alejado de núcleo: entonces se dice que el electrón está “excitado”
-
En estado de excitación, el electrón es inestable y “salta” o “pasa” a otro nivel de energía, con emisión de energía luminosa cuantificada.
-
La energía liberada por el electrón es una cantidad definida igual a la diferencia de energía entre ambos niveles.
-
Esa diferencia es igual a la frecuencia de la luz emitida multiplicada por una constante llamada de Planck.
Más tarde, Arnold Sommerfeld (1868-1951), en una ampliación de modelo de Bohr, supuso que las órbitas también podían ser elípticas.
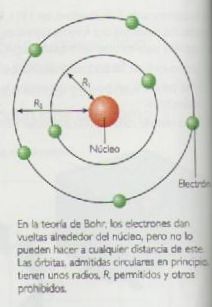
Modelo atómico actual
El modelo atómico de Bohr es muy útil, pero la ciencia va evolucionando y experiencias posteriores llevaron a abandonar la idea de las órbitas estacionarias de Bohr, que se regían según las leyes de la mecánica clásica, para establecer una nueva mecánica; la mecánica cuántica. Sus padres fueron: Werner Kart Heisenberg (1901-1976), Edwin Schrödinger (1887-1961) y Paul Dirac (1902-1984).
Se abandonó el concepto de órbita estacionaria, debido fundamentalmente a que no se no se puede determinar con precisión la posición exacta de un electrón en un determinado instante.
En la mecánica cuántica se define el orbital como una zona del espacio donde la probabilidad de encontrar al electrón es la máxima.
Ya se ha admitido, según la estructura atómica iniciada por Thomson y perfeccionada por Bohr y Ruthenford, y aplicando la teoría cuántica al átomo de hidrógeno, que:
-
El átomo posee carga positiva en los protones del núcleo y cargas negativas en los electrones ubicados en los diferentes niveles energéticos
-
Como las cargas eléctricas (unitarias) son iguales (en valor absoluto) y de signo contrario para protones y electrones, y el átomo es eléctricamente neutro, el número de protones debe ser igual al número de electrones.
-
Conociendo la masa de un protón y la de un electrón (1,7.10ˉ²g y 9,1.10ˉ²g ), se observó que en casi todos los átomos (exceptuando el hidrógeno) la suma de las masa de protones y electrones era menor que la masa del átomo
Investigando esa diferencia James Chadwick identificó en el año 1932 una partícula de masa igual a la del protón, pero sin carga eléctrica, a la que denominó neutrón.
-
Esta partícula neutra se halla en el núcleo atómico, de manera tal que la suma de las masas de los protones y de los neutrones coincide, con gran aproximación, con la masa del átomo.
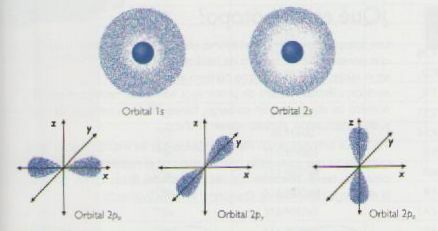
Los puntos representan la zona orbital de máxima probabilidad de encontrar al electrón.
| Científico/s, fecha | Avances |
| Leucipo y Demócrito, siglo V a.C. | Teoría atomística: partículas muy pequeñas, “átomos”. |
| Empédocles, siglo V a.C. | Materia formada por 4 elementos: agua, tierra, fuego y aire. |
| Aristóteles, siglo I V a.C. | Añadió un 5to elemento que venía del cielo: el éter. |
| J. Dalton, 1803 | Teoría atómico-molecular. La teoría de Dalton es una teoría científica, frente a las especulaciones de los filósofos griegos. |
| J. J. Thomson, 1897 | Modelo atómico “pastel de pasas”. Descubrimiento del electrón. |
| E. Rutherford, 1911 | Modelo planetario para el átomo. Descubrimiento del protón. La mayor parte del átomo está vacía: las cargas positivas se sitúan en la parte central: el núcleo. |
| N. Bohr, 1913 | Modelo de niveles de energía basado en la teoría cuántica y en los espectros. Los electrones se sitúan en torno al núcleo en diferentes capas o niveles. |
| A. Sommerfeld, 1916 | Órbitas elípticas, introducción de los subniveles de energía. |
| L. de Broglie, 1924 | Modelo onda-partícula para el electrón. Toda partícula lleva asociada una onda. |
| W. K. Heisenberg, 1926 | Principio de incertidumbre. Es imposible conocer simultáneamente la posición y la velocidad de una partícula. |
| E. Schrödinger, 1927 | Ecuación de onda para el electrón. Mecánica cuántica ondulatoria. |
| J. Chadwick, 1932 | Descubrimiento del neutrón. El átomo queda definitivamente al descubierto |
Descargar
| Enviado por: | Adriana Fresco |
| Idioma: | castellano |
| País: | Argentina |
