Química
Termodinámica del equilibrio de un Zwitterión
Termodinámica del Equilibrio de un Zwitterión
Introducción
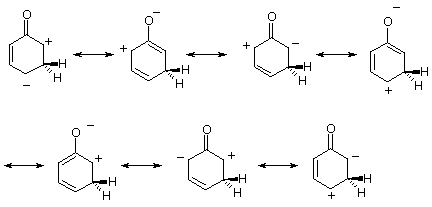
Zwitterión es un compuesto neutral con todo la geometría no permite un esquema simple de la vinculación. las estructuras principales de la resonancia son los zwiteriones y las siete estructuras posibles de la resonancia se representan en el esquema siguiente.
La posición de equilibrio depende de la habilidad del disolvente de donar puentes de hidrógeno y de las características dieléctricas y de la polarizabilidad del disolvente.
Si se incrementa la temperatura, el equilibrio se desplaza hacia la forma menos polar la lactona.
Por esta razón las altas concentraciones tienden a aparecer dos formas de la RB(catión y dímero)
Objetivos
1.Determinar calorimétricamente una constante de equilibrio.
2.Estudiar el efecto térmico sobre una constante de equilibrio
Conclusiones
-
Determinamos mediante la utilización del colorante xanteno rodamina, a constante de equilibrio ya que debido a los cambios de color del colorante, se midieron las A(absorbancia) a diferentes temperaturas obteniéndose las concentraciones de Z y L a dichas temperaturas
-
Las posibles causas de error están: No haber calibrado correctamente la escala, haber extrapolado mal.
-
Se comprobó al estudiar el efecto térmico sobre la K de equilibrio, que la temperatura la hace variar de siguiente forma, si la reacción es exotérmica, y se aumenta la temperatura, la K disminuirá, y si es endotérmica, aumentará.
-
La reacción de equilibrio L=Z es una reacción exotérmica, ya que al aumentar la temperatura, la K de equilibrio disminuyó.
-
Sugerencias: Si se cometió algún error, que es muy posible por la falta de conocimiento de la utilización del Spectronic 20.
Bibliografía
Guía de laboratorio
Levine, Ira. Físico Química.
Chang, Raymond. Química. McGraw Hill.México, 1999.
D.A.Hinckley y P.C Seybold, J.. Chem Ed.64, 362(1987)
Descargar
| Enviado por: | Skydriver |
| Idioma: | castellano |
| País: | Panamá |
