Ingeniero de Telecomunicación
Química. Enlaces químicos
-
OBJETIVO:
Observar las características de los diferentes tipos de enlaces, tales como iónico, covalente, covalente coordinado, covalente polar y por puente de hidrógeno, además de identificar algunos elementos a la flama.
-
INTRODUCCIÓN GENERAL:
ENLACE IONICO.
Consiste en la atracción electrostática entre átomos con cargas eléctricas de signo contrario. Este tipo de enlace se establece entre átomos de elementos poco electronegativos con los de elementos muy electronegativos. Cuando una molécula de una sustancia contiene átomos de metales y no metales, los electrones son atraídos con más fuerza por los no metales, que se transforman en iones con carga negativa; los metales, a su vez, se convierten en iones con carga positiva. Entonces, los iones de diferente signo se atraen electrostáticamente, formando enlaces iónicos.
ENLACE COVALENTE.
La combinación de no metales entre sí no puede tener lugar mediante este proceso de transferencia de electrones, en estos casos, el enlace consiste en una compartición de electrones; el enlace covalente es la formación de pares electrónicos compartidos, independientemente de su número.
El par compartido es aportado por sólo uno de los átomos formándose entonces un enlace que se llama coordinado o dativo.
Si los átomos son no metales pero distintos (como en el óxido nítrico, NO), los electrones son compartidos en forma desigual y el enlace se llama covalente polar —polar porque la molécula tiene un polo eléctrico positivo y otro negativo, y covalente porque los átomos comparten los electrones, aunque sea en forma desigual. Estas sustancias no conducen la electricidad, ni tienen brillo, ductilidad o maleabilidad.
-
ENLACE COVALENTE E IÓNICO:
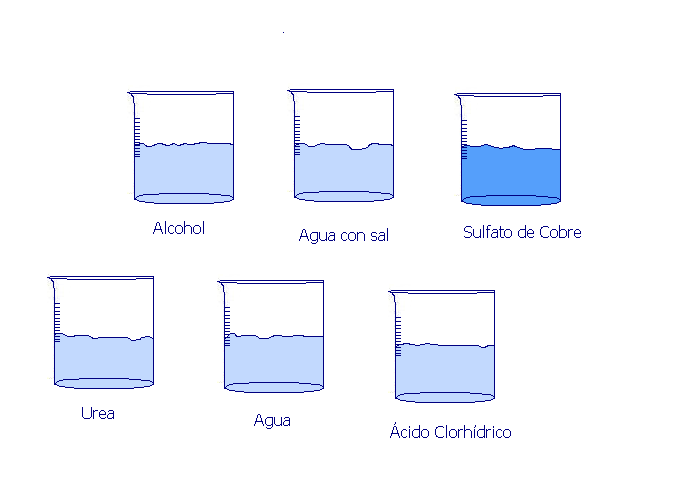
1. Colocar en 5 vasos de precipitados las siguientes sustancias:
-
Solución de NaCl (cloruro de Sodio)
-
Solución de Urea
-
Solución de CuSO4 (Sulfato de Cobre)
-
Cloruro de Amonio
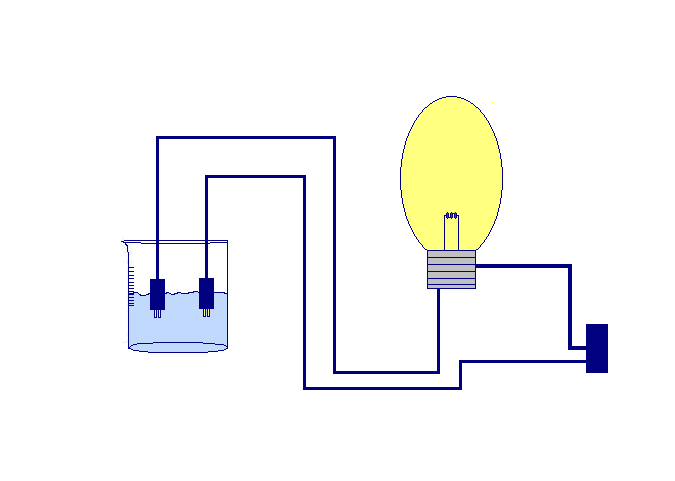
2. A cada vaso de precipitado se le introduce los polos de un circuito eléctrico con un foco, si no prende es un enlace covalente:
-
Agua
-
Urea
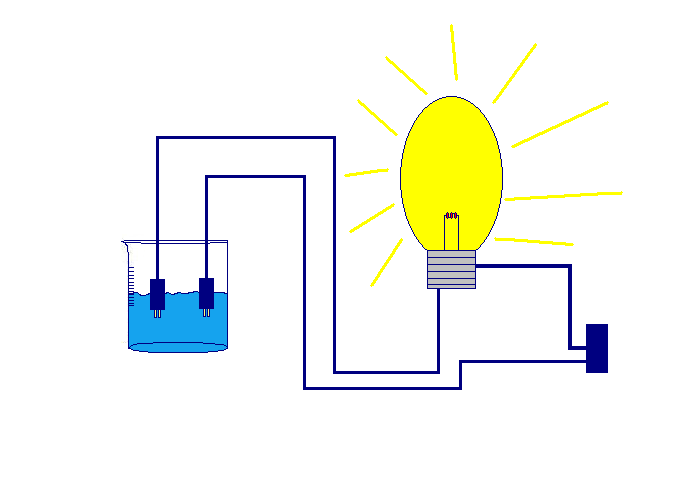
Si prende es un enlace iónico:
-
CuSO4
-
ENLACE COVALENTE COORDINADO:
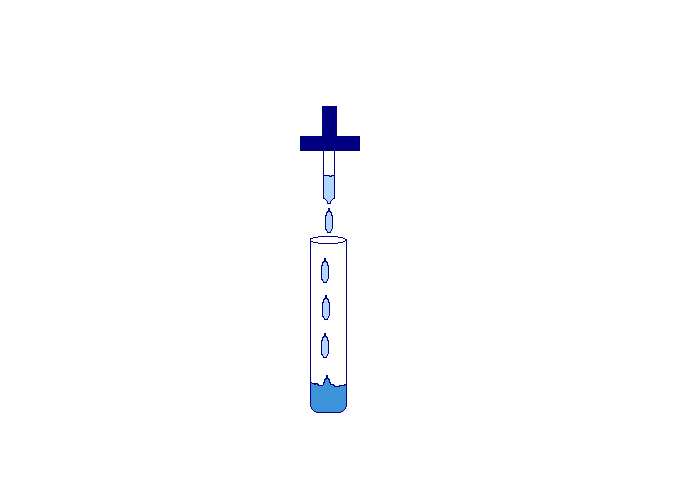
En un tubo de ensaye se le pone CuSO4 y se le agrega hidróxido de amonio.
2. Y se colorea de azul brusia.
3. Se coloca el compuesto en un vaso de precipitados.
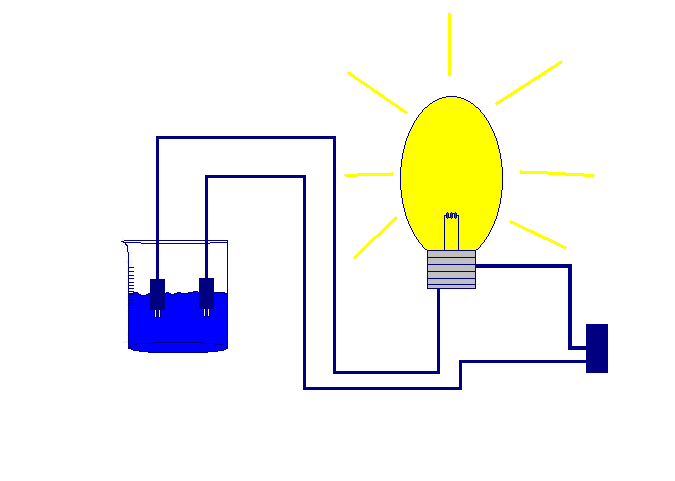
Al meter la lámpara, esta prende por el exceso de hidróxido de amonio.
-
CONCLUSIÓN GENERAL:
Pude observar la diferencia entre cada enlace (covalente, covalente coordinado, covalente polar e iónico), introduciendo los polos del circuito eléctrico con un foco, y si prendía es que era un en lace iónico y si no un enlace covalente.
La urea, no prendió el foco por lo tanto tiene enlace covalente.
El NaCl, si prendió el foco por lo tanto tiene enlace iónico.
El CuSO4, si prendió el foco por lo tanto tiene enlace iónico.
El cloruro de amonio, fue el que mas condujo electricidad, por lo tanto tiene enlace iónico.
-
BIBLIOGRAFÍA:
-
Encarta 2000, “Enlaces Químicos”
-
Enciclopedia Temática Multimedia Grijalbo, “Puentes de hidrógeno”
Practica 4
Practica 4
Descargar
| Enviado por: | Gori |
| Idioma: | castellano |
| País: | México |
