Química
Química
Examen de Química
2º Parcial.
Dentro de una capa dada. Compare las energías de las subcapas s, p, d, f, de un átomo con muchos electrones. Es decir, compare las energías de los orbitales dentro de una subcapa. (Con gráficas)
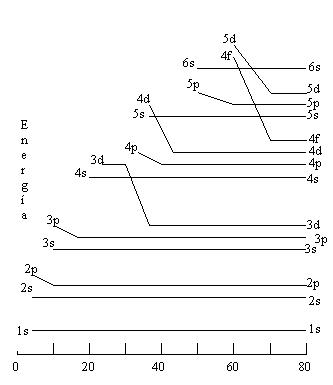
Esta pregunta se responde con la teoría de Hartree la cual predice que la energía de la subcapa se vuelve más negativa conforme disminuye los valores de n y l. Esto puede verse en la tabla 1. La subcapa 1s, que es la única subcapa en la capa n =1 tiene la energía más baja. Las dos subacapas de la capa n =2 son ambas de mayor energía y de estas, la subcapa 2s tiene una energía menor que la subcapa 2p. En la capa n =3 las subcapas 3s, 3p y 3d también se encuentran ordenadas por la energía, de acuerdo con la teoría de Hartree. Sin embargo la energía de la subcapa 4s en realidad es más baja que la correspondiente a la capa 3d ya que, la dependencia en l de la energía Enl de las subcapas puede ser más importante que la dependencia en n en capas externas con valores grandes de n.
Las subcapas externas siempre satisfacen la siguiente regla:
“Dada una n, la subcapa externa con menor l tendrá la menor energía. Dada una l, la subcapa externa con la menor n tendrá la menor energía”
Sabiendo esto podemos concluir que cuando n =1 tiene menor energía y cuando n = 6.... tiene mas energía.
Z
3. Identifique el elemento específico que corresponde a las siguientes configuraciones.
1s2, 2s2, 2p6, 3s2.
Esta configuración electrónica pertenece al Mg (Magnesio)
[Kr] 5s2, 4d10, 5p4.
Esta configuración electrónica pertenece al Telurio.
Se desglosa de la siguiente manera:
1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d,10, 4p6, 5s2, 4d10, 5p4.
Identifique el número de suborbitales que cada una de las designaciones siguientes pueden tener.
N = 5 número de suborbitales = 9
4f número de suborbitales = 7
5dxy número de suborbitales = 5
TABLA 1
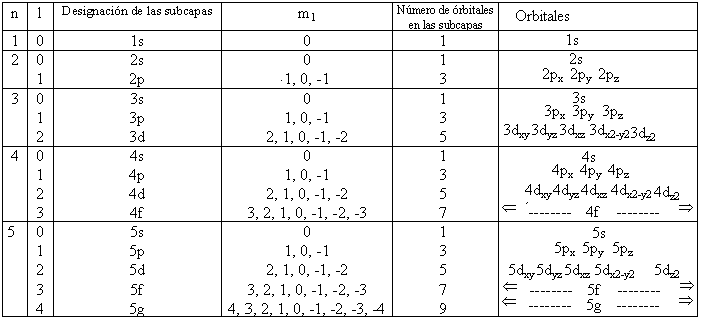
A continuación se muestra una tabla de notación electroscópica para justificar el porque de que cuando l = 4 se pone en el orbital la letra ..g.
TABLA 2
| l | 0 1 2 3 4 5 6 ... |
| Notación electroscópica | s p d f g h i ... |
¿En que año fue fundada la UVM y por quién?
La Universidad del Valle de México comenzó su labor educativa el 16 de Noviembre de 1960 en la Institución Harvard, con una población de 212 estudiantes, 23 profesores y 14 colaboradores administrativos impartiendo nivel básico, medio básico y medio superior, bajo la batuta de los Sres. Don José Ortega Romero, Don Ignacio Guerra Pellegaud, Don Alejandro Pearson, Don Salvador Camilleri, Don Jorge Malo y Don Manuel Olivar. Cabe destacar que la más importante de todas estas personas fue el señor Don José Ortega Romero quien siguió con este ambicioso proyecto después que los demás fundadores se retiraron.
Descargar
| Enviado por: | Alex |
| Idioma: | castellano |
| País: | México |
