Química
Química industrial y de laboratorio
INTRODUCCIÓN A LA QUÍMICA INDUSTRIAL
La química industrial, también conocida con el nombre de química técnica o ingeniería química, es la rama de la química que se dedica a transformar compuestos químicos básicos en otros productos químicos de gran demanda. La industria química se ocupa de la extracción y procesamiento de las materias primas, tanto naturales como sintéticas, y de su transformación en otras sustancias con características diferentes de las que tenían originariamente. Estas transformaciones se llevan a cabo mediante una serie de reacciones químicas muy complejas.
La domesticación del fuego fue lo que permitió a la humanidad manipular las primeras artes químicas, pero hasta el siglo XVI no se percibe una actividad productiva organizada. El aumento del nivel de vida y las demandas crecientes de la población en los países industrializados trajeron consigo nuevos requerimientos energéticos y de suministros. Hoy la química es uno de los pilares de la producción primaria de cualquier país desarrollado.
Química de laboratorio e industrial
Se pueden distinguir los siguientes términos:
-
La industria química, que es el conjunto de actividades dedicadas a la manufactura de elementos químicos y de sus compuestos y derivados.
-
Una empresa química es una unidad económica de producción y distribución de los productos químicos.
-
Una planta química es la parte de una empresa dedicada expresamente a la producción química. La ubicación de una de estas plantas químicas tiene que tener en cuenta una serie de condiciones, como la distancia a los puntos de obtención de las materias primas, etc.
Todo proceso industrial nace en un laboratorio, donde se hacen los cálculos precisos, pero el proyecto del proceso en una planta de producción debe prever aspectos que no se consideran en un laboratorio antes de la puesta en marcha de un proceso de producción. Para ello se construyen las llamadas plantas piloto, donde se comprueba la viabilidad del proceso de fabricación y se evalúan los rendimientos y los posibles riesgos sobre un funcionamiento muy parecido al que tendría la planta definitiva.
TIPOS Y SECTORES DE LA INDUSTRIA QUÍMICA
La preparación industrial de un producto suele ser muy diferente (en cuanto a los procesos utilizados) a la obtención de dicho producto en un laboratorio, pues en éste último se suelen utilizar métodos más sencillos, pero menos eficaces. En un principio las operaciones de la industria química tan sólo diferían de las de los laboratorios en pequeñas modificaciones o aumentos del tamaño de los aparatos y máquinas utilizadas. En la actualidad cualquier proceso químico tiene que seguir una serie de pasos obligados (que asegurarán el perfeccionamiento de dicho proceso) antes de convertirse en proceso industrial (además, no se desarrollará a gran escala hasta que se haya demostrado su rentabilidad): en primer lugar es necesario un estudio detallado en un laboratorio de la viabilidad de las reacciones, estos estudios previos a la utilización de una reacción con fines industriales son esenciales y tienen como objetivo el conocimiento de las condiciones óptimas en las que se debería llevar a cabo una reacción de forma que se obtenga el máximo rendimiento posible en el menor tiempo; tras estos primeros estudios se harán ensayos en plantas o instalaciones piloto, momento en el cual habrá que enfrentarse con los problemas prácticos que se plantean en las industrias; una vez hecho todo esto, el proceso de producción se llevará a cabo en la planta industrial.
Tipos de plantas químicas
Las plantas químicas se clasifican según el tipo de productos que se fabrican, y el empleo que después se les da:
-
Plantas químicas básicas o de cabecera En ellas se trabaja con materias primas naturales, para fabricar productos sencillos semielaborados (transforman las materias primas como hulla, petróleo, gas natural, fosfatos, sal o celulosa en una amplia gama de productos como amoniaco, ácidos, alquitranes, carburantes, abonos, cauchos sintéticos, explosivos, disolventes, barnices, textiles químicos y plásticos, etc.). Las materias primas que utilizan las obtienen del aire (oxígeno y nitrógeno), del agua (hidrógeno, el agua se utiliza como disolvente y reactivo), de la tierra (minerales, carbón y petróleo) o de la biosfera (madera, caucho, grasas...). Este tipo de industrias se suelen encontrar en lugares cercanos a las fuentes de suministro. Requieren grandes inversiones financieras en la forma de capital o de infraestructuras y dos de las ramas más importantes de esta industria son la carboquímica (en la que el carbón mediante las reacciones de descomposición química proporciona alquitrán, amoniaco y benzol, así como ácidos, abonos, gasolina, caucho sintético, colorantes y productos plásticos; aunque la carboquímica había sido desbancada casi completamente por la petroquímica, ahora puede verse reforzada con las nuevas bases industriales y socioeconómicas que contemplan los pros y los contras de la dependencia del petróleo para la economía y respecto al medio ambiente) y la industria petroquímica (en la cual se refina el petróleo crudo o bruto para elaborar un sinfín de productos como keroseno, gasoil, lubrificantes, disolventes, pinturas, detergentes, herbicidas, abonos, aislantes, productos sintéticos, cosméticos y plásticos).
-
Plantas químicas intermedias. Los productos intermedios son compuestos estables que pueden originar cada uno unos cuantos productos finales, pero que no son directamente utilizables por el consumidor. Como ejemplo de este tipo de productos se pueden citar el fenol o el cloruro de vinilo, los cuales pueden producir diversas resinas y plásticos.
-
Plantas de química fina. Fabrican productos intermedios pero de elevada pureza y rigurosas especificaciones de calidad. Son productos que se emplean en la fabricación de preparados farmacéuticos, reactivos de laboratorio, aditivos de alimentación, etc.
-
Plantas químicas transformadoras o finales. Son las que a partir de los productos intermedios generan nuevos productos que podrán ser utilizados en otros sectores. Estos productos tienen las características deseadas para su uso final, pero todavía no poseen la presentación adecuada para su consumo. Tienen un gran valor añadido y están sometidos a una gran fluctuación en la demanda
-
Plantas químicas de consumo. Los productos de consumo son los finales, una vez envasados, con los aditivos correspondientes y la concentración adecuada para su empleo. Una misma industria puede actuar como transformadora y de consumo. Son las que a partir de los productos semielaborados provenientes de las industrias de base generan nuevos productos que saldrán al mercado o bien podrán ser utilizados en otros sectores.
También se pueden clasificar según el volumen de producción y en el grado de diferenciación del producto obtenido por una u otra empresa:
-
Productos de gran volumen de producción, no diferenciados según el fabricante.
-
Productos de gran volumen de producción, pero específicos de un fabricante concreto
-
Productos químicos finos, de pequeño volumen de producción no diferenciados.
-
Especialidades, de pequeño volumen de producción y específicos de una marca.
Sectores de la industria química
Se pueden distinguir cuatro grandes sectores:
-
Minería y metalurgia. Aparecen subsectores según el metal o mineral que traten. Los más destacables son el sector siderúrgico, el del aluminio y el del cobre
-
Química inorgánica. Incluye la producción de ácidos, bases, óxidos, gases nobles, sales de flúor, de cloro, de bromo, de yodo, de azufre, nitrógeno, fósforo y silicio, entre otras, así como la producción de agua oxigenada y haluros no metálicos.
-
Química orgánica. Incluye toda la química del carbono y sus derivados. Entre sus subsectores se incluye la química farmacéutica, perfumería y cosmética.
-
Química agrícola industrial. Se ocupa de aumentar el aprovechamiento de los productos agrícolas, especialmente los no alimentarios. Se persigue la máxima explotación de los recursos vegetales.
A parte de estos campos ya existentes, están apareciendo algunos nuevos dedicados a la obtención y explotación de nuevos materiales, a la química medioambiental, etc.
FABRICACIÓN Y OPERACIONES UNITARIAS
La fabricación puede resumirse en el abastecimiento de materias primas, operaciones físicas de acondicionamiento de las materias primas, las reacciones químicas, las operaciones físicas de separación de los productos y el acondicionamiento y envasado de los productos.
La actual definición de operación unitaria, dada por Little, es la de cada una de aquellas operaciones básicas en las que puede descomponerse cualquier proceso químico
Acondicionamiento de las materias primas y productos
Las más destacadas son:
-
Trituración y molienda. Reducen el tamaño de las partículas de sólidos.
-
Tamizado. Separa las partículas que llegan a él, deja pasar algunas a través de la malla y retiene otras.
-
Mezclado de sólidos y pastas. Puede realizarse mediante agitadores de paletas o agitadores de bombo.
-
Circulación de productos. Comprende la circulación de fluidos por conducciones, el paso a través de un lecho sólido y el movimiento de las partículas sólidas en el seno de un fluido. Para impulsar los gases se usan compresores, sopladores, ventiladores y eyectores. Para impulsar líquidos se usan bombas centrífugas, bombas volumétricas y tornillos de Arquímedes.
Reactores químicos
Son recipientes donde se llevan a cabo las reacciones químicas. Deben permitir la entrada de reactivos, la retirada de productos y la regulación de la presión y temperatura para que la reacción transcurra según la velocidad y el rendimiento deseados.
Pueden trabajar en régimen continuo, donde los reactivos son añadidos y los productos de la reacción retirados permanentemente, sin interrumpir la reacción, o régimen discontinuo, donde se trabaja en ciclos añadiendo los reactivos, realizando la reacción y deteniéndola para retirar los productos y añadir nuevos reactivos.
Los principales tipos de reactores son:
-
De tanque agitado, los cuales intentan conseguir el máximo grado de mezcla y permiten trabajar de forma continua o discontinua independientemente de la tasa de producción. Sobre todo se utilizan para reacciones homogéneas entre líquidos y gases.
-
Reactores tubulares. Son adecuados para reacciones en fase gaseosa. El reactor tubular calentado a fuego directo consiste en un tubo colocado dentro de un horno. El reactor tubular de carcasa y tubos es análogo a un intercambiador de calor de tubos. La reacción puede realizarse en el interior o en el exterior del tubo central, mientras que por el otro espacio circula el fluido refrigerante o calefactor.
-
Reactores de lecho fijo, móvil o fluido. En ellos los gases circulan a través de un lecho de partículas catalíticas que pueden estar fijas o no, de lo cual depende el tipo de reactor.
-
Hornos rotatorios. Se usan en la industria del cemento. Son una especie de reactores tubulares donde los sólidos entran y van avanzando a lo largo de ellos ayudados por una rotación axial y una ligera inclinación de los hornos.
-
Reactores de película descendente. En ellos una delgada capa de líquido resbala por la pared de un tubo, entrando en contacto con un gas que fluye a contracorriente. Al ser la capa de líquido tan delgada, se controla su temperatura con gran precisión. Se usan en la fabricación de determinados productos alimenticios y de detergentes.
-
Fermentadores. Se usan en las reacciones con microorganismos. Son tanques agitados con minucioso control de temperatura y presión.
-
Reactores fotoquímicos. Son similares a tanques agitados o a reactores tabulares, pero incorporan dispositivos luminosos para llevar a cabo reacciones activadas por energías de frecuencias determinadas.
-
Reactores electroquímicos. Obtienen los productos de la reacción sobre los electrodos, donde se lleva a cabo una reacción electrolítica gracias al suministro de corriente eléctrica continua.
Operaciones de separación de materia
Se pueden enumerar las siguientes:
-
Destilación. Separe los componentes de una mezcla aprovechando su diferente volatilidad. Hay varios tipos de destilación:
-
Destilación simple, que consiste en hervir la mezcla líquida condensando aparte los vapores que forman el destilado, mientras en la caldera queda el residuo.
-
Destilación a reflujo, parte del condensado se devuelve a la columna de destilación. Equivale a una redestilación y, por tanto, a una mejor separación.
-
Destilación por arrastre de vapor, se inyecta vapor de agua recalentado a la mezcla que se quiere destilar. Así se reduce la presión de vapor de la mezcla, las sustancias se evaporan más fácilmente y se separan a menor temperatura.
-
Absorción y desorción. La absorción consiste en poner en contacto una mezcla gaseosa con un líquido para que se disuelvan o queden retenidos ciertos componentes gaseosos y así se libere de ellos el gas resultante. La desorción es la operación inversa a la absorción y suele facilitarse mediante el arrastre o por otro gas inerte.
-
Extracción. Es una operación basada en la disolución selectiva de uno o varios componentes de una mezcla sólida o liquida. Se distinguen:
-
Extracción líquido-líquido
-
Extracción sólido líquido(lixiviación, lavado o percolación). Suele recuperarse el componente extraído.
-
Adsorción y desorción. Es la retención de algunos componentes de una mezcla líquida o gaseosa en la superficie de un sólido mediante enlaces químicos o sólo por fuerzas de Van der Waals. La desorción es la operación inversa. Se regenera el sólido para su reutilización y se recupera el componente adsorbido. El sólido adsorbente se dispone dentro de una columna por la que pasa el fluido que se ha de adsorber.
-
Intercambio iónico. Se basa en la facilidad de ciertas sustancias para intercambiar algunos iones que forman parte de su composición por iones de un líquido que circula a través. Según qué iones pueda intercambiar la resina, se conocerá como resina de intercambio catiónoco, o resina de intercambio aniónico.
-
Cristalización. Generalmente, en el seno de disoluciones líquidas sobresaturadas. En los cristalizadores-evaporadores la sobresaturación se consigue por evaporación; en los cristalizadores de tanque se produce la cristalización al enfriar; los cristalizadores de vacío se usan si el producto no resiste el aumento de temperatura.
-
Secado. Los secadores calientan el producto sin entrar en contacto con la fuente de calor o lo ponen en contacto con una corriente de aire caliente y seco. Los hay de bandejas, en los que se deposita el sólido en capas de poca profundidad; rotativos, donde el sólido desciende a lo largo de un cilindro rotativo inclinado y recibe la acción del aire caliente a contracorriente, y atomizadores, donde la suspensión se expulsa en forma de gotas, y el aire caliente evapora bruscamente el agua, resultando un sólido con gran porosidad.
-
Liofilización. El agua se elimina por sublimación. Se utiliza mucho en productos alimenticios, en algunos preparados termolábiles y, en general, en productos cuyas propiedades se alterarían mediante un secado a base de calor, ya que algunos componentes volátiles se perderían y otros se verían afectados.
-
Filtración. Para sólidos suspendidos en un líquido se usan filtros-prensa o de placas, rotatorios y centrífugos. Para sólidos suspendidos en un gas se utilizan filtros de mangas y electro filtros con electrodos cargados a varios miles de voltios.
-
Ósmosis inversa. Se separa el disolvente gracias a la aplicación de una presión superior y en sentido contrario a la presión osmótica.
-
Sedimentación. Por diferencia de densidad, las sustancias sólidas se depositan en el fondo.
-
Flotación. Es la separación de un líquido y partículas sólidas recubiertas de burbujas de aire.
-
Centrifugación. Un campo de fuerza superior a la gravedad actúa separando fases de densidades demasiado parecidas.
Almacenaje de materiales
-
Sólidos. Pueden almacenarse a la intemperie si no resultan alterados. Si los sólidos no resisten a la acción atmosférica, se almacenan en silos donde se descargan por transporte neumático o mediante medios mecánicos.
-
Líquidos. Se almacenan en tanques cilíndricos de poca altura. Cuando se trata de líquidos inflamables y volátiles, el techo es flotante y descansa directamente sobre el líquido. Así se reduce al máximo el cúmulo de vapor por encima del líquido y el riesgo de inflamabilidad.
-
Gases. Los gases fácilmente licuables se almacenan como líquidos, a temperatura ambiente y a presión, en tanques esféricos. Si son difíciles de licuar, es mejor almacenarlos a baja temperatura que a elevada presión.
INDUSTRIA QUIMICA, TECNOLOGÍA Y MEDIO AMBIENTE
La química industrial tiene un papel muy importante en el incremento de la calidad de vida de la sociedad, pero esta indudable mejora en la calidad de vida tiene un alto precio: la generación de grandes cantidades de residuos que provocan un grave perjuicio al medio ambiente.
Son cuantiosos los estropicios derivados de la gran actividad industrial que se está llevando a cabo en el mundo desarrollado hoy en día, y la presencia de ciertos elementos o productos en grandes cantidades trastorna el equilibrio normal de los ecosistemas y repercute muy negativamente en el medio ambiente. Pero también ha proporcionado alternativas para evitar el uso de sustancias perjudiciales.
Emisiones a la atmósfera
La contaminación de la atmósfera por residuos o productos secundarios gaseosos, sólidos o líquidos, pueden poner en peligro la salud del hombre y la salud y bienestar de las plantas y animales, atacar a distintos materiales, reducir la visibilidad o producir olores desagradables. Entre los contaminantes atmosféricos emitidos por fuentes naturales, sólo el radón, un gas radiactivo, es considerado un riesgo importante para la salud.
La lluvia ácida
Las lluvias ácidas constituyen actualmente una preocupación mundial porque corroen los metales destruyen el equilibrio de la Naturaleza y son muy peligrosas para la salud humana. En gran parte son causadas por el azufre de los carburantes, dado que el azufre está presente en los combustibles fósiles ( petróleo, y sobre todo carbón). Al quemarse este se desprende dióxido de azufre SO2, que se mezcla con la lluvia y forma ácido sulfuroso. Si bien su acidez es muy débil la lluvia ácida pone en peligro el equilibrio ecológico de la superficie terrestre. En otros subproductos de la combustión se encuentra el anhídrido sulfuroso, que además puede oxidarse en el aire para dar anhídrido sulfúrico (otro compuesto gaseoso formado por la combinación con el oxígeno). Este último, al humedecerse con la humedad atmosférica da lugar a la formación de ácido sulfúrico que puede ser vertido a la tierra a través de la lluvia.
El ácido nítrico formado en la atmósfera a partir de óxidos de nitrógeno generados en las tormentas y desprendidas por muchas fábricas de productos químicos contribuyen también a la lluvia ácida.
El uso industrial del amoniaco en equipos de refrigeración y aire acondicionado provoca, en este caso, la neutralización de la lluvia ácida al ser éste una base. podemos
El fenómeno de las lluvias ácidas ( que en algunos casos pueden alcanzar la acidez del vinagre) afecta a parte del norte de Europa y a Estados Unidos y representa una tremenda amenaza ambiental, en particular para los lagos y explotaciones agrícolas. Incluso los monumentos de piedra sufren importantes degradaciones por esta causa tanto mayor cuanto más próximo se encuentren a las zonas industriales. Son los países industrializados los que en mayor medida.
El “smog”
El "smog" (niebla fotoquímica) es un término de la contaminación del aire que se usa diariamente. En realidad, el smog es ozono a nivel del suelo formado por la reacción de los contaminantes con la luz solar. La siguiente figura muestra los factores que intervienen en la creación del smog.
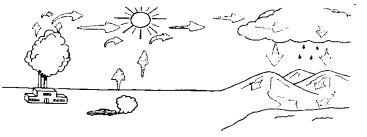
El agente más influyente para la aparición del smog es la actuación en la atmósfera del óxido nítrico (NO) y del dióxido de nitrógeno (NO2).
El efecto invernadero
La atmósfera es prácticamente transparente a la radiación solar de onda corta, absorbida por la superficie de la Tierra. Gran parte de esta radiación se vuelve a emitir hacia el espacio exterior con una longitud de onda correspondiente a los rayos infrarrojos, pero es reflejada de vuelta por gases como el dióxido de carbono, el metano, el óxido nitroso, los halocarbonos y el ozono, presentes en la atmósfera. Este efecto de calentamiento es la base de las teorías relacionadas con el calentamiento global.
El contenido en dióxido de carbono de la atmósfera ha venido aumentando un 0,4% cada año como consecuencia del uso de combustibles fósiles como el petróleo, el gas y el carbón; la destrucción de bosques tropicales por el método de cortar y quemar también ha sido un factor relevante que ha influido en el ciclo del carbono. La concentración de otros gases que contribuyen al efecto invernadero, como el metano y los clorofluorocarbonos, está aumentando todavía más rápido. El efecto neto de estos incrementos podría ser un aumento global de la temperatura, estimado en 2 a 6 °C en los próximos 100 años. Un calentamiento de esta magnitud alteraría el clima en todo el mundo, afectaría a las cosechas y haría que el nivel del mar subiera significativamente. De ocurrir esto, millones de personas se verían afectadas por las inundaciones.
Según un estudio reciente, publicado por la revista Nature, la primavera es más larga debido en parte al efecto invernadero. Este estudio afirma que desde principios de 1980 la primavera se adelanta y la vegetación crece con mayor vigor en las latitudes septentrionales; esto se debe al calentamiento global que ha afectado a una gran parte de Alaska, Canadá y el norte de Asia y Europa, que a su vez está relacionado con el efecto invernadero de origen humano (teoría según la cual la población humana ha contribuido a la concentración de gases, tales como el dióxido de carbono, en la atmósfera). Mediante el uso de imágenes obtenidas a través de satélites climáticos, los científicos proporcionan pruebas del cambio climático y aportan datos significativos para el estudio del calentamiento global del planeta.
Derivados halogenados
-
Los productos orgánicos halogenados tienen propiedades particulares que los hacen muy deseables para algunas aplicaciones. Cuando se liberan a la atmósfera, donde persisten, dando lugar a reacciones perjudiciales para el equilibrio atmosférico.
-
Los clorofluorocarbonatos se han usado como propelentes y gases de circuitos de refrigeración. En la estratosfera, la radiación ultravioleta libera radicales que reaccionan con el ozono destruyéndolo.
-
Las dioxinas se generan en la combustión de plásticos como el PVC. Su toxicidad y su carácter cancerígeno han levantado voces para la prohibición de los PVC.
-
El triclorometano, el clorotileno o el tricloruro de metilo se usan para desengrasar metales; el tetracloroetileno(CCL2=CCL2)para el lavado en seco; el p-diclorobenceno como repelente de insectos y en desodorantes; los bifenlios pliriclorados como herbicidas e insecticidas, etc. La mayoría de estos compuestos acaban escapando a la atmósfera, donde protagonizan reacciones radicalarias.
Contaminación por humos y partículas
Los humos producidos por las industrias contienen partículas sólidas en suspensión que pueden servir de núcleos de agregación para el agua y producir nieblas más persistentes que las naturales. Además reducen la visibilidad y la penetración de la radiación ultravioleta del Sol. Si se llegase a almacenar en la estratosfera una concentración suficiente de partículas de dimensiones mayores que un micrómetro, se podría alterar la transferencia del calor radiado del Sol a la Tierra y, como consecuencia una alteración climática.
Medidas de protección
Para reducir las emisiones de SO2 se trabaja con carbón lavado, es decir, carbón del que se ha eliminado el azufre que contenía.
Descargar
| Enviado por: | El remitente no desea revelar su nombre |
| Idioma: | castellano |
| País: | España |
