Industria y Materiales
Polímeros
POLÍMEROS
1. DEFINICIÓN.
Los polímeros son compuestos químicos cuyas moléculas están formadas por la unión de otras moléculas más pequeñas llamadas monómeros, las cuales se enlazan entre sí como si fueran los eslabones de una cadena. Estas cadenas, que en ocasiones presentan también ramificaciones o entrecruzamientos, pueden llegar a alcanzar un gran tamaño, razón por la cual son también conocidas con el nombre de macromoléculas. Habitualmente los polímeros reciben, de forma incorrecta, el nombre de plásticos, que en realidad corresponde tan sólo a un tipo específico de polímeros, concretamente los que presentan propiedades plásticas (blandos, deformables y maleables con el calor).
Dependiendo de su origen, los polímeros pueden clasificarse en naturales y artificiales. Entre los naturales se hallan sustancias muy comunes de las que suele ignorarse su naturaleza polimérica: Los hidratos de carbono o polisacáridos, como el almidón o la celulosa; la lana, la seda y otras proteínas, constituidas por aminoácidos; los ácidos nucleicos (el ADN y el ARN), responsables de la información genética, cuyos monómeros constituyentes son un azúcar (ribosa o desoxirribosa), ácido fosfórico y las bases nitrogenadas que constituyen las letras del código genético, y otras sustancias tales como el caucho, derivadas de pequeñas moléculas de hidrocarburos.
Con el desarrollo de la tecnología y la industria química el hombre ha aprendido a imitar a la naturaleza, e incluso a mejorarla, sintetizando nuevos polímeros artificiales inexistentes en ella, normalmente a partir de derivados del petróleo. El primero en ser creado de forma totalmente artificial fue, en 1909, la baquelita, aunque con anterioridad se habían obtenido algunos, como el celuloide, mediante la modificación de polímeros naturales, celulosa en este caso. En la actualidad la síntesis y el procesado de materiales poliméricos es una de las más importantes ramas de la industria química, y los polímeros están presentes de forma habitual en nuestra vida cotidiana. Sin pretender ser, ni mucho menos, exhaustivos podemos recordar algunos polímeros tan usuales y frecuentes como el polietileno y el polipropileno, utilizados para la elaboración de bolsas de plástico; el poliestireno, o corcho blanco, para embalajes; el PVC, o policloruro de vinilo, para envases y tuberías; el PET (polietilentereftalato), también para envases; el teflón, como aislante; las poliamidas (nailon) y los poliésteres (tergal), como fibras sintéticas; el metacrilato, como sustitutivo del vidrio; el caucho sintético, para neumáticos... También existen polímeros artificiales de naturaleza inorgánica, como las siliconas, donde el carbono ha sido sustituido por átomos de silicio encadenados con átomos de oxígeno.
Como es fácil apreciar, la vida actual no sería imaginable sin los materiales poliméricos, tal es su implantación en nuestra sociedad. A las aplicaciones beneficiosas de los polímeros sintéticos hay que añadir el grave problema que crea su resistencia a la degradación una vez usados, lo que dificulta su eliminación e incluso su reciclado. Aunque actualmente se está intentando sustituir los polímeros más perniciosos, como el PVC y en general los que contienen flúor y cloro, por otros más inocuos, y se ha comenzado a implantar polímeros biodegradables, todavía hoy un porcentaje muy importante de nuestras basuras está constituido por polímeros de difícil eliminación.
2. HISTORIA.
La noción de molécula es intuitiva, es una consecuencia de la concepción discontinua de la materia y corresponde a la idea de una especie química definida que no puede fragmentarse más allá de cierto límite sin perder sus características propias.
Este concepto se ha caracterizado por diversos métodos analíticos, ya sea por vía húmeda o a través de técnicas instrumentales como, por ejemplo los rayos X, para definir estructuras cristalinas.
Hasta mediados del siglo pasado, existía un buen número de moléculas conocidas de dimensiones finitas y de un número de átomos limitado, en I mayoría de los casos, como el H2O, NH3, CH4, también se encontraban en los estudios de química orgánica, compuestos más elaborados como la sacarosa C12H22O11, el caroteno C40H56 o la triestearina C57H110O6. Sin embargo, el número de átomos de estas substancias no pasaba de una o dos centenas. Por otra parte, se sabia que algunas substancias de origen natural, como la celulosa, el almidón y el hule, que a pesar de corresponder a composiciones moleculares muy simples, sus propiedades físico-químicas eran diferentes de aquellas que tenían fórmulas similares p idénticas, como por ejemplo el hule y la celulosa, cuyas fórmulas obtenidas por análisis elemental son respectivamente C5H8 y C6H10O5, Para explicar estas anomalías se les atribuirla, a la celulosa y al hule, una estructura micelar, es decir, las pequeñas moléculas de C5H8 o C6H10O5 se encontraban, según esta teoría, agrupadas en partículas mucho más voluminosas e indisociables por medio de fuerzas de asociación intensas, pero indeterminadas, lo que era difícil de explicar, ya que éstas debían de ser de la misma magnitud que la de uniones ordinarias entre átomos para que aún en solución mantuvieran sus propiedades de cohesión.
Se sabe que, por ejemplo, las moléculas de jabón al variar la dilución, se cambian las características de éstas, fenómeno que no sucede en el caso de la celulosa.
Ya en 1900, Weber suponía que el hule natural era una verdadera macromolécula, sin embargo, no contó con el apoyo de los investigadores de la época; fue solamente hasta 1922 con lo trabajos de Herman Staudinger que se empezó a debatir seriamente sobre la estructura de estos compuestos. Se requirieron alrededor de 10 años más para lograr convencer total mente sobre la nueva teoría, y a partir de 1933, aproximadamente, se empezó a desarrollar la teoría macromolecular de tal forma que aunque en 1891 se produjo por primera vez el rayón en Francia, y en 1919 se inició la producción de baquelita a partir de resinas fenólicas, fue a partir de los años 30 cuando se produjo un desarrollo explosivo de la industria de los polímeros precedida de una intensa investigación, y así, en 1931 se produce el hule sintético (neopreno), en 1933 se descubre el polietileno (lCl) Inglaterra. En 1935 Carothers descubre el nylon, en 1936 Rohm and Haas comercializa el polimetilmetacrilato, en 1937 sale al mercado el poliestireno, etc. Posteriormente, se desarrollan los catalizadores Ziegler Natta, se estudia la estructura del ácido desoxirribonucleico, en fin, seria difícil enumerar todos los adelantos logrados a la fecha en el estudio de los polímeros, solo se mencionará que su campo de acción es muy amplio ya que abarca los polímeros naturales (los cuales existen en todo ser vivo), como lo son la celulosa el hule, el algodón de origen vegetal y proteínas, seda, ana, ácidos nucleicos provenientes de los seres animales.
En lo referente a polímeros sintéticos se tiene una gran variedad, se obtienen por medio de síntesis de pequeñas moléculas las cuales, la mayoría de ellas, son derivados del petróleo.
Así pues, una vez que se establecieron las bases de la química macro molecular con Staudinger, al comprobarse que estos productos se podrían obtener por síntesis y que había la posibilidad de fabricarlos a diferentes grados de polimerización y, por tanto, pesos moleculares variables, se trató de fijar un criterio para definir el umbral inferior a partir del cual un polímero se puede considerar como tal. Se observó que la temperatura de fusión de las olefinas aumentaba a medida que la longitud de la cadena del hidrocarburo lo hacia.
3. CLASIFICACIÓN.
3. 1. Obtención.
Se pueden clasificar por el medio en el que se obtuvo el polímero y su naturaleza.
-
Naturales: son los que la naturaleza ha creado. Ej. algodón, seda, nosotros, seres vivos. También se conocen como biopolímeros.
-
Artificiales: son los que el hombre produce por medio de reacciones químicas.
3. 2. Tipo de enlace.
Otro tipo de clasificación (aunque no tan utilizada) es la que se realiza con el tipo de enlace con que esta formado.
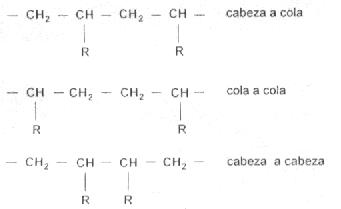
4. POLIMERIZACIÓN.
El objeto de la polimerización es obtener una sustancia macromolecular con propiedades diferentes a las del monómero, o moléculas aisladas de peso molecular conocido.
Durante la polimerización la cual tiene lugar bajo condiciones variadas como temperatura o presión elevada, acción de la luz, o presencia de aceleradores, las moléculas aisladas o monómeros se ensamblan bajo reacción exotérmica, dando macromoléculas. La capacidad de los compuestos orgánicos de polimerizarse depende de ciertas condiciones de enlazamiento de los átomos de la molécula monómera. Particularmente hacen posible la polimerización los enlaces múltiples, bien dobles enlaces de carbono (átomos de carbono unidos a través de dos valencias) o bien enlaces triples, así como el tipo y posición de átomos o grupos atómicos eficaces.
Fundamentalmente todos los polímeros se forman mediante la creación de enlaces químicos entre moléculas relativa mente pequeñas, o monómeros, para formar moléculas muy grandes (macromoléculas), o polímeros. Los enlaces se forman por medio de un o de una combinación de dos tipos de reacciones: de adición o de condensación.
4. 1. Polimerización por adición.
El proceso de polimerización por adición se caracteriza por la simple combinación de moléculas sin que se generen productos secundarios como resultado de la combinación. Las moléculas originales no se descomponen para producir residuos de reacción que es necesario eliminar del producto. Cuando se enganchan unidades de un solo monómero, el producto resultante es un homopolímero, como el etileno, por ejemplo, que se prepara a partir del monómero etileno. Cuando se utilizan dos o más monómeros en el proceso, como etileno y propileno, por ejemplo, el producto es un copolímero.
La formación de un homopolímero es análoga al enlazamiento de vagones idénticos de un tren. Cada uno de los vagones es análogo a una pequeña molécula llamada mero, que se enlaza a otros meros idénticos para formar una cadena de muchos meros llamada polímero. Al igual que los vagones, el mero debe contar con un medio para engancharse o enlazarse con otros meros por ambos extremos (es decir, debe ser al menos bifuncional).
El proceso mismo de polimerización implica la formación, no de un solo tren (una macromolécula), sino muchos; cada una de las macromoléculas compite por los meros (vagones de la estación de ferrocarril).
Por tanto al término del proceso de polimerización, el producto consiste en muchas macromoléculas de diferente longitud, compuestas de la misma clase de mero.
El proceso de polimerización por adición se lleva a cabo por uno de tres caminos. La primera reacción de adición implica la activación química externa de las moléculas, que las induce a combinarse por una reacción en cadena, como se ilustra con la polimerización del etileno. La reacción inicial de este proceso comprende la ruptura del doble enlace del etileno, seguida de la reacción de propagación y de la reacción de terminación. Los átomos se enlazan directamente dentro de la molécula que reacciona. La segunda forma como se produce una polimerización por adición es mediante una transposición de los átomos dentro de ambas moléculas reaccionantes, como se muestra para el caso de la formación de poliuretano. Un tercer camino para que ocurra una polimerización por adición es por apertura de anillo, en la que una molécula, compuesta de un anillo de átomos, se abre y se enlaza a otras moléculas anulares que también se abren por influjo de activadores catalíticos. En los tres métodos de polimerización por adición se conserva la característica propia de una reacción de polimerización por adición: que no hay productos secundarios ni pérdida de átomos de las moléculas reaccionantes.
En la polimerización de adición se distinguen tres etapas: iniciación, propagación y terminación. Durante la etapa de terminación se forma por reacción de catalizador con una unidad monomérica, un centro activo capaz de propagarse.
Ejemplo. Este proceso se demostró para el polietileno es la repetición de la siguiente reacción:
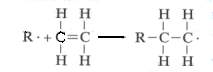
donde R• representa un iniciador activo y es un electrón desapareado.
La propagación representa el crecimiento lineal de la molécula al unirse entre sí las unidades monoméricas para producir la cadena molecular de polietileno:
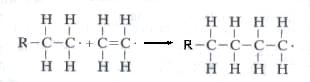
El crecimiento de la cadena es relativamente rápido. El tiempo necesario para el crecimiento de una molécula de, por ejemplo, 1000 unidades monoméricas es del orden de 10^-2 a 10^-3s.
La propagación puede terminar por varios caminos. En primer lugar, los extremos activos de dos cadenas que se propagan pueden reaccionar formando una molécula no reactiva:
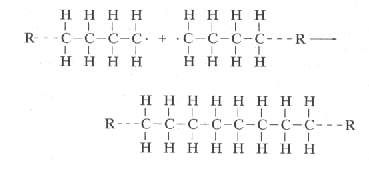
De este modo termina el crecimiento de las dos cadenas. En segundo lugar, el extremo activo de una cadena puede reaccionar con un iniciador u otra especie química que tiene un enlace activo simple:
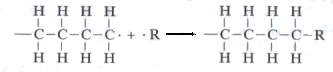
y como resultado cesa el crecimiento de la cadena.
Las velocidades relativas de iniciación, propagación y terminación determinan el peso molecular, por lo que normalmente se controlan para obtener un polímero con grado de polimerización predeterminado. Como la polimerización termina al azar, se genera una gran cantidad de variedad de longitudes de cadena, que origina una distribución de pesos moleculares.
4. 2. Polimerización por condensación.
En este proceso, la unión química de dos moléculas sólo se consigue mediante la formación de una molécula secundaria (usualmente pequeña) con átomos de las dos moléculas para crear la unión (de las moléculas), con lo cual la polimerización puede continuar. En estas reacciones el producto secundario residual se extrae inmediatamente del polímero porque puede inhibir la polimerización subsiguiente o permanecer como impureza indeseable en los productos terminados.
Un proceso de este tipo es por ejemplo el que tiene lugar en la fabricación de resinas sintéticas de fenol - formaldehído o baquelitas. En él dos clases diferentes de moléculas con los grupos activos cresol y formaldehído, forman, bajo presión y calentamiento (y si es preciso, en presencia de aceleradores de la reacción) macromoléculas entrecruzadas, separándose agua.
La polimerización por condensación (o reacción por etapas) es la formación de polímeros por mediación de reacciones químicas intermoleculares que normalmente implican más de una especie monomérica y generalmente se origina un subproducto de bajo peso molecular, como el agua, que se elimina. Las substancias reactivas tienen fórmulas químicas diferentes de la unidad que se repite, y la reacción intermolecular ocurre cada vez que se forma una unidad repetitiva. Por ejemplo, al considerar la formación de un poliéster a partir de la reacción entre el etilenglicol y el ácido adípico, la reacción intermolecular es la siguiente:
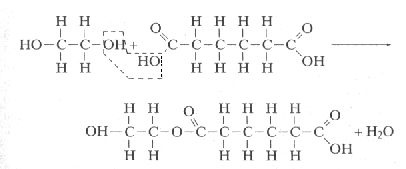
Este proceso por etapas se repite sucesivamente y se produce, en este caso, una molécula lineal. La química de la reacción específica no es importante, sino el mecanismo de la polimerización por adición.
Los tiempos de reacción para la polimerización por condensación son generalmente mayores que los de la polimerización por adición. Para generar materiales con elevados pesos moleculares se necesitan tiempos de reacción suficientemente largos para completar la conversión de los monómeros reactivos. También se producen varias longitudes de cadena y se genera una distribución de pesos moleculares.
Las reacciones de condensación forman a menudo monómeros trifuncionales capaces de generar polímeros entrecruzados y reticulados.
5. ESTRUCTURA MOLECULAR.
Las técnicas modernas de síntesis de polímeros permiten un gran control sobre varias posibilidades estructurales. Este es un factor del cual depende la característica de un polímero.
5. 1. Polímeros Lineales.
En un polímero lineal las unidades monoméricas se unen unas a otras formando cadenas sencillas. Estas largas cadenas son flexibles y se comportan como una masa de fideos, esquematizada en la figura, donde cada círculo representa una unidad monomérica. Las cadenas de los polímeros lineales pueden unirse entre sí por fuerzas de van der Waals. Polietileno, cloruro de polivinilo, poliestireno, poli (metacrilato de metilo), nilón y fluorocarbonos son algunos polímeros de estructura lineal.
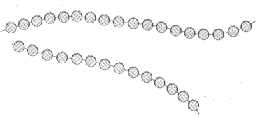
5. 2. Polímeros ramificados.
Se sintetizan polímeros cuya cadena principal está conectada lateralmente con otras cadenas secundarias, como está esquematizado en la figura. Son los llamados polímeros ramificados. Las ramas, que forman parte de la cadena molecular principal, son el resultado de las reacciones locales que ocurren durante la síntesis del polímero. La eficacia del empaquetamiento de la cadena se reduce con las ramificaciones y, por tanto, también disminuye la densidad del polímero.
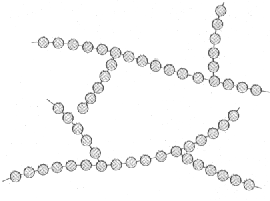
5. 3. Polímeros entrecruzados.
En los polímeros entrecruzados, cadenas lineales adyacentes se unen transversalmente en varias posiciones mediante enlaces covalentes, como está re presentado en la figura. El entrecruzamiento se realiza durante la síntesis o por reacciones químicas irreversibles que normalmente ocurren a elevada temperatura. A menudo el entrecruzamiento va acompañado por la adición mediante enlace covalente de átomos o moléculas a las cadenas. Muchos de los materiales elásticos de caucho están entrecruzados.
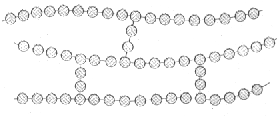
5. 4. Polímeros reticulados.
Las unidades monoméricas trifuncionales, que tienen tres enlaces covalentes activos, forman redes tridimensionales (figura) en lugar de las cadenas lineales generadas por las unidades monoméricas bifuncionales. Los polímeros compuestos por unidades trifuncionales se denominan polímeros reticulados. Un polímero entrecruzado, prácticamente, se puede clasificar como polímero reticulado. Estos materiales tienen propiedades mecánicas y térmicas específicas. Los polímeros epoxy y los fenol-formaldehído pertenecen a este grupo.
Conviene recordar que algunos polímeros no pertenecen a un solo grupo. Por ejemplo, un polímero predominantemente lineal puede tener algún número limitado de ramas y de entrecruzamiento o de reticulación bidimensional.
6. MÉTODOS INDUSTRIALES DE POLIMERIZACIÓN.
Hay muchos procesos diferentes donde se producen los materiales plásticos industrialmente. Se utilizan como materiales de partida gas natural, petróleo y carbono para producir los productos químicos básicos para los procesos de polimerización. Estos productos químicos son entonces polimerizados mediante muchos procesos diferentes obteniéndose materiales plásticos en forma de gránulos, bolitas, polvos, o líquidos que son posteriormente procesados en productos acabados.
Técnicamente las reacciones de polimerización pueden efectuarse de diferentes maneras según la naturaleza del monómero y la utilización que se vaya a hacer del polímero.
6. 1. Polimerización en masa.
El monómero líquido se polimeriza por la reacción del calor en presencia de un iniciador conveniente, pero en ausencia de disolvente. El medio reaccionante se hace cada vez más viscoso y puede solidificarse. Si partir de cierto grado de polimerización el polímero es insoluble en el monómero, se precipita.
Este procedimiento proporciona polímeros muy puros, pero bastante polidispersos, ya que la masa al hacerse más viscosa dificulta la agitación y el calentamiento uniforme. Además, las reacciones de polimerización, al ser exotérmicas, producen aceleraciones que a veces toman carácter explosivo.
Sin embargo, el método se emplea para obtener directamente el polímero con la forma de un molde. Con los monómeros de bajo punto de ebullición, la polimerización en masa se realiza en algunos casos, bajo presión, cómo en el caso del etileno que se lleva por encima de su temperatura crítica y es de hecho una polimerización en masa.
6. 2. Polimerización en solución.
Permite realizar una reacción más regular. El polímero puede ser soluble en el disolvente o precipitar a partir de cierto grado de polimerización. En este último caso, la polimerización de la solución da polímeros con buena homogeneidad desde el punto de vista de los grados de polimerización. Este método exige sin embargo, una cantidad de disolvente bastante importan te, para limitar la viscosidad del medio. El disolvente debe ser eliminado enseguida del polímero y recuperado cuidadosamente para evitar un alto costo de fabricación. Este método tiene la ventaja de que se limita la temperatura de reacción con el punto de ebullición bajo, se obtienen polímeros de pesos moleculares muy elevados en el caso de polimerizaciones muy exotérmicas. Este tipo de polimerización se emplea sobre todo cuando el polímero final va a aplicarse en forma disuelta, como en el caso de adhesivos o barnices.
6. 3. Polimerización en emulsión.
Presenta la gran ventaja de sustituir por agua los disolventes costosos utilizados como medio de dispersión. Los monómeros al ser generalmente insolubles en agua o muy poco solubles, se emulsionan con agentes emulsificantes, y eventualmente en presencia de coloides protectores, reguladores de pH y de un iniciador soluble en el medio acuoso.
La iniciación de la polimerización está localizada en el medio acuoso y no en el interior o en la superficie de las gotitas del monómero. El crecimiento de las cadenas tiene lugar, muy probablemente, en el interior de las gotitas monómero-polímero. Incluso las reacciones de terminación se efectúan en ellas. Este será cedido al medio acuoso o a las gotas polímero-monómero a medida que el monómero se polimeriza. Efectivamente existe una disminución regular del volumen de las gotas del monómero, mientras que aumenta el volumen de las del polímero.
El resultado de la polimerización es un látex, emulsión acuosa del polímero, que se puede emplear directamente para ciertas aplicaciones. Es posible, igualmente, evaporar este látex y obtener el polímero sólido, eventualmente en forma pulverulenta. La polimerización en emulsión ha tenido un gran desarrollo técnico, sobre todo para la preparación de ciertos elastómeros (copolimeros butadieno - estireno). Sin embargo, tiene el in conveniente de dar polímeros difíciles de separar de las impurezas, correspondientes a los productos que facilitan la emulsión, que se añaden inicialmente en cantidades bastante importantes en el medio reaccionante, y que forman capas absorbidas de los granos de gran superficie especifica.
6. 4. Polimerización en suspensión.
El monómero se dispersa en un medio acuoso, en gotitas relativamente gruesas (orden del milímetro), utilizándose como únicos agentes accesorios, un estabilizador, que impide la coalescencia de las gotitas y un agente tenso activo que regula su tamaño Al contrario de la polimerización en emulsión, el iniciador debe ser soluble en las gotas del monómero. Se utilizan principalmente peróxidos orgánicos y la polimerización no facilita la eliminación del calor desprendido. En el curso de la polimerización, la dimensión de las gotitas iniciales del monómero no cambia. La viscosidad de las gotas crece hasta que se hacen sólidas, más o menos elásticas, El polímero se presenta finalmente en forma de perlas fáciles de lavar y que retiene pocas impurezas debido a su pequeña superficie específica, es necesario sin embargo eliminar perfectamente el agente tensoactivo por medio de un electrolito fuerte.
7. COPOLIMEROS.
Por copolimerización se entiende la polimerización conjunta de dos o varios monómeros, por lo que la macromolécula del copolímero obtenido con tiene como unidades estructurales los monómeros participantes.
La copolimerización entre dos monómeros ha sido objeto de muchos estudios, mientras que las mezclas de tres o más compuestos polimerizables, provocan grandes dificultades debido al número de variables, sin embargo, se producen técnicamente también terpolimeros (a partir de tres monómeros). El caso más general es el de dos monómeros.
Aunque los monómeros de la mayoría de los copolímeros están aleatoriamente dispuestos se han identificado cuatro tipos distintos de copolímeros: aleatorios, alternados, por bloques y por injerto.
7. 1. Copolímeros aleatorios.
Los diferentes monómeros están aleatoriamente dispuestos dentro de las cadenas poliméricas. Si Ay B son diferentes monómeros.

7. 2.Copolímeros alternados.
Los diferentes monómeros muestran una alternancia ordenada definida.

7. 3. Copolímeros en bloques.
Los diferentes en la cadena están dispuestos en bloques relativamente largos de cada monómero.

7. 4. Copolímeros injertados.
Se injertan apéndices de un tipo de monómero a la cadena larga de otro monómero.

7. 5. Clasificación de los diferentes tipos de copolímeros.
Las macromoléculas formadas al principio de la copolimerización son más ricas en uno de los componentes, por lo que en la mezcla de los monómeros disminuye éste. Las macromoléculas formadas al final de la reacción contienen menos del monómero reactivo. Según los valores de r1 y r2, las curvas que representan la variación, de la composición del copolímero en función de la composición de la mezcla de los monómeros tienen formas variadas.
Los valores de r1 y r2 dependen del modo de iniciación; pueden modificarse cuando se para de una copolimerización radical a una iónica, e incluso en este último caso, son diferentes cuando se trata de una iniciación catiónica o aniónica.
Tipos:
I. Copolimerización radial a 60 °C
II. Copolimerización catiónica a 25 °C
III. Copolimerización aniónica a -50 °C
7. 6. Aplicación de los copolímeros.
En los primero años del desarrolló de los polímeros se intento mezclar dos copolímeros con objeto de mejorar algunas propiedades, pero se encontró con la dificultad de la poca miscibilidad entre los copolímeros de ahí la necesidad de partir de dos o más monómeros que al polimerizar juntos las propiedades cambian sin que haya separación de éstos.
La importancia industrial de los copolímeros es muy grande ya que un copolímero puede modificarse en sus características para conseguir mayor flexibilidad, pegajosidad, adherencia, aumentar su temperatura de transición vítrea, disminuir su costo, etc., siempre y cuando se logre una buena selección del comonómero.
No se puede en todos los casos copolimerizar dos o mas monómeros ya que sus reactividades pueden ser muy diferentes, para su selección deberá tenerse en cuenta los valores los radios, que en la mayoría de los casos se encuentran ya publicados.
Algunos ejemplos de copolímeros industriales se mencionan a continuación:
Etilen-vinil acetato (EVA), Estireno-Butadieno (SBR), Estireno-Acrilonitrílo (SAN), Acrilonitrilo-Butadieno-Estireno (ABS), Acetato de vinilo con diferentes esteres acrílicos.
8. CARACTERIZACIÓN QUÍMICA DE POLÍMEROS.
Normalmente resulta complejo llegar a la identificación total de un material plástico, de manera que existe un buen número de interrogantes que es necesario aclarar.
¿Se trata de un material termoplástico o de un material entrecruzado?, ¿cuál es la naturaleza de este material?, ¿está plastificado, estabilizado al calor, a los rayos UV? Si es el caso ¿cuáles son los estabilizantes?, ¿hay cargas inertes?, eventualmente es posible determinar el tipo de polimerización que permitió obtener este producto.
Son algunas de las preguntas que el profesional de la química deber ser capaz de responder por tener amplios conocimientos teóricos y prácticos en los análisis realizados a productos de la competencia, o contratipos, en cinéticas de reacción de los diferentes procesos de fabricación, en la definición de parámetros de reacción, etc.
Por otro lado, existen diversos métodos de identificación y caracterización de los polímeros como: análisis físicos, fisicoquímicos y el análisis estructural. Entre los ensayos más comunes se encuentran las pruebas de grupos funcionales, térmicas, mecánicas y estructurales.
8. 1. Pruebas preliminares.
Para iniciar se necesita tomar en cuenta que en la mayoría de los casos e1 material por analizar es un material complejo, debido a que pueden intervenir en su formulación de aditivos, estabilizantes, plastificantes, etc. Por esto resulta necesario primeramente separarlo por disolución y precipitación en un disolvente adecuado.
En este sentido es importante realizar diversas pruebas para caracterizar al polímero problema.
a) Ensayos iniciales
Las observaciones iniciales son sumamente importantes, debido a que pueden orientar la investigación posterior, algunas pruebas que se practican son:
— Producto transparente: polímero acrílico o estirénico
— Sonoridad metálica al impacto: polímero de estireno
— Se raya fácilmente con al uña: polietileno, etc.
El valor que puedan representar todas las observaciones depende esencialmente del ingenio, conocimiento y práctica del investigador para interpretar los resultados.
b) Prueba de combustión
Se coloca una pequeña porción de la muestra sobre una espátula y se calienta a la flama en un mechero de Bunsen, las observaciones que se deben hacer son las siguientes:
- El producto no arde y se quema sin deformación: En general se trata de un polímero entrecruzado producto de poli condensación del tipo fenolformaldehido, ureaformaldehido, melaminaformaldehido, etc.
- El producto arde en la flama y se apaga fuera de ella: En general son productos dorados o fluorados. o bien pueden ser materiales auto extinguibles como PVC o PVDC.
- Arde en la flama y fuera de ella: En ese caso se observa el color de la flama, si es azul, pueden ser poliamidas o poliacrilatos. Si la flama es amarilla se trata de celulosa, pero si la flama es intensa y muy luminosa es polestireno.
Por otro lado, la presencia de un depósito blanco en las cenizas, puede deberse a un polímero de silicón (hollín blanco, 513).
La presencia de olor a aceite quemado se debe a polietileno.
c) Prueba de calentamiento
Una pequeña muestra (0.5 g) del producto se coloca en un tubo de ensaye y se calienta lentamente, el olor desprendido puede definir al producto:
Olor a fenol y formaldehido: polifenolformaldeflido.
Olor a formaldehido y pescado: poliureaformaldehido
OIor acre. Al adicionar AgN se observa precipitado de AgCI.: PVC y derivados
Olor a ácido acético: acetado de polivinilo.
Olor característico de cada monómero: poliestireno y polimetacrilato de metilo, etc.
8. 2. Pruebas en productos puros.
Al purificar el polímero por sucesivas disoluciones y precipitaciones se puede esperar obtener un producto puro, después de eliminar los diferentes aditivos. En este caso se realizan análisis mucho más precisos.
a) Puntos de fusión y reblandecimiento.
Tanto el valor de la temperatura de fusión y de reblandecimiento como la manera en que el fenómeno ocurre puede ser una indicación interesante.
Así los productos muy cristalinos como las poliamidas tiene una fusión muy franca.
Se puede encontrar en la literatura tablas que clasifican a los polímeros por orden de puntos dé fusión o de reblandecimiento crecientes.
b) Medida de densidad.
Los métodos de determinación de densidad son muy variados en el caso particular de los polímeros se debe cuidar que la superficie de la muestra no contenga pequeñas burbujas de aire y tomar encuenta que numerosos polímeros pueden contener oclusiones gaseosas. modificando la medición e incurriendo en errores.
c) Índice de refracción
La medida del índice, de refracción de la muestra puede dar una indicación complementaria útil, comúnmente como medida de especificación. Es importante hacer notar que la temperatura de la muestra ene1 refractómetro debe ser constante. En la literatura sobre polímeros se pueden encontrar valores del índice de refracción de productos puros.
d) Análisis cualitativo
Se realiza la detección de azufre, nitrógeno y halógenos el método de Lassaigne En un tuvo de ensayo se calienta al rojo una pequeña porción de polímero con sodio metálico, después se enfría y se agrega lentamente exceso de etanol. En seguida el tubo se vuelve a calentar y se sumerge en agua destilada. El tubo se rompe y la solución se hierve y filtra, estas operaciones provocan la degradación total del polímero en medio alcalino fuerte, por otro lado el exceso de Sodio se neutraliza formando el alcóxido correspondiente en presencia de alcohol.
El filtrado se divide en porciones para cada una de las pruebas, la detección de azufre es positiva si hay formación de precipitado negro cuan do se adiciona ácido acético y una sal de plomo.
9. FISICOQUÍMICA DE LOS POLÍMEROS
El éxito en la aplicación en la disolución de los polímeros se debe en gran medida a la selección correcta del disolvente. En este sentido existen varias formas cualitativas y cuantitativas para elegir el disolvente adecuado.
Se deberán considerar dos puntos importantes.
a) El disolvente es absorbido por el polímero produciendo hinchamiento y generando un gel.
b) El gel formado gradualmente se desintegra formando una solución verdadera.
9.1 Reglas empíricas.
Existen tres criterios generales para establecer el comportamiento de la solubilidad.
a) El tamaño del polímero en estudio.
b) La viscosidad de las soluciones generadas.
e) La presencia de alguna fase cristalina
En primer término la solubilidad es favorecida cuando existe similitud estructural y química. Es decir la solución se forma cuando existen fuerzas atractivas entre las moléculas del disolvente y del soluto. En este sentido se puede concluir que las atracciones soluto solvente son mayores cuando las dos moléculas tienen polaridad equivalente.
9. 2. Energía libre de mezclado.
En un intento por resolver el problema de solubilidad de un polímero en solución y mezclas, desde el punto de vista cuantitativo se usa la ecuación de la primera ley de la termodinámica, es decir, la energía libre de mezclado que gobierna la solubilidad de un componente en otro.
a) Polímeros en solución y su comportamiento
Una amplia variedad de aplicaciones de los polímeros en diversas áreas de la ingeniería se debe a los polímeros en solución, en el caso por ejemplo de la producción de pinturas barnices y adhesivos se requiere un buen control de la viscosidad de las soluciones.
En solución las atracciones intermoleculares entre el disolvente y el soluto son efectivas cuando el soluto se disuelve, en primer término cuan do un polímero se disuelve existe un proceso lento de hinchamiento, conocido como solvatación en donde el polímero hinchado se relaciona al parámetro de solubilidad y a la densidad de energía cohesiva.
Por otra parte entre más alto sea el peso molecular resulta más difícil seleccionar al mejor disolvente,
Los polímeros lineales y ramificados se disuelven posteriormente en una segunda etapa, mientras los polímeros entrecruzados permanecen en condiciones de hinchamiento. En este sentido es importante conocer que es lo que se está disolviendo empleando la segunda ley de la termodinámica y los parámetros de solubilidad.
b) Separación fraccionada.
En el sentido más general, fraccionar un polímetro consiste en separarlo en sus diferentes especies moleculares de manera a obtener fracciones cuyas moléculas sean idénticas: así una muestra puede presentar tres tipos de heterogeneidad
— Pesos moleculares diferentes.
— Configuraciones diferentes (moléculas lineales o ramificadas).
— Composición química diferente (para los copolímeros).
En la mayoría de los casos, la configuración y la composición química son iguales para todas las moléculas, el fraccionamiento se limitará a la separación de las especies según su tamaño.
10. DEGRADACIÓN DE POLÍMEROS.
La degradación o envejecimiento de los polímeros se refiere a los cambios que sufren estos materiales en sus propiedades al interaccionar con el medio y el ambiente en que se encuentren.
Existen diferentes maneras de considerar la degradación: natural, acelerada, artificial, física y química.
La natural considera al polímero sometido a la influencia de elementos naturales o bien toma en cuenta las consecuencias de su uso.
La acelerada consiste en someter al material polimérico a condiciones climatológicas diferentes para las que fue diseñado, lo cual va a repercutir en su tiempo de vida útil.
La artificial es un caso muy particular de envejecimiento y consiste en aplicar al material condiciones de exposición controlada y se realiza en equipos o cámaras que simulan un clima natural.
La física engloba a todos los fenómenos que interaccionan con los polímeros sin modificar la estructura química de los mismos; en este tipo de envejecimiento se consideran dos fenómenos: uno que implica transferencia de masa y otro en el que no la hay.
La química implica la modificación estructural del material polimérico expuesto a determinadas condiciones como puede ser la luz. Temperatura en presencia o ausencia de oxigeno, disolventes, diferentes tipos de radiaciones y diversos microorganismos.
10. 1. Reacciones de degradación
La degradación de los polímeros es un proceso que ocurre por la ruptura de la cadena principal o la de los enlaces de los grupos laterales.
Los tipos de degradación más importantes son:
a) Degradación al azar, que es un proceso caracterizado por la ruptura del enlace de la cadena principal en la forma aleatoria.
b) Degradación de los enlaces débiles. El caso clásico es cuando las cadenas poliméricas contienen un carbón cuaternario, es decir, el polimetacrilato de metilo en donde por calentamiento se logra casi el 100% de recuperación del monómero (en atmósfera inerte) al no existir hidrógenos laterales en la cadena se evita la formación de agua.
c) Proceso de depolimerización. Es un proceso inverso al de la polimerización. Consiste en las siguientes etapas:
a) Inicio en el final de la cadena
b) Degradación
c) Terminación de segundo orden, ya sea por desproporción y/o combinación.
En este tipo de degradación, la depolimerización ocurre principalmente en macromoléculas
Es importante aclarar que en la depolimerización la reacción se produce en cadena, en tanto que en la degradación al azar y en la de enlaces débiles es una reacción en etapas.
Los procesos tanto de depolimerización como de degradación al azar, pueden ocurrir al someter a la acción del calor, luz o radiaciones ultrasónicas. Una muestra polimérica, en cuyo caso recibe el nombre de degradación térmica, fotodegradación y degradación radioactiva, respectivamente.
También existe la degradación mecánica que se produce por la acción de fuerzas cortantes, vibraciones ultrasónicas, por congelación rápida y repetida del disolvente de una solución de polímeros, agitación a una alta velocidad.
La degradación química, que se origina por la acción de agentes químicos y, por último, la biodegradación que se produce por acción de enzimas, bacterias, hongos.
Características de la degradación de los polímeros.
| Tipos de reacción | Puntos de Inicio | Estructura típica de los polímeros | Productos |
| Depolimerización | Final de cadena | Polímeros, vinílicos | Monómeros |
| Degradación al azar | Puntos al azar | Polímeros de condensación o en polímeros vinílicos no sustituidos o monosustituidos | Productos de mezclas diversas |
| Degradación en los enlaces débiles | Enlaces débiles | Polímeros naturales | Productos de mezclas diversas |
11. ADITIVOS DE LOS POLÍMEROS.
La mayoría de las propiedades de los polímeros son intrínsecas, es decir, son caracteríscas esenciales del polímero específico. Algunas de estas propiedades se relacionan y se controlan con la estructura molecular, sin embargo, muchas veces es necesario modificar las propiedades mecánicas, químicas y físicas en un grado mucho mayor que el permitido por la simple alteración de la estructura molecular fundamental. Por ello, substancias alógenas, denominadas aditivos, se introducen intencionadamente para modificar muchas de estas propiedades y para aumentar la utilidad del polímero. Son aditivos típicos los rellenos, los plastificantes, los estabilizantes, los colorantes y los ignífugos.
11. 1. Rellenos.
Los materiales de relleno se adicionan a los polímeros para incrementar las resistencias a la tracción, a la compresión y a la abrasión, la tenacidad, la estabilidad dimensional y térmica y otras propiedades. Como relleno se utiliza serrín, sílice, arena, vidrio, arcilla, talco, caliza e incluso polímeros sintéticos, todos ellos finamente pulverizados. Los tamaños de las partículas van de 10 nm a dimensiones macroscópicas. El coste del producto final disminuye por que estos materiales baratos substituyen una parte del volumen de los polímeros más caros.
11. 2. Plastificantes.
La flexibilidad, la ductilidad y la tenacidad de los polímeros pueden mejorarse con la ayuda de los aditivos denominados plastificantes. Su presencia también reduce la dureza y la fragilidad. Los plastificantes suelen tener baja presión de vapor y bajo peso molecular. Las diminutas moléculas de los plastificantes ocupan posiciones entre las grandes cadenas poliméricas, incrementando la distancia entre cadenas y reduciendo los enlaces secundarios intermoleculares. Generalmente se utilizan plastificantes en la elaboración de polímeros frágiles a temperatura ambiente, tales como cloruro de polivinilo y algún copolímero del acetato. Los plastificantes disminuyen la temperatura de transición vítrea y de este modo los polímeros se pueden utilizar a temperatura ambiente en aplicaciones que requieren algún grado de flexibilidad y de ductilidad. Estas aplicaciones incluyen láminas delgadas o películas, tubos, impermeables y cortinas.
11. 3. Estabitizantes.
Algunos materiales poliméricos, en condiciones ambientales normales, se deterioran rápidamente, generalmente en términos de integridad mecánica. Este deterioro suele ser el resultado de la exposición a la luz, en particular a la radiación ultravioleta, y también a la oxidación. La radiación ultravioleta interacciona con los enlaces covalentes y puede romper algunos de ellos a lo largo de la cadena molecular; esto puede generar también un entrecruzamiento de cadenas. El deterioro por oxidación es consecuencia de la interacción química entre átomos de oxígeno y moléculas poliméricas. Los aditivos que contrarrestan este proceso de deterioro se denominan estabilizantes.
11. 4. Colorantes.
Los colorantes dan un color específico al polímero. Se pueden adicionar como tintes o pigmentos. Los tintes actúan como disolventes y se incorporan a la estructura molecular del polímero.
Los pigmentos son como material de relleno que no se disuelven, sino que permanecen como fases separadas; generalmente son partículas de pequeño tamaño, transparentes y con índice de refracción próximo al polímero base. Otros aditivos dan opacidad y color al polímero.
11. 5. Ignífugos
La inflamabilidad de los polímeros es una característica del máximo interés, sobre todo en la fabricación de textiles y de juguetes para niños. La mayoría de los polímeros, en estado puro son inflamables, a excepción de los que contienen elevada proporción de cloruros y/o fluoruros, tales como los cloruros de polivinilo y politetrafluoretileno. La resistencia a la inflamabilidad de los polímeros combustibles aumenta adicionando aditivos denominados ignífugos (o retardadores de llama).
Estos aditivos funcionan interfiriendo el proceso de combustión mediante una fase gaseosa o iniciando una reacción química que enfría la región de combustión y cesa el fuego.
12. USOS Y APLICACIONES.
¿Imaginas la cantidad de posibilidades que tienes de desarrollarte en la industria al fabricar productos de Polímeros?
12. 1. Automotriz.
La industria automotriz ha recibido con gran aceptación la infinidad de artículos que pueden ser fabricados de resina con refuerzo de fibra de vidrio.
Partes automotrices pequeñas, asientos, porta equipajes o la elaboración de carrocerías completas son sólo un ejemplo de los alcances que tiene este tipo de aplicación.
El avance tecnológico que se genera en la industria, día con día hace indispensable la creación de materiales más innovadores, altamente resistentes, ligeros y considerablemente económicos.
La resina poliéster ha cumplido con los requisitos y al conjugarse con un material como la fibra de vidrio ha dado como resultado un producto de gran demanda en el mercado automotriz.
12. 2. Concreto.
La fabricación de concreto polimérico para fachadas, domos, estructuras, pisos e incluso para casas prefabricadas son sólo un ejemplo de la infinidad de posibilidades que existen en esta industria.
Su magnífico desempeño ha generado una enorme demanda en esta industria, pues ha demostrado ser un producto con excelentes propiedades y características que pueden modificarse de acuerdo a las necesidades de aplicación.
12. 3. Mueblera.
Una industria de resiente incursión es la mueblera. Las propiedades de flexibilidad, resistencia a la corrosión, a la intemperie y a altas temperaturas han hecho del plástico reforzado el material idóneo para la fabricación de puertas y molduras de imitación madera.
12. 4. Muebles de baño.
Es sólo una de las innumerables aplicaciones que se ha encontrado en la industria sanitaria a la Resina poliéster reforzada con fibra de vidrio.
Su insuperable versatilidad te permite hacer con este producto infinidad de artículos con alta resistencia a la corrosión, a temperaturas altas, al impacto y con acabados y texturas de gran belleza. La conjunción de resina, fibra de vidrio y complementos han dado como resultado productos
12. 5. Artesanal.
Actualmente esta industria ha alcanzado un enorme auge comercial por la infinidad de artículos que pueden elaborarse con las Resinas poliéster.
Además de ser una actividad recreativa, la fabricación de figuras artesanales se ha vuelto un negocio altamente rentable. Su facilidad de fabricación y el bajo costo de inversión que representa ha generado una enorme demanda de los productos destinados para estos fines.
Resinas especiales para vaciados, encapsulados o moldes; el caucho de silicón, indispensable para la fabricación de moldes de larga vida útil, moldes de poliuretano para vaciados de figuras; son sólo una muestra de las posibilidades que se pueden elegir en el mundo de las resinas poliéster.
13. LUGARES DE INVESTIGACIÓN.
La investigación científica en el ICTP abarca una amplia serie de áreas innovadoras y de gran actualidad. Los trabajos realizados en los departamentos y grupos de investigación que componen el Instituto se resumen brevemente. Además, varios grupos de investigación del Instituto mantienen colaboraciones institucionales con Grupos de Investigación de otros centros a través de las Unidades Asociadas.
13. 1. Departamento de Física e Ingeniería de Polímeros.
El Departamento consta de dos grupos cuyas principales áreas de investigación están relacionadas con el diseño de nuevos materiales poliméricos tales como mezclas y materiales Compuestos, agentes de interfase y de vehiculización, con énfasis en la correlación entre la estructura, morfología y propiedades en estado sólido de los distintos sistemas
13. 2. Departamento de Fotoquímica de Polímeros.
La investigación del Departamento se centra en polímeros fotosensibles. Consta de las siguientes líneas: 1) Recubrimientos y sistemas multicomponentes fotocurables, orgánicos e híbridos. 2) Censores fluorescentes de interés aplicado (estructura-fluorescencia-propiedades). 3) Aplicaciones agrícolas y fotodegradación-estabilización de polímeros. 4) Láseres poliméricos y ablación láser de polímeros
13. 3. Departamento Química Física de Polímeros.
Las líneas de trabajo desarrolladas en el Departamento son: Estudios cinéticos por RPE de la polimerización radical, síntesis y propiedades de cristales líquidos y sustratos biodegradables, propiedades conformacionales, simulación y medida de transporte en membranas, propiedades térmicas y mecánicas de poliolefinas metalocénicas, relajaciones mecánicas y dieléctricas, y espectroscopía e imagen de RMN.
13. 4. Departamento de Química Macromolecular.
El Departamento lo forman tres grupos de trabajo dedicados a la síntesis, caracterización y evaluación de polímeros especiales y con aplicaciones específicas. Las líneas fundamentales son: 1) Modificación química de polímeros y redes poliméricas, 2) Polímeros bioactivos y biomateriales, y 3) Polímeros de condensación y membranas poliméricas.
13. 5. Departamento de Química y Propiedades de Materiales Poliméricos.
En la actualidad el Departamento trabaja en las siguientes líneas: Homo- y copolimerización radical, procesos convencionales y nuevos procesos de polimerización viva/controlada, copolímeros de bloque y de injerto, modificación química de copolímeros anfifílicos y polímeros biocompatibles, aplicaciones bioactivas y medioambientales, síntesis de poliolefinas, correlaciones microestructura química-táctica con estabilidad termooxidativa, microestructura-propiedades eléctricas, dieléctricas y termooxidación de polímeros de interés industrial.
13. 6. Departamento de Química y Tecnología de Elastómeros.
En la actualidad abarca las siguientes áreas: Preparación, estudio y propiedades de Compuestos de caucho vulcanizable, elastómeros termoplásticos, reforzamiento en elastómeros vulcanizables y termoplásticos, vulcanización de elastómeros, y síntesis de elastómeros de poliuretano. Además proporciona asistencia científico-tecnica a la industria del sector caucho.
BIBLIOGRAFÍA
Libros
Título: LOS POLÍMEROS. Síntesis, caracterización, degradación y reología.
Autor: Uribe Velasco, Miguel
Mehrenberger Y. Pierre
Editorial: © Instituto Politécnico Nacional, 1996.
Título: Introducción a la Ciencia e Ingeniería de los materiales. Tomo II
Autor: William D. Callister, Jr.
Editorial: © Reverte S. A., 1996.
Título: Ciencia de los Materiales, selección y diseño.
Autor: Pat L. Mangonon.
Editorial: © Prentice Hall, 2001.
Título: Fundamentos de la Ciencia e Ingeniería de Materiales.
Autor: William F. Smith
Editorial: © Mc Graw Hill, 1998.
Internet:
http://www.ciencia-ficcion.com/glosario/p/polimero.htm.
http://www.micromegas.com.mx/apuntes/documents/quiorg4-1/quiorg03.doc
http://www.poliformasplasticas.com.mx/aplicaciones/
LOS POLÍMEROS.
ÍNDICE.
1. Definición. 1
2. Historia. 2
3. Clasificación. 3
3.1 Obtención 3
3.2 Tipo de enlace 3
4. Polimerización 3
4.1 Polimerización por adición 4
4.2 Polimerización por condensación 6
5. Estructura Molecular 7
5.1 Polímeros lineales 7
5.2 Polímeros ramificados 7
5.3 Polímeros entrecruzados 8
5.4 Polímeros reticulados 8
6. Métodos Industriales de Polimerización 9
6.1 Polimerización en masa 9
6.2 Polimerización en solución 9
6.3 Polimerización en emulsión 10
6.4 Polimerización en suspensión 10
7. Copolímeros 11
7.1 Copolímeros aleatorios 11
7.2 Copolímeros alternados 11
7.3 Copolímeros en bloques 11
7.4 Copolímeros injertados 12
7.5 Clasificación de los diferentes tipos de polímeros 12
7.6 Aplicación de los copolímeros. 12
8. Caracterización Química de Polímeros 13
8. 1 Pruebas preliminares. 13
8. 2 Pruebas en productos puros. 14
9. Fisicoquímica de los Polímeros 15
9.1 Reglas empíricas. 15
9.2 Energía libre de mezclado. 15
10. Degradación de Polímeros 16
10. 1 Reacciones de degradación 16
11. Aditivos de los Polímeros 17
11. 1 Rellenos. 17
11. 2 Plastificantes. 18
11. 3 Estabitizantes. 18
11. 4 Colorantes. 18
11. 5 Ignífugos 18
12. Usos y Aplicaciones 19
12. 1 Automotriz. 19
12. 2 Concreto. 19
12. 3 Mueblera. 19
12.4 Muebles de baño. 19
12.5 Artesanal. 20
13. Lugares De Investigación 20
13. 1 Departamento de Física e Ingeniería de
Polímeros. 20
13. 2 Departamento de Fotoquímica de Polímeros. 20
13. 3 Departamento Química Física de Polímeros. 20
13. 4 Departamento de Química Macromolecular. 20
13. 5 Departamento de Química y Propiedades de Materiales Poliméricos 21
13. 6 Departamento de Química y Tecnología de
Elastómeros. 21
14. Bibliografía 22
20
cabeza a cola
cola a cola
cabeza a cabeza








Descargar
| Enviado por: | ServandoFlores Pérez |
| Idioma: | castellano |
| País: | México |
