Biología, Botánica, Genética y Zoología
Parasitología
|
ANTONIO ATENCIA MELIÁN - TÉCNICO DE MICROBIOLOGÍA |
Í N D I C E
Protozoos: Plasmodium
-
Introducción……………………………………………………………...……. 3
-
Ciclo Biológico………………………………………………………...……...4-5
-
Patogenia………………………………………………………………...……...6
-
Sintomatología………………………………………………………...………..6
-
Diagnostico Clínico……………………………………………………………..7
-
Tratamiento …………………………………………………………………….7
-
Profilaxis………………………………………………………………………...8
-
Epidemiología…………………………………………………………………...8
Platelmintos: Schistosoma
-
Introducción………………………………………………………………..10-11
-
Ciclo Biológico…………………………………………………………………12
-
Patogenia………………………………………………………………………13
-
Sintomatología…………………………………………………………...........13
-
Diagnostico Clínico………………………………………………………...13-14
-
Tratamiento…………………………………………………………………....14
-
Profilaxis……………………………………………………………………….14
-
Epidemiología……………………………………………………………...14-15
Nematodos: Capillaria
-
Introducción…………………………………………………………………...17
-
Ciclo Biológico……………………………………………………………..17-18
-
Patogenia………………………………………………………………………19
-
Sintomatología………………………………………………………………...19
-
Diagnostico Clínico…………………………………………………………....19
-
Tratamiento……………………………………………………………………19
-
Profilaxis……………………………………………………………………….20
-
Epidemiología………………………………………………………………….20
PROTOZOOS:
Plasmodium
Introducción
Plasmodium: generalidades
| (sin clasif.) Filo: Plasmodium | |||
-
Parasitosis caracterizada por episodios febriles típicos, precedido por escalofrío intenso que termina con diaforesis, hepatoesplenomegalia y anemia que varía de leve a grave.
-
Sinonimia: Malaria, Paludismo, fiebre intermitente, Fiebre de los Pantanos, fiebre palustre.
-
Plasmodiosis (Nombre científico)
-
Malaria (denominación mundial)
-
Paludismo (denominación latinoamericana)
-
Existen 4 especies de Plasmodium que
-
parasitan al hombre: P. vivax, P. malariae, P. falciparum y P. ovale.
-
Reservorio y huésped intermedio: hombre (fase asexual o esquizogónico)
-
Huésped definitivo: mosquito, en el que se lleva a cabo la reproducción sexual del plasmodio.
Historia
-
El paludismo es una de las enfermedades que ha aparecido en el hombre desde las fechas más remotas.
-
Marco Tenecio Columela, lo asoció a la existencia de mosquitos.
-
1880, Laveran agente etiológico, microorganismo de naturaleza animal.
-
1885, Danileuski, paludismo aviar.
-
1889, Sajaron descripción detallada del P. faciparum.
-
1890, Romanoswki introdujo el estudio microscópico de los plasmodios, el método panóptico de coloración con azul de metileno y eosina.
-
1897, Ross descubrió el transmisor del paludismo. Díptero del genero Anopheles y mas tarde todos los estadios morfológicos del esporogonio que se desarrolla en el mosquito.
-
1922, P. ovale en África.
-
1934, Raffaele y Cols. Fases exoeritrocíticas pigmentadas en el ciclo asexual de los plasmodios del paludismo de las aves.
-
1948, Garnham describe la fase exoeritrocitica de P. vivax en los hepatocitos humanos.
Ciclo Biológico
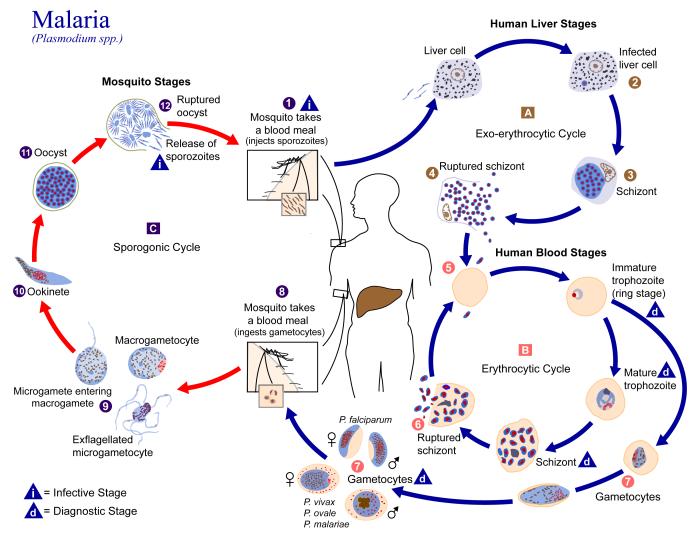
En el ciclo del Plasmodium existe un agente vector (la hembra de un mosquito), donde el Plasmodium se reproduce sexualmente y un hospedador vertebrado intermediario (el ser humano u otro animal). La siguiente explicación puede seguirse en la figura de abajo.
Etapas exo-eritrocíticas o hepáticas (A en la figura). Tras la picadura del mosquito, éste inocula el parásito existente en su saliva en la sangre o en el sistema linfático del huésped (1). En ese momento, el Plasmodium se encuentra en la fase de su ciclo conocida como esporozoito. Los esporozoitos pasan al torrente sanguíneo hasta que llegan a los hepatocitos del hígado (2). Allí se multiplican por esquizogénesis (disgregación) formando el esquizonte hepático (3), tras lo cual se rompe el hepatocito, apareciendo un nuevo estadío del Plasmodium, el merozoito (4). Aquí hay un primer ciclo asexual, en el que los merozoitos pueden o bien reinfectar hepatocitos o bien volver de nuevo al torrente sanguíneo, donde penetran en los eritrocitos.
Etapas eritrocíticas o sanguíneas (B). En los eritrocitos, los merozoitos comienzan a alimentarse de la parte proteíca de la hemoglobina contenida en éstos, apareciendo entonces el trofozoito (5). Nuevamente por esquizogénesis se multiplica en el interior de dichas células, formándose el esquizonte hemático. También se rompe la célula, en este caso el eritrocito, liberando nuevos merozoitos (6). La mayoría de los merozoitos continúan con este ciclo replicativo infectando nuevos eritrocitos, pero algunos se convierten en gametocitos, masculinos y femeninos (7).
Etapas en el mosquito (C). Si el individuo infectado es nuevamente picado por un mosquito, los gametocitos masculinos y femeninos pasan al mosquito (8). En el interior de éste se diferencian en gametos (4-8 microgametos por cada gametocito masculino y una macrogameta por cada gametocito femenino) y al fusionarse ambos gametos, se producen los zigotos (9). Los zigotos, a su vez, se convierten en oocinetos móviles y alargados (10), que invaden la pared intestinal del mosquito, donde se desarrollan en ooquistes (11). Los ooquistes crecen, se rompen y liberan una nueva generación de esporozoitos (12), que hacen su camino a la glándulas salivares del mosquito. Es en esta fase en la que el Plasmodium puede volver a ser inyectado en el huéped.
En algunas especies de Plasmodium, el esquizonte hepático puede permacer en estado latente, en forma de hipnozoito. La reactivación de los hipnozoitos puede ocurrir hasta un máximo de 30 años después de la infección inicial en el ser humano. No se conoce todavía cuáles son los factores de reactivación. Entre las especies que forman hipnozoitos están P. malariae, P. ovale y P. vivax. La reactivación no se produce en las infecciones por P. falciparum. No se sabe si la reactivación del hipnozoito se produce en las restantes especies que infectan a los seres humanos, pero es posible que este sea el caso.
La transición desde la etapa hepática a la eritrocítica ha sido confusa hasta hace poco tiempo. En el año 2006[] se demostró que el parásito sale de los hepatocitos en merosomas que contienen cientos o miles de merozoitos. Se ha demostrado posteriormente que estos merosomas se dirigen a los capilares pulmonares y lentamente se desintegran en unas 48-72 horas liberando los merozoitos. La invasión de los eritrocitos es mayor cuando el flujo sanguíneo es lento y las células están perfectamente empaquetadas: estas dos condiciones se dan juntas en los capilares alveolares.
Patogenia
P. vivax y P. ovale tienen predilección por hematíes jóvenes, P. malariae sólo por los maduros y P. falciparum por los hematíes de todas las edades, lo que explica el alto grado de parasitación que alcanza este último durante la infección. El merozoíto deja alteraciones morfológicas visibles al microscopio electrónico en forma de gránulos densos y que se denominan knobs o nudos en la membrana del hematíe. Están repletos de antígenos parasitarios, como HRP1, HRP2, rosetinas, Pf EMP-1 y serán el punto de anclaje del hematíe parasitado a los receptores del endotelio vascular en un fenómeno complejo de citoadherencia y secuestro que es patrimonio exclusivo de P. falciparum. CD36, molécula de adhesión intercelular (ICAM-1), molécula de adhesión vascular (VCAM-1), trombospondina (TSP) y molécula de adhesión endotelial (ELAM-1) son los receptores más importantes y más abundantes en el endotelio cerebral. Las plaquetas expresan en su superfície una integrina (LFA-1) que se funde con el endotelio, expresándola en su superfície, lo que aumenta la citoadherencia endotelial. Las citocinas producidas por los macrófagos estimulados, como el factor de necrosis tumoral alfa (TNF), activan los receptores endoteliales aumentando la citoadherencia, producen daño endotelial directo y estimulan la producción de óxido nítrico (NO). En la figura 3 se muestra el fenómeno de citoadherencia. Hay una correlación evidente entre los niveles séricos de TNF (> 200 pg/ml) y la mortalidad, por lo que se podría considerar que el paludismo es una enfermedad mediada por toxinas, similar a la del shock séptico. La formación de rosetas es otro factor patogénico añadido: un hematíe parasitado y adherido se agrega a otros 10 hematíes no parasitados mediante rosetinas y otros ligandos, lo que aumenta el bloqueo de la microcirculación. En ocasiones existe una disociación entre el grado de parasitación y la gravedad, tanto en no inmunes como en semiinmunes, lo que sugiere la existencia de otros factores patogénicos. Hoy día se aboga por diferencias de virulencia entre distintas cepas de la misma especie.
Sintomatología
El período de incubación de la enfermedad varía entre 8 y 30 días. En todas las especies de plasmodium, la sintomatología está caracterizada por la clásica crisis febril palúdica que consiste en un cuadro que comienza con unas horas de malestar general, dolor de cabeza y molestias musculares, para posteriormente aparecer escalofríos con intensa sensación de frío, que requiere cubrirse con abundante ropa, coincidiendo cuando los parásitos rompen los glóbulos rojos y escapan hacia la sangre. Tras este periodo que dura de 15 a 60 minutos, aparece el período febril, con enrojecimiento facial, piel seca y elevación de la temperatura que pueden alcanzar hasta los 41 °C. Este episodio suele durar 2-6 h y durante esta fase es posible que los parásitos invadan otros glóbulos rojos. El tercer período se caracteriza por gran sudación, descenso de la temperatura, abatimiento y somnolencia. Este período suele durar 2-4 h. Esta sintomatología se repetirá por ciclos de 48-72 horas según el subtipo de plasmodium.
El paciente podrá presentar síntomas más inespecíficos derivados de la anemia producida por la destrucción de glóbulos rojos, así podrá presentar síntomas como cansancio, palidez, taquicardia, coloración amarillenta de la piel entre otros. En la exploración física se evidenciarán agrandamiento del bazo y del hígado.
Existe un tipo de plasmodium muy agresivo denominado Plasmodium falciparum que con frecuencia produce complicaciones en otros órganos, en muchas ocasiones debidas a un fenómeno de falta de riego. Así puede producir alteraciones a nivel cerebral, del riñón, alteraciones de la coagulación, bajo azúcar en la sangre, entre otros.
Diagnóstico Clínico
El diagnóstico se confirma mediante la visualización al microscopio de los parásitos dentro de los glóbulos rojos mediante diferentes técnicas. La más usada es la denominada como Gota gruesa, que consiste en obtener una muestra de sangre y analizarla al microscopio y permite conocer si existe infección malárica aunque no es capaz de diferenciar el subtipo. Para ello será necesaria una extensión de sangre teñida con diferentes colorantes y llevar a cabo un estudio microscópico más detenido.
Existen kits para el diagnóstico rápido de paludismo con bastante fiabilidad, sin embargo no distinguen bien el tipo de plasmodium y además suele ser casi siempre para detectar el subtipo Falciparum.
Se investigan otros procedimientos como la detección mediante técnicas de ingeniería genética del material del genoma del parásito, sin embargo este resulta un sistema poco económico.
En un análisis de sangre rutinario podremos encontrar un recuento de glóbulos rojos disminuido, y en ocasiones un aumento de glóbulos blancos. Aparecerá elevación de los niveles de LDH y Bilirrubina.
Tratamiento
La malaria por Falciparum siempre requerirá hospitalización. En general el tratamiento va a depender básicamente del área geográfica donde se ha producido la infección, dado que existirán regiones resistentes a unos tratamientos.
Normalmente, la cloroquina es el fármaco utilizado con más frecuencia, aunque no debe de emplearse en niños, ya que puede ocasionar efectos secundarios importantes, especialmente a nivel de la visión. Sin embargo en caso de infecciones resistentes a la cloroquina, se suministrará la quinidina o quinina que debe de utilizarse con precaución por sus efectos tóxicos, o la combinación de pirimetamina y sulfadoxina. Otro fármaco útil es la mefloquina, el cual tiene mínimos efectos secundarios y es efectivo frente a las cepas de Plasmodium Falciparum resistentes a la cloroquina.
Para prevenir recaídas de la enfermedad se utiliza fosfato de primaquina que además es especialmente útil para aquellos subtipos de plasmodium que tienen tendencia a permanecer latentes en el hígado, donde el resto de tratamientos tienen menos efectividad.
Profilaxis
Las medidas preventivas se van a basar en evitar la picadura del mosquito y la administración de fármacos antiparasitarios.
En general en las regiones del mundo donde existe paludismo la población puede haber desarrollado inmunidad frente a la infección, por ello será en aquellos visitantes procedentes de zonas sin malaria en los que la enfermedad se trasmitirá con más frecuencia. Por ello se recomienda el uso de fármacos antipalúdicos a aquellas personas que van a viajar a zonas con malaria. Se debe consultar con tiempo a su médico con el fin de comenzar el tratamiento 2 semanas antes de llevar a cabo el viaje e incluso mantener el tratamiento hasta 4 semanas después.
El tratamiento farmacológico empleado dependerá del área geográfica del viaje y la resistencia o no a cloroquina. En general el tratamiento incluirá los siguientes fármacos: mefloquina, atovaquona/Proguanil y doxiciclina.
Sin embargo las personas que reciben medicamentos contra el paludismo pueden infectarse. Por lo tanto, se debe evitar la picadura del mosquito usando mallas en las ventanas, repelentes contra insectos y prendas de vestir que cubran completamente manos y piernas.
Epidemiología
PLATELMINTOS:
Schistosoma
Introducción
Schistosoma
Los schistosoma son un género de parásitos trematodos y Platihelmintos, comúnmente llamados bilharzia. Causan la infección más importante del hombre de entre todos los gusanos planos. La especie adulta fue descubierta en un paciente de Egipto en 1851 durante una autopsia hecha por el Dr. Theodore Maximilian Bilharz. Todas las especies de Schistosoma tienen al molusco como hospededario intermedio, una relación que fue hecha a comienzos del siglo 20. En África, después de la malaria es la enfermedad tropical mas prevalente en el hombre y de gran importancia socio-económica y en salud pública para países en desarrollo.[ Se encuentra prevalente en 3/4 partes de los países en desarrollo y más del 80% de los afectados viven en el África al sur del Sahara.
La enfermedad es la Schistosomiasis, que es la 2ª enfermedad en importancia después de la malaria. También se la conoce como BILHARZIASIS, ya que fue Bilharz el primero que vió un Schistosoma.
La SCHISTOSOMIASIS está producida por especies del género Schistosoma, el cual se incluye dentro de la familia Schistosomatidae.
Características generales
Dentro del género Schistosoma, hay 6 especies que afectan al hombre produciendo la enfermedad denominada SCHISTOSOMIASIS o BILARZIASIS. Son unisexuales, es decir, dioicos.
Los machos. Son planos y sus laterales están incurvados, dejando una cavidad llamada canal ginecóforo (donde está la hembra). No tiene faringe y los ciegos intestinales son simples y soldados posteriormente. Tienen un número variable de testículos.
Las hembras. Presentan el cuerpo cilíndrico, más fino y tampoco tienen faringe. Presentan un solo ovario que puede ser: preecuatorial, ecuatorial, postecuatorial. Presentan también una sola banda de glándulas vitelógenas en posición ecuatorial. Tienen un útero corto y un número variable de huevos (dependiendo de la especie de la que se trate). El poro genital es postacetabular. Los huevos sin opérculo con espolones y embrionados en el momento de la puesta.
Las ventosas pueden ser:
-
- Sésiles.
-
- Pedunculadas.
Son parásitos hemáticos (los adultos), de mamíferos y de aves. El ciclo biológico es diheteroxeno: con un vertebrado y un molusco (acuático de agua dulce y no presenta metacercarias).
Especies y diferencias
Diferenciación según la morfología del adulto:
1.- Presenta cuerpo con tegumento:
a) Liso
b) Con papilas (ornamentación).
2.- Tipo de ventosas:
a) Sésiles
b) Pedunculadas
3.- Posición respecto al ecuador donde se unen los ciegos.
4.-Número de testículos.
5.- Posición respecto al ecuador del ovario.
6.- Número de huevos en el útero.
* Schistosoma haematobium. * Schistosoma mansoni.
-
- Tegumento con tubérculos pequeños. - Tegumento con tubérculos
grandes.
-
- Ventosas sésiles. - Ventosas sésiles.
-
- Macho: unión de los ciegos ecuatorial - Macho: unión de los ciegos
(4-5 testículos) preecuatorial (6-9 testículos)
-
- Hembra: ovario postecuatorial. - Hembras: ovario preecuatorial.
20-100 huevos (50 media). 1-2 huevos.
* Schistosoma japonicum. * Schistosoma mekongi.
-
- Tegumento liso. - Ventosa oral con acetábulo
pedunculado.
-
- Ventosa oral sésil y acetábulo pedunculado - Tegumento liso - Ventosas sésiles.
-
- Machos: unión de ciegos postecuatorial. - Macho: unión de ciegos
-
postecuatorial.
- 7 testículos. - 7 testículos.
-
- Hembras: ovario preecuatorial. - Hembras: ovario ecuatorial.
- Hasta 300 huevos con una media de 50. - 120-130 huevos.
* Schistosoma intercalatum.
-
- Tegumento con tubérculos pequeños.
-
- Ventosas sésiles.
-
- Macho: unión de los ciegos es ecuatorial.
4-5 testículos.
-
- Hembra: ovario postecuatorial.
10-100 huevos.
Ciclo Biológico
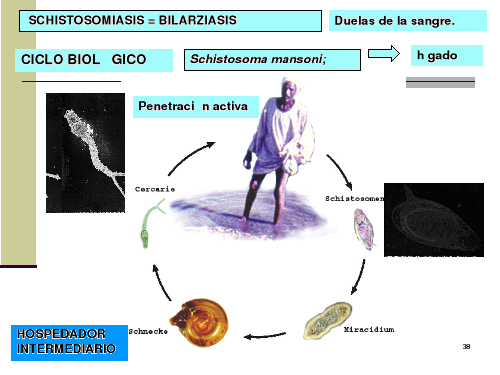
Se trata de un ciclo diheteroxeno. Los adultos son hematófagos. Viven en las venas que irrigan distintos órganos abdominales del hospedador. (Al conjunto de venas se le llama plexo). Aquí se da la fecundación. El macho transporta a la hembra hasta las venas más finas y allí abandona al macho para con su menor tamaño proseguir por las vénulas más finas. Allí deposita los huevos, éstos atraviesan la pared de las vénulas donde fueron depositados, atraviesan los tejidos y caen bien a la luz intestinal, o la luz de la vejiga de la orina (vesical), dependiendo de la especie.
Los huevos salen al exterior por la orina o por heces (según especies). Se piensa que los huevos cuando están en las vénulas, se rodean por pequeños coágulos de sangre que con la acción de los fibroblastos y las células endoteliales hace que se adelgace la pared de las vénulas y así las pueden atravesar mejor.
Los huevos salen embrionados y en agua dulce, eclosionan, liberan el miracidio que penetra en el caracol (1º hospedador intermediario). En el caracol se produce un esporocisto madre que origina esporocistos hijos. Finalmente se liberan al agua las cercarias. Éstas se caracterizan porque presentan una cola bifurcada (por ello se las llama furcocercarias), y presentan unas glándulas de penetración.
Estas cercarias contactan con la piel humana, la atraviesan (por las glándulas de penetración), pierden la cola y ahora se llaman Schistosómulos. Éstos alcanzan la circulación periférica, pasan al hígado, donde maduran para luego trasladarse al microhábitat que le es típico (las venas), así queda cerrado el ciclo.
Patogenia
El huésped intermediario de S. mansoni es un caracol que libera cercarias en lagos/estanques de agua dulce. Las cercarias penetran a través de piel expuesta del nadador e inician dermatitis. La mayoría migra al hígado y madura en formas de hembra o macho características que viven en las venas del mesenterio y se reproducen continuamente. La hembra produce hasta 300 huevos/día. La respuesta inmune a los huevos contribuye a patología hepática y esplénica. Los huevos se excretan por las heces.
Sintomatología
I. Periodo de invasión. Entrada del parásito por la piel. Produce escozor y a veces lesiones cutáneas pasajeras.
II. Periodo de incubación. Migración del Schistosoma por el sistema circulatorio hasta su microhábitat definitivo. Pueden darse ligeras hemorragias (incluso en pulmón), alergias pulmonares, inflamación del pulmón e hígado. Aparece un estado de toxemia (toxinas en sangre) que produce fiebres irregulares. También produce eosinofilia y leucocitosis.
III. Periodo de estado. Puesta de huevos. Se dan hemorragias y los síntomas del periodo anterior, además de dolores abdominales y según especies: orinas sanguinolentas (Schistosoma haematobium) o heces sanguinolentas (resto de las especies).
IV. Periodo de reparación de tejidos. Los tejidos dañados se regeneran rápidamente o no se reparan porque se originan neoplasias (sobre todo por S. haematobium) Aparecen granulomas (por presencia de huevos) y fibrosis en el hígado. Esta fibrosis es peri-portal, y recibe el nombre de fibrosis de Symmer o en “boquilla de pipa”.
La reacción inmunitaria del organismo es evadida por los Schistosomas por mimetismo molecular y en el organismo (hombre) se producen anticuerpos diferentes para los distintos estadíos del parásito, tenemos:
Anticuerpos antihuevo
Anticuerpos anticercaria
Anticuerpos antiadulto
Diagnóstico Clínico
-Etiológico-
Para ello haremos la búsqueda de los huevos en heces (técnica de Kato-Katz), o en orina por la técnica de filtración. Podemos buscar los huevos en la mucosa intestinal por medio de una biopsia.
-Serológico-
IFI.
ELISA.
Técnicas de precipitación “in vivo”:
a) Técnica de Vowel-Minning (técnica de reacción de circumprecipitación cercariana R.C.C). Con esta técnica ponemos las cercarias en contacto con el suero del paciente. Si el suero presenta anticuerpos específicos, veremos la presencia de un precipitado muy específico porque intervienen antígenos metabólicos de las cercarias.
b) Técnica de Oliver-Gonzalez (técnica de circumprecipitación oval R.C.O). Es igual que la anterior pero se usan huevos vivos.
Con estas técnicas podemos determinar la evolución de la enfermedad, ejemplo: para una Schistosomiasis reciente utilizaremos la técnica de R.C.C.
Tratamiento
-
- Prazicuantel (para todas las Schistosomiasis)
-
- Oxamniquina (para mansoni)
-
- Metrifonato o metrifonato y niridazol (para S. haematobium).
Profilaxis
A nivel de hospedador definitivo.
1. Educación sanitaria y no usar agua con posibles detritos.
2. Tratamiento de los enfermos.
3. Control de reservorios.
4. Evitar que las heces y la orina lleguen al agua.
Control a las cercarias:
1. Medidas de lucha contra cercarias (en agua), utilizando productos químicos.
Medidas de lucha contra el hospedador intermediario (caracol).
1. Control químico (molusquicidas) o biológico (depredadores de moluscos, moluscos contra moluscos).
Epidemiología
Asociada a personas que están en contacto con aguas contaminadas. Suele darse en zonas de regadío o donde el hombre está descalzo y en contacto con el agua.
La distribución geográfica, varía según las especies:
S. haematobium. África (sobre todo en Madagascar y Egipto), parte occidental de Asia. Como reservorios tenemos: monos y mandriles.
S. mansoni. Su origen fue en África pero por el traslado de esclavos, se da en el sur y centro de América (en islas de las Antillas). Reservorios: monos, mandriles y roedores.
S. japonicum. Extremo oriente, en la actualidad no existe en Japón. Los reservorios son: muchas especies diferentes (caballos, cerdos, vacas, perros...) Se trata de una especie muy eurixena.
S. intercalatum. Se da sobre todo en África central. Como reservorios están los roedores.
S. mekongi. Se da en Laos, Camboya, Tailandia, y Malasia. Los reservorios son desconocidos.
S. malayensis. Malasia.
NEMATODOS:
Capillaria
Introducción
Capillaria
Este parásito se encuentra sobre todo en roedores, gatos, perros, aves, aunque se han divulgado casos en seres humanos. Los gusanos viven en el hígado del hospedador, rodeado generalmente por una cápsula del tejido fino conectivo. La hembra del adulto produce los huevos, pero pocos de estos huevos pasan a las heces del hospedador.
Huevo de Capillaria
Especies y Agentes Causales
El nematodo Capillaria philippinensis causa capillariasis humano intestinal. Otras dos especies de capillaria son típicas en animales aunque existen casos raros de infecciones humanas. Ellos son C. hepatica, que causa en la gente capillariasis hepática, y C. aerophila, que causa en la gente capillariasis pulmonar.
Ciclo Biológico
Normalmente los huevos de Capillaria philippinesis son excretados por un ave 
por el cual llegan al agua de un río, lago, etc. (agua dulce). Allí los huevos maduran 
. Posteriormente un pez lo ingiere y las larvas del parasito penetran en su intestino y emigran a los tejidos 
.
La ingestión de pescado crudo o poco cocido causa la infección al humano 
. Los adultos de Capillaria philippinesis (machos: 2.3 a 3.2 mm; hembras: 2.5 a 4.3 mm) residen en el intestino humano, donde estos erosionan la mucosa 
. Las hembras depositan huevos sin eclosionar. Algunos de estos terminan madurando en el intestino, y liberan las larvas que pueden causar la autoinfección. Esto conduce a la hiperinfección (un número masivo de gusanos adultos) 
. Capillaria philippinesis actualmente es considerado un parásito de peces (hospedador intermedio) del cual se alimentará un pájaro (hospedador definitivo) 
.
Capillaria hepatica: los gusanos adultos residen en el hígado de varios animales, sobre todo ratas. Las hembras producen los huevos que son conservados en el hígado del roedor. Cuando el animal infectado es comido por otro animal, los huevos son liberados por la digestión, excretados en el excremento del segundo animal, y maduran en el suelo. O bien, los huevos pueden ser liberados después de la muerte y la descomposición del primer animal hará que maduren en el suelo. La ingestión por otro animal, hará que los huevos infecciosos liberen larvas en el intestino que emigrarán por la circulación portal al hígado, donde se desarrollan en adultos.
Capillaria aerophila: los gusanos adultos residen en el epitelio de la extensión traqueo bronquial de varios animales. Los huevos son tragados por el animal y excretados en su excremento. Los huevos se maduran en el suelo. La ingestión de huevos infecciosos completa el ciclo. El transporte o anfitriones también pueden intervenir en el ciclo.
Patogenia
En infecciones graves de capillariosis la acción patógena es mecánica (por presión y obstrucciones), irritativa (toxica y antigénica) debida a productos metabólicos de secreción y excreción así como la expoliatriz (principalmente histófagas) tiene como consecuencia una marcada cirrosis (se ha señalado algunos casos fatales en el hombre). El proceso que se desarrolla es el de una granuloma que puede contener los parásitos; cuando ocurre su degeneración se encuentran restos del parasito y masas de huevo; hay una lesión inflamatoria crónica de los linfocitos, células plasmáticas y macrófagos así como una reacción de tejido conectivo fibroso. Los granulomas pueden estar en cualquier área, aunque tienden a estar en la superficie del área periportal o de la vena central.
Sintomatología
Capillariasis intestinal (causado por C. philippinensis) se manifiesta con dolor abdominal y la diarrea, que, de ser intratado, puede hacerse severa debido a la autoinfección. Una perdición de proteína enteropática puede desarrollarse con caquexia y en el peor de los casos la muerte.
Capillariasis hepática (causado por C. hepatica) se manifiesta con una hepatitis aguda o subaguda con eosinofilia, con la diseminación posible a otros órganos. Puede ser fatal.
Capillariasis pulmonar (causado por C. aerophila) puede presentar síntomas como la fiebre, la tos, el asma, y la pulmonía, y también puede ser fatal.
Diagnóstico Clínico
El diagnóstico específico de C. philippinensis es establecido por la presencia de huevos, larvas y/o gusanos adultos en el ano, o en biopsias intestinales. Los huevos son la etapa típica encontrada en el excremento. En infecciones severas, huevos, larvas, y gusanos aún adultos pueden ser encontrados en el excremento.
En el diagnóstico específico de C. hepatica la infección está basada en la presencia de los gusanos adultos y/o huevos en el tejido de hígado en la biopsia o la autopsia. (Nota: la identificación de huevos de C. hepatica en el ano es un encuentro falso, que no es resultado de la infección del humano, debido a que esto se debe a la ingestión de multitud de hígados de animales infectados).
El diagnóstico específico de C. aerophila está basado en huevos que se manifiestan en el ano o en la biopsia pulmonar.
Tratamiento
La medicina de opción es mebendazol, y albendazol es una alternativa.
Profilaxis
Como muchas veces no hay tratamiento contra capillaria, el mejor control se logra por medio de medidas preventivas. Algunas drogas, administradas en bajas dosis pueden servir para disminuir altos niveles de infección en granjas donde haya problemas. Las aves de caza deben criarse sobre alambre para evitar infecciones. Algunas especies de capillaria tienen un ciclo de vida indirecto, y habrá que dirigir las medidas de control hacia los huéspedes intermediarios. Se puede usar higromicina en el control, y resulta valiosa la adición de Vitamina A.
Epidemiología
Capillaria philippinensis es endémico en Filipinas y también ocurre en Tailandia. Casos raros han sido relatados de otros países asiáticos, el Oriente Medio, y Colombia. Los casos raros de infecciones humanas con C. hepatica y C. aerophila han sido relatados por todo el mundo.
- 1 -
Descargar
| Enviado por: | Antonio Atencia Melián |
| Idioma: | castellano |
| País: | España |
