Química
Enlaces químicos
Enlaces químicos: el enlace se define como la fuerza que mantiene juntos a grupos de dos o más átomos y hace que funcionen como unidad. Por ejemplo en el agua la unidad fundamental es la molécula H-O-H cuyos átomos se mantienen juntos por dos enlaces O-H. Se obtiene información acerca de la fuerza del enlace midiendo la energía necesaria para romperlo, o sea la energía de enlace.
Existen tres tipos importantes de enlaces que se forman entre los átomos de un compuesto:
1.1 Enlace iónico (o electrovalente): El enlace iónico se forma cuando un átomo que pierde electrones relativamente fácil (metal) reacciona con otro que tiene una gran tendencia a ganar electrones (no metal).
Ejemplo: Na + Cl = NaCl
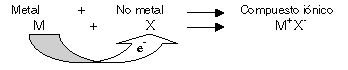
Propiedades:
-
No se forman moléculas aisladas, sino redes cristalinas. Para separar los iones de la red se requiere bastante energía.
-
Son sólidos no conductores. (Cargas estáticas en la red).
-
Elevado punto de fusión.
-
Duros y quebradizos.
* Se llama valencia iónica de un elemento al número de electrones que gana o que pierde al enlazarse iónicamente.
Enlace covalente : El enlace covalente, se dará entonces entre átomos de similar EN (afinidad por los electrones), compartiendo pares de electrones (aportando al par un electrón cada átomo), en número necesario para que cada átomo disponga después de establecido el enlace de 8 electrones en la última capa (recordar que 8 electrones en la última capa proporciona la máxima estabilidad posible para un átomo). Si los átomos que se unen formando este tipo de enlace son iguales se llamará enlace covalente homonuclear y si son diferentes se llamará enlace covalente heteronuclear.
Ejemplo:
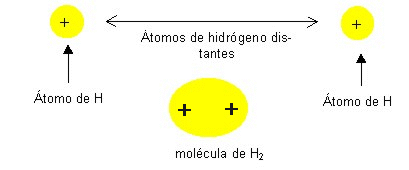
-
Se llama valencia covalente de un elemento al número de electrones compartidos cuando se forma este tipo de enlace.
-
La polaridad de un enlace se mide con el momento dipolar (producto de la carga localizada por la distancia entre los núcleos de los átomos que forman el enlace; una unidad para medir los momentos dipolares es el Debay, los momentos dipolares oscilan de 0 a 11 Debyes).
-
Los Cristales covalentes: son compuestos covalentes formados por redes gigantes, no por moléculas aisladas.
Enlace metálico: Los electrones de valencia de cada átomo pasan a un "fondo común", formando una nube electrónica que rodea a los iones positivos que integran la red metálica.
Propiedades:
- La estructura comentada puede explicar las propiedades claramente.
-Alta conductividad térmica y eléctrica, los electrones pueden moverse con libertad por la nube electrónica.
-Son dúctiles (factibles de hilar) y maleables (factibles de hacer láminas), su deformación no implica una rotura de enlaces ni una aproximación de iones de igual carga, como ocurría en los compuestos iónicos por ejemplo.
-Los puntos de fusión son moderadamente altos, la estabilidad de la red positiva circundada por la nube de electrones es alta.
-Son difícilmente solubles en cualquier disolvente, por el mismo motivo que justifica el punto anterior. (Pensar en la forma de "atacar" el agua a un compuesto iónico, en un metal que es "un todo uniforme" no existe esa posibilidad.
2. Regla del octeto y estructura de Lewis: A inicios del siglo XX, en 1916, de manera independiente, los científicos Walter Kossel y Gilbert Lewis concluyeron que la tendencia que poseen los átomos de lograr estructuras similares a las del gas noble más cercano explica la formación de los enlaces químicos. Esta conclusión es mundialmente conocida como la Regla del Octeto y se enuncia de la siguiente manera:
“Cuando se forma un enlace químico los átomos reciben, ceden o comparten electrones de tal forma que la capa más externa de cada átomo contenga ocho electrones, y así adquiere la estructura electrónica del gas noble más cercano en el sistema periódico”.
No obstante, hay muchas excepciones a esta regla y hasta se han logrado sintetizar algunos compuestos de los gases nobles. La estructura de Lewis permite ilustrar de manera sencilla los enlaces químicos, en ella, el símbolo del elemento está rodeado de puntos o pequeñas cruces que corresponden al número de electrones presentes en la capa de valencia.
2.1 Parámetros a considerar en una estructura de Lewis.
-
Escribe el número total de electrones de valencia.
-
Considera que cada enlace se formará a partir de dos, y solo dos, electrones.
-
Cada átomo deberá cumplir con la regla del octeto. Excepto el hidrógeno que deberá tener solo 2 electrones para cumplir con la regla del dueto.
3. La tabla periódica: Los primeros trabajos de Mendelejeff datan de 1860 y sus conclusiones fueron leídas 1869 en la sociedad Química Rusa. El mismo resumió su trabajo en los siguientes postulados:
Si se ordenan los elementos según sus pesos atómicos, muestran una evidente periodicidad.
Los elementos semejantes en sus propiedades químicas poseen pesos atómicos semejantes (K, Rb, Cs).
La colocación de los elementos en orden a sus pesos atómicos corresponde a su valencia.
Los elementos más difundidos en la Naturaleza son los de peso atómico pequeño. Estos elementos poseen propiedades bien definidas. Son elementos típicos.
El valor del peso atómico caracteriza un elemento y permite predecir sus propiedades.
Se puede esperar el descubrimiento de elementos aún desconocidos.
En determinados elementos puede corregirse el peso atómico si se conoce el de los elementos adyacentes.
3.1 Ventajas del sistema de Mendelejeff
Corrigió los pesos atómicos y las valencias de algunos elementos por no tener sitio en su tabla de la forma en que eran considerado hasta entonces.
Señaló las propiedades de algunos elementos desconocidos, entre ellos, tres a los que llamó eka-boro, eka-aluminio, y eka-silicio.
En 1894 Ramsy descubrió un gas el que denominó argón. Es monoatómico, no presenta reacciones químicas y carecía de un lugar en la tabla. Inmediatamente supuso que debían existir otros gases de propiedades similares y que todos juntos formarían un grupo. En efecto, poco después se descubrieron los otros gases nobles y se les asignó el grupo cero.
Todos los huecos que dejó en blanco se fueron llenando al descubrirse los elementos correspondientes. Estos presentaban propiedades similares a las asignadas por Mendelejeff.
3.2 Defectos de la tabla de Mendelejeff
No tiene un lugar fijo para el hidrógeno.
Destaca una sola valencia.
El conjunto de elementos con el nombre de tierras raras o escasas (lantánidos) no tiene ubicación en la tabla o es necesario ponerlos todos juntos en un mismo lugar, como si fueran un solo elemento, lo cual no es cierto.
No había explicación posible al hecho de que unos períodos contarán de 8 elementos: otros de 18, otros de 32, etc.
La distribución de los elementos no está siempre en orden creciente de sus pesos atómicos.
En el presente siglo se descubrió que las propiedades de los elementos no son función periódica de los pesos atómicos, sino que varían periódicamente con sus números atómicos o carga nuclear. He aquí la verdadera Ley periódica moderna por la cual se rige el nuevo sistema: "Las propiedades de los elementos son función periódica de sus números atómicos" Modernamente, el sistema periódico se representa alargándolo en sentido horizontal lo suficiente para que los períodos de 18 elementos formen una sola serie. Con ello desaparecen las perturbaciones producidas por los grupos secundarios. El sistema periódico largo es el más aceptado; la clasificación de Werner, permite apreciar con más facilidad la periodicidad de las propiedades de los elementos
He aquí una síntesis clara y muy completa no solo de la construcción de la tabla, sino también de su importancia química.
-
La tabla periódica moderna consta de siete períodos y ocho grupos.
-
PERÍODOS: Cada franja horizontal. Indica la cantidad de niveles de energía en que se hallan distribuidos los electrones de un elemento.
-
GRUPO: Cada franja vertical. Conjunto de elementos ordenados en forma de columnas verticales, que reúnen elementos de propiedades similares, numerados del 1 al 18.
-
FAMILIA: Grupo de elementos que tienen propiedades semejantes.
-
NÚMERO ATÓMICO: número de protones contenidos en el núcleo de un átomo.
-
MASA ATÓMICA: es la relación entre la masa de un elemento con respecto a la unidad de masa atómica. La masa atómica relativa de un elemento expresa, en gramos, la masa que hay de ese elemento por cada 6,02 x 1023 átomos.
-
Los iones son átomos o grupos atómicos que tienen un número de electrones excesivo o deficiente para compensar la carga positiva del núcleo.
-
ELEMENTOS ELECTROPOSITIVOS son aquellos que tienen tendencia a perder electrones transformándose en cationes; a ese grupo pertenecen los metales.
-
ELEMENTOS ELECTRONEGATIVOS son los que toman con facilidad electrones transformándose en aniones; a este grupo pertenecen los metaloides.
La Tabla Periódica es una herramienta usual del químico, su buen uso permite predecir, inteligentemente, las fórmulas químicas, las tendencias de las estructuras electrónicas y en general las propiedades. Las formas de presentación de la Tabla Periódica son incontables, a los grupos se les asigna números diferentes. La American Chemical Society ha propuesto una nueva numeración para los grupos, que va desde el 1 al 18. La Tabla que presentamos se acoge a esa nueva numeración, así como a otros cambios propuestos con relación a la ubicación de los elementos: lutecio, laurencio, lantano y actinio.
4. Metales: Corresponde a los elementos situados a la izquierda y centro de la Tabla Periódica (Grupos 1 (excepto hidrógeno) al 12, y en los siguientes se sigue una línea quebrada que, aproximadamente, pasa por encima de Aluminio (Grupo 13), Germanio (Grupo 14), Antimonio (Grupo 15) y Polonio (Grupo 16) de forma que al descender aumenta en estos grupos el carácter metálico); son elementos en su mayoría sólidos, que poseen brillo metálico, buena conductividad térmica y eléctrica, son dúctiles, maleables y forman iones positivos (cationes) por disociación de sus compuestos en solución, son electro positivos y forman sales, haluros y óxidos.
5. No metales: Los no metales, que son relativamente pocos. Los no metales son los elementos situados por encima de la línea quebrada de los grupos 13 a 17 y del hidrógeno ósea se encuentran el extremo superior derecho de dicha tabla. Son muy frágiles y no pueden estirarse en hilos ni en láminas. Se encuentran en los tres estados de la materia a temperatura ambiente: son gases (como el oxígeno), líquidos (bromo) y sólidos (como el carbono). No tienen brillo metálico y no reflejan la luz. Suelen presentar enlace covalente. Los números de oxidación suelen ser negativos.
6.Metaloides: El término metaloide significa "parecido a un metal" y sirve para agrupar elementos que tienen algunas propiedades de metales y no metales. Los metaloides son elementos que se encuentran en la línea que separa metales y no metales. Esta línea pasa entre el boro y aluminio y acaba entre el polonio y el astato. El aluminio se considera otro metal. El resto de los elementos vecinos a esta línea tienen características intermedias metal-no metal. Los más claros son los cinco que se mencionan a continuación y que se emplean en la fabricación de dispositivos de estado sólido en ordenadores y calculadoras (son semiconductores: pueden conducir la corriente en determinadas condiciones).
7. CONCLUSIONES.
-
El descubrimiento de un gran número de elementos y el estudio de sus propiedades puso de manifiesto entre algunos de ellos ciertas semejanzas. Esto indujo a los químicos a buscar una clasificación de los elementos no solo con objeto de facilitar su conocimiento y su descripción, para las investigaciones que conducen a nuevos avances en el conocimiento de la materia.
-
La orientación y información que nos da este trabajo es de un alto valor para la vida cotidiana y para algunas ramas de nuestra carrera.
-
El recordar la tabla periódica y sus elementos es de suma importancia para nosotros como ingenieros industriales, ya que con ella nos podemos guiar para la mejora de los procesos en las industrias debido a la diversidad e materiales que existen.
BIBLIOGRAFÍA.
Internet.
Autores:
-
Zumdahl, Fundamentos de Química, Mc Graw Hill, Pags.- 99,117 y 335-336.
-
Ramón García-Pelayo y Gross, Larousse Enciclopedia Científica, Larousse, Pags.- 546 y 547.
-
Restrepo Fabio y Vargas Leonel, Química Básica, Bedout, Pags.273 - 279.
-
Masterton William y Slowinski Emil, Química General Superior, Interamenricana, Pags- 135-164, 179-189, 192
-
Whitten, K.W. y Gailey, K. D., Química General, Interamericana.
http://www.geocities.com/Colosseum/Loge/3802/loseementosl.html
http://www.adi.uam.es/docencia/elementos/spv21/sinmarcos/elementos/familias.html
INDICE.
PAG
INTRODUCCION. 0
Enlaces químicos 1
Enlace iónico (o electrovalente) 1
Enlace covalente 2
Enlace metálico 3
2. Regla del octeto y estructura de Lewis 3
2.1 Parámetros a considerar en una estructura de Lewis. 4
3 La tabla periódica 4
3.1 Ventajas del sistema de Mendelejeff 5
3.2 Defectos de la tabla de Mendelejeff 6
4 Metales. 8
5 No metales. 9
6 Metaloides 9
7. Conclusiones. 10
BIBLIOGRAFÍAS 11
TRABAJO DE CONSULTA #1.
LAB. QUÍMICA I.
.
.
En la Asignatura de:
Laboratorio de Química 1.
Universidad Santiago de Cali.
Ingeniería Industrial
Curso 1A
Cali.
INTRODUCCIÓN.
En este trabajo veremos un recuento de lo visto en el bachillerato de conceptos básicos para introducirnos en la química universitaria los cuales hemos visto en dos videos en la primera clase de el profesor Armando Vélez, donde nos dejo para consulta los temas.
A continuación veremos los temas ampliados; los cuales se ha retomado de los videos.
Descargar
| Enviado por: | Aluna |
| Idioma: | castellano |
| País: | Colombia |
