Salud
Diabetes Mellitus tipo II


ESCUELA DE ENFERMERIA
“MADAME CURIE”
INCORPORADA A LA SECRETARIA DE EDUCACION Y CULTURA
TESIS:
DIABETES MELLITUS TIPO II
Que para obtener el Título de
ENFERMERO GENERAL
Octubre de 2009.
INDICE
Índice Páginas
PORTADA............................................................................................. S/N
AGRADECIMIENTO............................................................................. I
DEDICATORIA...................................................................................... II
JURAMENTO DE ENFERMERIA.......................................................... III
ANTECEDENTES................................................................................. 1
INTRODUCCIÓN................................................................................. 3
MARCO DE DESARROLLO YOBJETIVOS ........................................ 5
CAPITULO 1.- Anatomía, Fisiología del Páncreas y Fisiopatología………. 6
CAPITULO 2 - Definición y Etiología de Diabetes Tipo II................... 11
CAPITULO 3 - Complicaciones en la Diabetes Mellitus II..................... 16
CAPITULO 4 - Diagnóstico................................................................... 35
CAPITULO 5 - Tratamiento................................................................... 39
CAPITULO 6 - Cuidados de enfermería ............................................. 61
CAPITULO 7 - Guía de atención enfermera a personas con diabetes.... 64
CONCLUSIONES................................................................................. 67
PROPUESTAS EDUCATIVAS Y DE INVESTIGACIÓN....................... 68
BIBLIOGRAFÍA ..................................................................................... 69
AGRADECIMIENTO
Agradezco a mis maestros que me han ayudado durante toda mi formación profesional, brindándome a través de sus enseñanzas todo un conjunto de conocimientos que me han servido como base fundamental para el desarrollo de esta loable labor de enfermería.
Agradezco también al Dr. Eliseo y a su esposa, por sus consejos y todo su apoyo incondicional para la culminación de este importante trabajo.
Un sincero agradecimiento a todas las personas que me apoyaron y motivaron a través de sus consejos y palabras de aliento, que me han servido hoy por hoy para continuar luchando por mis sueños.
DIOS LOS BENDIGA......
DEDICATORIA
Dedico esta tesis a mi Dios Padre Todopoderoso que me dio la oportunidad nuevamente de pisar un aula y que con este trabajo poder conseguir mi formación como Enfermero General.
A mis profesores que me enseñaron lo mejor de ellos, a la Escuela de Enfermería Madame Curie, a mis hermanos y a mi madre por creer en mí.
A mis compañeros que compartieron conmigo esta experiencia y en especial, a la persona más importante en mi vida, por su paciencia, cariño, apoyo y tanto amor, a mi esposa, gracias por todo.
JURAMENTO DE ENFERMERIA
Juro Solemnemente delante de Dios
Y en presencia de esta asamblea,
Llevar una vida pura y dedicada con
Toda fidelidad a la práctica de mi oficio.
Me abstendré cuanto sea
Dañoso y nocivo y no suministraré
Nunca un medicamento perjudicial.
Haré todo lo posible para dignificar mi profesión
Guardando celosamente los asuntos personales
Que se me comuniquen confidencialmente
Así como los secretos familiares que me lleguen
A mi conocimiento por razones de mi oficio.
Me esforzare por ayudar
Al medico en su trabajo y me consagrare
A procurar el bienestar de las personas
Encomendadas a mi cuidado.
ANTECEDENTES
La Diabetes Mellitus es una de las enfermedades crónico-degenerativas que se presentan con mayor frecuencia en la población mundial, al grado de ser considerada una pandemia con tendencia ascendente.
En la actualidad, de acuerdo a la organización mundial de la salud, se estima que existen alrededor de 140 millones de personas con diabetes mellitus en el mundo, y se espera que esa cifra se eleve a 300 millones en los próximos 25 años. El aumento será de 40% en los países desarrollados y de 70% en los países en vías de desarrollo.
En 1995, México contaba con 3.8 millones de adultos con diabetes mellitus y ocupaba el noveno lugar dentro de los diez países con mayor numero de personas con diabetes; para el año 2025, se prevé alcance los 11.7 millones y pase a ocupar el séptimo lugar en orden de frecuencia. En América latina existen 20 millones de personas con diabetes mellitus, considerando que aproximadamente la mitad de los casos de diabetes mellitus tipo 2 son asintomático, existe una alta probabilidad que de no implementarse medidas de intervención parta anticiparse a la aparición del daño, el numero de casos se duplicara en los próximos 10 años.
Estas tendencias son el resultado de la transición demográfica en la población, como por los cambios que se están dando en los patrones culturales, que a su vez, repercuten en la alimentación y el estilo de vida de las personas.
Algunos estudios realizados en esta ultima década sobre prevalecía de Diabetes Mellitus tipo 2 en población urbana y rural en México, van de un rango de 0% a 9.8%.
Actualmente en el estado de Coahuila México hay una alta incidencia de casos por el tipo de alimentación ya que se consumen mucho las harinas y las comidas altas en grasas.
Por tanto, el objetivo de este importante trabajo, es presentar al equipo multidiciplinario de Salud, principalmente al personal de enfermería, esta información actualizada sobre el diagnóstico, tratamiento y prevención de la diabetes mellitus, en el aspecto médico; epidemiológico, terapéutico, y de prevención de alteraciones secundarias, con el convencimiento de que la educación, junto con el ejercicio y la nutrición adecuada, modificarán las actuales perspectivas. Así mismo se plantearán las bases para enfrentar los retos que esta enfermedad representa, de cara al nuevo milenio.
INTRODUCCIÓN
La Diabetes Mellitus Tipo II, es un síndrome heterogéneo de elevada frecuencia, abarca cerca de 90% del total de diabéticos. Su prevalencia se ha incrementado y se incrementara aun mas debido fundamentalmente a las modificaciones socioculturales inducidas por la urbanización (básicamente relacionadas con el incremento paralelo de la prevalencia de obesidad y por el progresivo envejecimiento poblacional).
Es causa de altos índices de morbimortalidad, encontrándose entre las 10 primeras causas, particularmente en la población mayor de 45 años de edad. La prevalencia aumenta con la edad, la obesidad, las dislipidemias y los antecedentes familiares de diabetes. Esta fuertemente asociada con la hipertensión arterial y enfermedad cardiovascular.
Las personas con diabetes tienen una esperanza de vida reducida y una mortalidad dos veces mayor que la población general. Una mejoría en el cuidado de la diabetes aumentaría la esperanza de vida de estas personas, pero esto a su vez, llevaría a una mayor incidencia de complicaciones crónicas microvasculares (nefropatía y retinopatía) y macrovasculares (enfermedades coronarias, cerebro-vasculares y vasculares periféricas), ya que la edad y la duración de la diabetes son los principales factores de riesgo no controlables para el desarrollo de estas complicaciones. Por lo que es necesario aplicar los conocimientos existentes y desarrollar tecnologías capaces de prevenir la aparición de la enfermedad y de sus complicaciones.
Por lo cual he estructurado este importante trabajo de la siguiente manera:
CAPITULO 1.- AnatomíA, Fisiología del Páncreas y Fisiopatología
CAPITULO 2 - Definición y Etiología de Diabetes Tipo II
CAPITULO 3 - Complicaciones en la Diabetes Mellitus Tipo II
CAPITULO 4 - Diagnóstico
CAPITULO 5 - Tratamiento
CAPITULO 6 - Cuidados de enfermería
CAPITULO 7 - Guía de atención enfermera a personas con diabetes.
Conclusiones
Propuestas educativas y de investigación
Bibliografía
MARCO DE DESARROLLO
Esta investigación se realizo a través de una revisión bibliográfica minuciosa de material obtenido en las bibliotecas del Hospital General de Zona # 11 y de la Unidad de Medicina Familiar 79 del Instituto Mexicano del Seguro Social, así como de referencias personales de personas diabéticas y sus familiares. Además se hicieron consultas de algunas paginas de Internet para complementar dicha información.
OBJETIVO GENERAL:
Proporcionar al cuerpo multidisciplinario de salud una herramienta de consulta basada en la bibliografía mas reciente, Con el fin de conocer la etiología, signos y síntomas del paciente con Diabetes Tipo II, de todos los cuidados de enfermería, así como la orientación al familiar, saber las técnicas y manejo del paciente diabético. hábitos de alimentación , explorar el nivel de conocimientos y autocuidado e identificar los niveles de glicemia inicial y final para un mejor control.
OBJETIVOS ESPECIFICOS
Evaluará el conocimiento de la diabetes tanto del paciente como de sus familiares.
Medirá el conocimiento del paciente diabético y familiares respecto a las posibles complicaciones de la enfermedad.
Evaluará las técnicas de autocuidado en el paciente diabético.
Conocerá el nivel de conocimientos del equipo de salud sobre la Diabetes Mellitus Tipo II, la dieta, su adherencia y cual es su relación con el control glicémico en pacientes diabéticos.
CAPITULO 1. ANATOMIA, FISIOLOGIA DEL PANCREAS Y FISIOPATOLOGIA
El páncreas es un órgano aplanado, localizado hacia atrás ligeramente abajo del estomago.
Páncreas. Se puede clasificar como glándula endocrina y glándula exocrina. El páncreas del adulto consiste en una cabeza, un cuello y una cola. La proporción endocrina del páncreas, consiste en un millón de acumulos de células que se denominan Islotes Pancreáticos o Islotes de Langerhans. Hay tres tipos de células que se encuentran en estos agrupamientos.
-
Célula alfa, las cuales secretan la hormona glucagón, que aumenta la concentración de azúcar en la sangre.
-
Células beta, las cuales secretan la hormona insulina que disminuye la concentración de azúcar en la sangre.
-
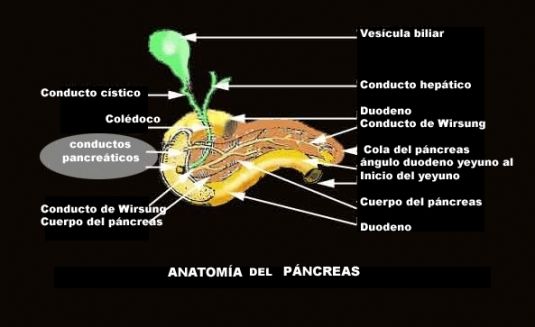
Células delta, las cuales secretan la hormona inhibidora del crecimiento, somatostatina. Esta hormona inhibe la secreción de la insulina y el glucagón.
Figura 1.- Anatomía del Páncreas.
Los islotes están infiltrados por capilares sanguíneos y rodeados de agrupamientos de células que reciben el nombre de acinos, que forman la parte exocrina de la glándula.
El glucagón y la insulina son las secreciones endocrinas del páncreas y se relacionan con la regulación de concentración de azúcar en la sangre.
Glucagón. El producto de las células alfa es el glucagón, una hormona cuya principal actividad fisiológica es aumentar la concentración de azúcar en la sangre. El glucagón logra esto por medio de la aceleración de la conversión glucógeno en el hígado hacia glucosa (glucogenolisis) y de la conversión en el hígado de otros nutrientes, tales como aminoácidos, gliserol y ácido láctico.
El hígado entonces libera la glucosa hacia la sangre y aumenta las concentraciones de azúcar sanguínea. La secreción del glucagón, esta directamente controlada por las concentraciones de azúcar en la sangre por medio de un sistema de retroalimentación negativa. Cuando las concentraciones de azúcar en la sangre disminuyen por debajo de los valores normales los elementos sensibles químicamente en las células alfa de los islotes estimulan a la célula para secreten glucagón. Cuando la azúcar de la sangre aumenta, las células ya no se estimulan y se suspende la producción. Si por alguna razón el instrumento de retroalimentación falla y las células alfa secretan glucagón continuamente, pueden aparecer hiperglucemia. El ejercicio y las comidas (con alto contenido proteico absoluto) aumentan las concentraciones de aminoácidos en la sangre pueden hacer que se provoque un aumento en la secreción de glucagón.
Insulina. Las células beta de los islotes producen la hormona insulina, la cual actúa para disminuir las concentraciones de glucosa en la sangre. Su principal acción fisiopatológica, es opuesta a la del glucagón. Esta se presenta de varias maneras: Acelera el transporte de glucosa desde la sangre hacia las células, en especial las fibras del músculo esquelético. La glucosa que entra hacia las células depende de la presencia de receptores en la superficie de las células blanco, también aceleran la conversión de glucosa a glucógeno, también disminuye la glucogenolisis y la gluconeogenesis, estimula la conversión de glucosa o de otros nutrientes o de ácidos (lipogénesis) y ayuda a estimular la síntesis de proteínas.
La regulación de la secreción de insulina al igual que la secreción de glucagón esta directamente determinada por la concentración de azúcar en la sangre.
FISIOPATOLOGIA
En 1979 la American Diabetes Association (ADA) publicó una clasificación de la diabetes. Dado que la etiología de esta enfermedad es poco conocida, se le clasificó según su tratamiento. Los dos tipos principales son el tipo I o Diabetes Mellitus Insulino-Dependientes (DMID) y el tipo II o no Insulino-Dependiente (DMNID).
Diabetes “SOBRE FLUJO” mellitus. “meli-miel”. Es un trastorno del páncreas caracterizado por la presencia de glucosa en la orina.
En la diabetes tipo II, hay 2 aspectos principales relacionados con la insulina: resistencia insulínica y alteración de la secreción de insulina. La resistencia insulínica es la disminución de la sensibilidad de los tejidos a la insulina. Normalmente, la insulina se fija a los receptores especiales de las superficies celulares por lo que aparece una serie de reacciones en el metabolismo de la glucosa dentro de la célula. La resistencia se acompaña de disminución de estas reacciones intracelulares, por lo que la insulina se vuelve menos eficaz para estimular la captación de glucosa por los tejidos.
Para superar la resistencia insulínica y evitar la formación gradual de glucosa en sangre, debe aumentarse la cantidad de insulina secretada. En las personas con intolerancia a la glucosa, esto se debe a una secreción excesiva de insulina; el nivel de glucosa es normal o ligeramente elevado.
Sin embargo, si las células beta son incapaces de continuar con la creciente demanda de insulina, la leucemia se eleva y se desarrolla diabetes tipo II.
La diabetes tipo II es más común en obesos mayores de 30 años de edad, debido a la intolerancia progresiva lenta (por años) a la glucosa, el inicio de la diabetes tipo II, quizá pase inadvertido por muchos años.
Si se experimentan síntomas por lo regular son ligeros e incluyen fatiga, irritabilidad, poliuria, polidipsia y heridas en la piel que cicatrizan mal, infecciones vaginales o visión borrosa (sí la glucemia es muy alta). En la mayoría de los pacientes (cerca del 75%), la diabetes tipo II se descubre de manera incidental cuando se realizan pruebas de laboratorio sistémicas.
Las consecuencias de la diabetes no descubierta durante muchos años son las complicaciones a largo plazo por ejemplo: Oculopatias, Neuropatias periféricas, Basculopatias periféricas, las cuales se desarrollan antes de efectuar él diagnostico real de diabetes.
Debido a que la resistencia insulínica se relaciona con obesidad, el tratamiento básico de la diabetes tipo II consiste en que el paciente baje de peso.
CAPITULO 2. DEFINICION Y ETIOLOGÍA DE DIABETES TIPO II.
La diabetes es un conjunto heterogéneo de alteraciones, caracterizadas por la elevación de la concentración de glucosa en la sangre, o hiperglucemia. Normalmente, en la sangre circula cierta cantidad de glucosa, la cual se forma en el hígado a partir de los alimentos ingeridos. La insulina, hormona producida por el páncreas, controla la concentración de glucosa en la sangre al regular su producción y almacenamiento.
En la diabetes se reduce la capacidad del cuerpo para responder a la insulina, o el páncreas deja de producirla. Lo anterior conduce a la hiperglucemia, que puede resultar en complicaciones metabólicas graves, como la cetaocidosis diabética y el síndrome hiperosmolar o cetronico (hyperglycemic hyperosmolar nonketotic, HHNK). La hiperglucemia de larga duración es una de las causas de complicaciones macrovasculares crónicas (padecimientos renales y de los ojos) hay complicaciones neuropátias (enfermedades de los nervios). La diabetes también esta relacionada con una mayor presencia de enfermedades macrovaculares, entre otras, infarto al miocardio, apoplejía y vasculopatía periférica. Las características se resumen de la siguiente forma:
| Tipo I, diabetes mellitus insolino-dependiente. (DMID). Tipo II, diabetes mellitus no insulino-dependiente. (DMNID) | Diabetes juvenil (DJ) diabetes de inicio juvenil (DIJ) Diabetes cetogena Diabetes lábil. Diabetes del adulto (DA). Diabetes de la edad adulta Diabetes ceto-resistente Diabetes estable. | Los pacientes no producen, o producen poca, insulina endogena. Necesitan inyecciones de insulina para prevenir la cetoacidosis y mantener la vida. Suele producirse el inicio de forma súbita en niños menores de 15 años, aunque puede aparecer en cualquier edad. El inicio suele producirse después de una infección vicia. Parece probable una disposición cromosoma, aunque la incidencia familiar no es tan frecuente como en el tipo II. Los pacientes no pueden utilizar la insulina producida, en cantidades normales, por su propio organismo. Este grupo forma la gran mayoría de pacientes diabéticos. Suele iniciarse a partir de los 40 años, presentando un importante historial familiar de diabetes. Suele ser obesos. El riesgo de presentar diabetes tipo II aumenta con la edad. Las mujeres tienen un riesgo mayor, independientemente de la edad. Las personas con diabetes tipo II raramente presentan cetosis, excepto en casos de estrés o infección. Estos pacientes pueden presentar diabetes tipo II durante años y pasar progresivamente a ser insulino-dependientes. |
Etiología
Los mecanismos exactos que conducen a la resistencia insulinica y a la alteración de la secreción de insulina en la diabetes tipo II se desconocen hasta este momento. Se considera que los factores genéticos participan en el desarrollo de la resistencia a la insulina. Además, se sabe que hay ciertos factores de riesgo aunados al desarrollo de diabetes tipo II que son:
-
Personas mayores de 40 años
-
Obesidad
-
Antecedentes de Diabetes Mellitus en familiares de primer grado de consanguinidad
-
Mujeres con antecedentes de hijos macrosómicos (más de 4Kg ó 9 libras)
-
Menores de 50 años portadores de enfermedad coronaria
-
Dislipidémicos
-
Pacientes con hipertensión arterial
MANIFESTACIONES CLINICAS.
-
Perdida de peso. (en ocasiones voluntaria).
-
Debilidad y fatiga.
-
Visión borrosa.
-
La vulvovaginitis y el prurito.
-
Glucosuria.
-
Cetonuria. (presencia de cuerpos cetónicos en orina).
-
Elevación de la glucemia en mas de una ocasión por encima de 120 mg/dl, ya sea sangre venosa o capilar.
-
Hemoglobina glucosilada.
-
Poluria.
-
Polidipsia.
-
Polifagia.
-
Hipertencion e insuficiencia renal.
-
Evidencias de patología periférica de las extremidades inferiores.
-
Predisposición a las infecciones.
-
Impotencia en el varón.
-
Neurópata principalmente en manos, pies, piernas y cabeza.
-
Falta de sensibilidad al frío y al calor.
-
Sensación de hormigueo y adormecimiento de los miembros.
-
Embarazos complicados.
-
Trastornos cardiovasculares. (la posibilidad de sufrir cardiopatía esquémica y accidentes vasculocerebrales).
Abordaje del riesgo cardiovascular en la Diabetes Mellitus 2
El diabético es un paciente con un riesgo aterogénico elevado y es frecuente que se asocien distintos factores cardiovasculares (FRCV). El diabético siempre presenta una mayor mortalidad de la población general con el mismo número de FRCV, por tanto es imprescindible un abordaje global del riesgo cardiovascular .Existen numerosas evidencias de la relación entre el grado de control glucemico y la presencia de complicaciones macrovasculares y la mortalidad. Los pacientes con intolerancia a la glucosa o glucemia basal alterada presentan un riesgo cardiovascular intermedio entre la población general y la diabética. En ellos es también importante reducir sus FRCV (con intervenciones basadas en la práctica de ejercicio físico regular.Alimentacion equilibrada y abstención tábaquica). Para la toma de decisiones de tratamiento farmacológico en prevención primaria de la cardiopatía isquemica (CI) es muy útil las tablas de Framingham para el cálculo del riesgo de sufrir un episodio coronario a los 10 años, en función de variables como la edad, el sexo la hipercolesterolemia, la diabetes mellitus y la hipotensión arterial.
Antes de aparecer la diabetes, los pacientes suelen perder la respuesta secretora inicial de insulina a la glucosa y pueden secretar cantidades relativamente grandes de proinsulina. En la diabetes establecida, aunque los niveles plasmáticos de insulina en ayunas pueden ser normales o incluso estar aumentados en los pacientes con DM tipo II, la secreción de insulina estimulada por la glucosa está claramente disminuida. El descenso de los niveles de insulina reduce la captación de glucosa mediada por la insulina y deja de limitar la producción de glucosa hepática.
La hiperglucemia puede ser no sólo una consecuencia, sino también una causa de un mayor deterioro de la tolerancia a la glucosa en el paciente diabético (toxicidad de la glucosa), porque la hiperglucemia reduce la sensibilidad a la insulina y eleva la producción de glucosa en el hígado. Una vez que mejora el control metabólico del paciente, la dosis de insulina o de fármaco hipoglucemiante se puede reducir generalmente.
Algunos casos de DM tipo II se producen en adolescentes jóvenes no obesos (diabetes de inicio en la madurez en personas jóvenes. En estos pacientes se han demostrado alteraciones en la secreción de insulina y en la regulación de la glucosa hepática.
Diabetes atribuida a una enfermedad pancreática.
La pancreatitis crónica, particularmente en los alcohólicos, se asocia a menudo a diabetes. Estos pacientes pierden tanto islotes secretores de insulina como islotes secretores de glucagón. En consecuencia pueden estar moderadamente hiperglucémicos y sensibles a dosis bajas de insulina. Dada la falta de una contrarregulación efectiva (insulina exógena que no es antagonizada por el glucagón) padecen a menudo de una rápida aparición de hipoglucemia. En Asia, África y el Caribe se observa con frecuencia DM en pacientes jóvenes intensamente malnutridos con una grave deficiencia de proteínas y una enfermedad pancreática; estos pacientes no tienen tendencia a la CAD, pero pueden necesitar insulina.
Diabetes asociada a otras enfermedades endocrinas.
La DM tipo II puede ser secundaria a síndrome de Cushing, acromegalia, feocromocitoma, glucagonoma, aldosteronismo primario o somatostatinoma. La mayoría de estos trastornos se asocian a resistencia a la insulina periférica o hepática. Muchos pacientes se harán diabéticos en cuanto disminuya también la secreción de insulina. La prevalencia de la DM tipo I es mayor en ciertas enfermedades endocrinas autoinmunitarias, por ejemplo, enfermedad de Graves, tiroiditis de Hashimoto y enfermedad de Addison idiopática.
Diabetes resistente a la insulina asociada a la acantosis nigricans.
Síndromes de resistencia a la insulina tipos A y B). Existen dos raros síndromes debidos a una notable resistencia a la insulina en el receptor insulínico asociados a la acantosis nigricans. La acantosis nigricans es una hiperpigmentación aterciopelada del cuello, las axilas y la ingle y probablemente es la manifestación cutánea de una hiperinsulinemia intensa y crónica. El tipo A se debe a alteraciones genéticas en el receptor insulínico. El tipo B es producido por anticuerpos circulantes contra el receptor insulínico y puede asociarse con otras manifestaciones de enfermedad autoinmunitaria.
Diabetes lipoatrófica.
Es éste un raro síndrome en el cual la DM resistente a la insulina se asocia con una desaparición simétrica extensa o prácticamente completa del tejido adiposo subcutáneo. Se ha relacionado con alteraciones genéticas en el receptor de insulina.
CAPITULO 3. COMPLICACIONES EN LA DIBETES MELLITUS II.
La DM tiene varias formas de presentación iniciales. La DM tipo I se presenta generalmente con hiperglucemia sintomática o CAD. La DM tipo II puede presentarse con hiperglucemia o CHHNC, pero se diagnostica con frecuencia en pacientes sintomáticos durante una exploración médica de rutina o cuando el paciente presenta manifestaciones clínicas de una complicación tardía.
Después del comienzo agudo de una DM tipo I suele existir una notable secreción de insulina. Los pacientes con una DM tipo I pueden disfrutar de un período de luna de miel caracterizado por una larga fase de niveles de glucosa casi normales sin ningún tratamiento.
Los síntomas iniciales son poliuria, náuseas, vómitos y, especialmente en los niños, dolor abdominal. La letargia o somnolencia es de aparición frecuentemente más tardía. En los pacientes no tratados puede progresar a coma. Un pequeño porcentaje de pacientes se presentan en coma. En los pacientes sin historia de DM tipo I puede no pensarse al principio en una CAD, porque el paciente puede no mencionar espontáneamente una historia de poliuria. La CAD puede confundirse con un abdomen agudo quirúrgico en los niños por el dolor abdominal intenso y la presencia de leucocitosis. En una CAD sin complicaciones la temperatura del paciente suele ser normal o baja. Generalmente existen signos de deshidratación y algunos pacientes están hipotensos. Puede haber respiración de Kussmaul (un patrón característico de respiraciones profundas y lentas) y puede detectarse acetona en el aliento.
Hiperglucemia sintomática.
Se produce poliuria seguida de polidipsia y pérdida de peso cuando los niveles elevados de glucosa plasmática causan una glucosuria intensa y una diuresis osmótica que conduce a deshidratación. La hiperglucemia puede causar también visión borrosa, fatiga y náuseas y llevar a diversas infecciones fúngicas y bacterianas. En la DM tipo II, la hiperglucemia sintomática puede persistir días o semanas antes de que se busque atención médica; en las mujeres, la DM tipo II con hiperglucemia sintomática suele asociarse con prurito debido a candidiasis vaginal.
Complicaciones tardías.
Las complicaciones tardías aparecen tras varios años de hiperglucemia mal controlada. Los niveles de glucosa están aumentados en todas las células, a excepción de donde existe una captación de glucosa mediada por la insulina (sobre todo en el músculo), produciéndose un aumento de la glicosilación y de la actividad de otras vías metabólicas, que puede ser causada por las complicaciones. La mayoría de las complicaciones microvasculares pueden retrasarse, prevenirse o incluso invertirse mediante un control estricto de la glucemia, es decir, consiguiendo niveles de glucosa en ayunas y posprandiales próximos a la normalidad, que se reflejan en concentraciones casi normales de hemoglobina glucosilada (Hb A1C). Una enfermedad microvascular como la aterosclerosis puede producir síntomas de arteriopatía coronaria, claudicación, erosión de la piel e infecciones. Aunque la hiperglucemia puede acelerar la aterosclerosis, los muchos años de hiperinsulinemia que preceden a la aparición de la diabetes (con resistencia a la insulina) pueden representar el principal papel iniciador. Sigue siendo frecuente la amputación de un miembro inferior por vasculopatía periférica grave, claudicación intermitente y gangrena. El antecedente de una retinopatía simple (las alteraciones iniciales de la retina que se observan en la exploración oftalmoscópica o en fotografías de la retina) no altera la visión de manera importante, pero puede evolucionar a edema macular o a una retinopatía proliferativa con desprendimiento o hemorragia de la retina, que pueden causar ceguera. Alrededor de un 85% del total de diabéticos desarrollan con el tiempo algún grado de retinopatía (Retinopatía diabética).
Complicación más frecuente pie diabético.
La epidemiología del pié diabético es aún desconocida ya que engloba distintas condiciones patológicas y en los distintos trabajos publicados no existe una clasificación y descripción uniformes.
En el consenso publicado por la Sociedad Española de Angiología y Cirugía Vascular se define el pie diabético como una "alteración clínica de base etiopatogénica neuropática e inducida por la hiperglucemia mantenida, en la que con o sin coexistencia de isquemia, y previo desencadenante traumático, produce lesión y/o ulceración del pie".
Desde un punto de vista práctico, nos ha resultado de utilidad etiquetar como pie diabético, todas aquellas lesiones que los diabéticos presentan en las extremidades inferiores y algunas de ellas no siempre entran en esta definición. Este enfoque, aunque pueda parecer que sobreestima las lesiones, es útil para el médico general, ya que una herida aparentemente sin importancia puede comportarse de una forma muy virulenta en el diabético. Hemos tenido casos en que no hemos podido demostrar componente neuropático ni isquémico predominando el componente infeccioso. En otros casos, la gangrena de un dedo se presenta sin desencadenante traumático. Preferimos clasificar nuestros pacientes según el componente predominante que produce la lesión: neuropatía, enfermedad vascular periférica e infección, sabiendo de antemano que en la mayoría de los casos existirá una participación de más de uno de ellos.
Polineuropatía periférica.
La neuropatía periférica es una complicación frecuente de la DM tanto de tipo I como en la de tipo II, y su incidencia aumenta de forma paralela a la duración y severidad de la hiperglucemia. Es raro que ocurra en diabéticos de menos de 5 años de evolución, aunque en pacientes con DM tipo II al existir periodos largos de hiperglucemia asintomáticos, este tiempo de presentacion puede ser más corto. Prácticamente todos los diabéticos de más de 10-15 años de evolución tienen alguna evidencia de neuropatía, afectando en nuestro país a casi el 23% de los mismos. La neuropatía sensorial hace que el pie se vuelva insensible ante estímulos normalmente dolorosos. Las personas no diabéticas cambian la posición del pie cuando presentan disconfort al caminar, sin embargo el sujeto diabético con neuropatía puede pasar todo el día con un cuerpo extraño dentro del calzado sin darse cuenta.
La neuropatía motora produce una atrofia de los músculos intrínsecos del pie y además un adelgazamiento de la almohadilla grasa que se encuentra situada bajo las cabezas de los metatarsianos. Esto produce deformidades como "dedos en martillo", "dedos en garra" o hallux valgus que predisponen al traumatismo y la ulceración. La neuropatía autónoma disminuye la sudoración del pie y produce una piel seca y con intensa hiperqueratosis y grietas que constituyen puertas de entrada a la infección.
Por otro lado, la afectación de los nervios simpáticos, una auténtica "autosimpatectomía", produce una vasodilatación que ocasiona un aumento de la reabsorción ósea, colapso articular y deformidades cuya máxima expresión la constituye el pie de Charcot (neuroartropatía de Charcot) se encuentran localizadas debajo de la cabeza del primer una presión mantenida en la zona, al metatarsiano y rodeadas de un grueso halo de hiperqueratosis. Se producen debido a adelgazamiento de la almohadilla grasa y a la prominencia ósea por el desequilibrio entre flexores y extensores del dedo. Puede tener una profundidad variable y llegan a afectar al hueso provocando osteomielitis. Dependiendo de la profundidad y afectación de las estructuras subyacentes, la úlcera se clasificará en distintos grados como veremos a continuación.
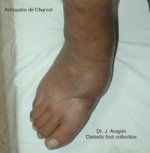
En la Neuroartropatía de Charcot existe una pérdida de la bóveda plantar, un acortamiento del eje antero-posterior del pie, edema importante del mismo y una convexidad medial. Todas estas deformidades predisponen a la ulceración.
Enfermedad vascular periférica
En el clásico estudio de Framinghan quedó establecido que la enfermedad arterial oclusiva tiene una prevalencia cuatro veces mayor en la población diabética que en los que no padecen esta enfermedad. Aunque la enfermedad vascular periférica en los diabéticos es el resultado de una aterosclerosis acelerada en cuya patogenia intervienen distintos factores, es similar a la que presentan las personas no diabéticas.
Típicamente, las lesiones son multisegmentarias tienen una preferencia por las arterias infrageniculares y suele respetar las arterias del pie. Los factores de riesgo asociados al desarrollo de enfermedad vascular periférica son: tabaco, hipertensión arterial, dislipemias, hiperglucemia, hiperinsulinismo, obesidad y microalbuminuria. Estos factores de riesgo deben ser controlados de forma adecuada, ya que por ejemplo la hipertensión arterial se asocia con un incremento en el riesgo de amputación.
Microangiopatía diabética
A nivel de la microcirculación existe un engrosamiento de la membrana basal capilar. Este engrosamiento no es oclusivo y es el cambio estructural dominante en la retinopatía y en la nefropatía. La consecuencia es un aumento de la permeabilidad capilar y un deterioro en la autorregulación del flujo que en el riñón se manifiesta por microalbuminuria y en el ojo por la formación de exudados. En el pie diabético se teoriza que estos cambios pueden dificultar la migración leucocitaria así como la respuesta hiperémica que se produce tras una lesión. Esto facilitaría la infección así como la progresión de la misma.
Infección.
Las causas por las que los diabéticos son tan susceptibles a la infección, no permanecen del todo aclaradas. Experimentalmente, se han encontrado defectos en la función leucocitaria tanto en la quimiotaxis, respuesta fagocítica como en la capacidad de muerte intracelular, pero existen autores que no encuentran evidencias suficientes que demuestren que la respuesta inmune se encuentre dañada en el paciente con DM.
Si dejamos aparte estas controversias, lo que la experiencia clínica sugiere es que los pacientes diabéticos debido a la insuficiencia vascular y a la neuropatía, presentan un riesgo mayor de presentar lesiones en los pies que los individuos no diabéticos y, que una vez que la infección se ha establecido, presenta una mayor gravedad y refractariedad al tratamiento.
La extremidad isquémica no responde a la infección con incremento de la perfusión local, formación de edema e infiltración leucocitaria de la misma forma que la extremidad bien vascularizada. Tampoco los antibióticos llegan al sitio de la infección en una concentración adecuada debido a la inadecuada perfusión tisular.
Aproximación diagnóstica al pie diabético.
Para obtener unos resultados óptimos en el tratamiento del pie diabético, debemos conocer tanto los factores etiopatogénicos que actúan en la producción de las lesiones como la fisiopatología de las mismas. Por ello, difiere notablemente el manejo de una úlcera isquémica, neuropática o mixta. Además la infección se puede añadir a cualquiera de las anteriores o ser por sí misma el factor predominante. Sólo un diagnóstico certero etiológico conducirá a los mejores resultados y a evitar las frustraciones que producen las ulceraciones que evolucionan de forma tórpida a pesar de que los tratamientos locales son considerados adecuados. Una secuencia fácil de realizar es la que mostramos en el algoritmo siguiente.
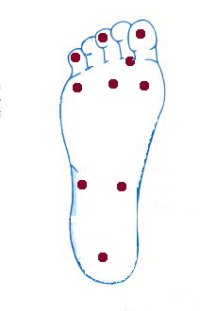
Realizamos la prueba en 10 puntos: primero, tercero y quinto dedos, primera, tercera y quinta cabezas de los metatarsianos, 2 pruebas en el medio pie, una en el talón y otra en el pliegue entre primer y segundo dedos.
Anotamos la presencia de sensibilidad sobre las 10 pruebas realizadas, conociendo que la ausencia de sensibilidad en 4 de los 10 sitios tiene un 97% de sensibilidad y un 83% de especificidad para identificar la pérdida de sensación protectora.
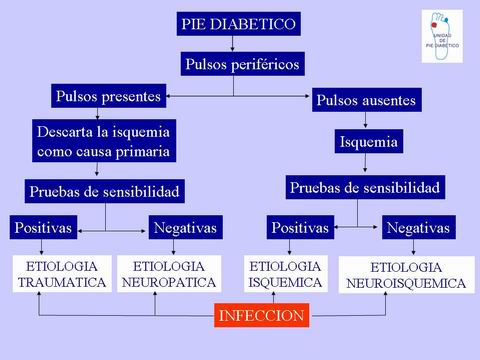
Como hemos reflejado en el algoritmo anterior lo primero que hay que realizar es una palpación de los pulsos en ambas extremidades inferiores del paciente. Una ausencia de pulsos, nos indicará que la isquemia se encuentra implicada en la patogenia de la lesión, aunque el desencadenante sea otro. No siempre es fácil la palpación de los pulsos pedios ya que la presencia de edema o la no compresibilidad de la arteria por calcificación de la misma puede dificultar la maniobra exploratoria.
Nos ayuda a valorar el componente isquémico la inspección del pie: la desaparición del vello del dorso, el engrosamiento y deformidad de las uñas (onicogriposis), la atrofia del tejido celular subcutáneo o el rubor que adopta el pie cuando se encuentra colgando son signos de isquemia.
El paciente también nos puede referir historia de claudicación intermitente o la presencia de dolor en reposo, que suele ser de predominio nocturno y que calma al colgar las extremidades de la cama. No es infrecuente que estas fases de la enfermedad vascular periférica falten en el diabético debido a la presencia de neuropatía concomitante y se presente en nuestra consulta con lesiones gangrenosas en su extremidad.
El estudio mediante Doppler se realiza a continuación y se determinan la presión sistólica en el tobillo así como el índice tobillo/brazo o índice YAO. El estudio Doppler es fácil de realizar y aporta datos de gran importancia para disponer la terapéutica del paciente. Es importante conocer que la frecuente calcificación de la capa media arterial presente en muchos diabéticos puede dar índices tobillo/brazo falsamente elevados aún en presencia de severa enfermedad vascular.
La polineuropatía distal mixta y simétrica constituye la forma más frecuente de neuropatía diabética. La afectación sensitiva, que generalmente predomina sobre la afectación motora, aparece primero en las regiones más distales de la extremidad y progresa hacia las regiones proximales adoptando una distribución "en calcetín".
En nuestro centro utilizamos tres pruebas para explorar la presencia de neuropatía periférica. La percepción de sensibilidad vibratoria mediante un diapasón de 128 Hz, la presencia de reflejo aquíleo mediante el martillo de reflejos y la sensibilidad táctil con los filamentos de Semmes-Weinstein (5.07-10g) para detectar la pérdida de sensibilidad protectora.
El diapasón lo colocamos en la punta de los dedos y en el relieve óseo de la cabeza del primer metatarsiano. El reflejo aquíleo hay que valorarlo con prudencia ya que su ausencia indica neuropatía, pero un reflejo positivo no la descarta.
La sensibilidad con los filamentos de Semmes-Weinstein (5.07-10g) se explora de la siguiente manera. En primer lugar realizamos la prueba en una mano del paciente y le pedimos que cuando sienta el toque del filamento en el pie nos lo comunique. No debe colocarse sobre callosidades ni sobre heridas abiertas. El filamento es empujado en el punto a explorar de forma perpendicular hasta que se dobla que es cuando se realiza la fuerza exacta.
El diagnóstico de infección la mayoría de las veces es fácilmente establecido pero en ocasiones puede suponer un desafío. Es importante conocer los signos y síntomas de infección en el pie del diabético ya que un diagnóstico y tratamiento precoz es la única forma de impedir la progresión del problema séptico y evitar la amputación. Esto se torna aún más importante ante la presencia de una grave infección necrotizante.
En ocasiones existe el antecedente de un traumatismo que puede ser tan pequeño como una rozadura de calzado y en otras el paciente no nos refiere el antecedente traumático simplemente porque no se ha dado cuenta. Los siguientes signos y síntomas deben hacernos sospechar de la presencia de infección en el pie de un diabético. No nos cansaremos de repetir que es necesario un alto índice de sospecha para que el diagnóstico, y consecuentemente el tratamiento, no sean retrasados.
Signos de infección en el pie diabético.
-
GENERALES: Mal control metabólico del paciente, Fiebre, Taquicardia, Leucocitosis persistente, Elevación de la velocidad de sedimentación globular.
-
LOCALES: Herida que desprende mal olor, Presencia de zonas cutáneas con cambio de coloración, Eritema en el pie, Edema del pie, Presencia de linfangitis, Crepitación en los tejidos adyacentes a la herida, Supuración evidente de los bordes de la herida a la presión.
Clasificación del pie diabético.
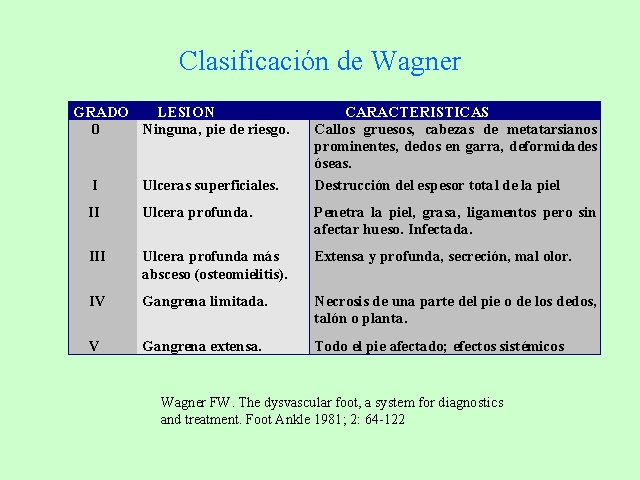
Existen varias clasificaciones para el pie diabético. En nuestra unidad seguimos la clasificación de Wagner que nos ha proporcionado una excelente correlación tanto con el porcentaje de amputaciones como con la morbimortalidad. Conforme las lesiones son de grado superior, aumenta la posibilidad de sufrir una amputación mayor y aumenta asimismo la mortalidad asociada. Una crítica a esta clasificación es que no tiene en cuenta la etiopatogenia de la lesión, pero en realidad los Grados I, II y III se correlacionan con lesiones neuropáticas y los IV y V con lesiones isquémicas.
Tratamiento del pie diabético.
Debido a la complejidad del manejo del pie diabético, el tratamiento por un equipo multidisciplinario es el método más efectivo para alcanzar resultados favorables en una población de alto riesgo. La ubicación del equipo en un centro dedicado de forma exclusiva al manejo de esta patología presenta grandes ventajas con respecto a la organización, comunicación entre profesionales, optimización de recursos y fluidez en el trabajo.
Aunque lo anteriormente expuesto resulta el ideal, el primer escalón diagnóstico y terapéutico al que acude el paciente con pie diabético es al de la asistencia primaria. Es el médico de asistencia primaria quien debe detectar la presencia de la lesión y el factor patogénico implicado en la producción de la misma. Resulta de suma importancia el conocimiento de las siguientes premisas con respecto al tratamiento del pie diabético.
Estamos tratando un paciente diabético con una lesión en el pie. Olvidar esta secuencia y pensar que lo más importante es el problema local, conducirá al fracaso en la cicatrización del proceso. El control metabólico del paciente resulta de suma importancia.
Desconocer la patogenia de una úlcera sólo conduce a un cambio continuo de pomadas, apósitos y tratamientos tópicos que intentan acelerar una curación dificultada por otros factores.
Pie diabético no equivale a pie isquémico. Atribuir a la falta de riego todas las ulceraciones en el pie puede conducir a actitudes fatalistas, falta de confianza en los resultados y amputaciones innecesarias.
El tratamiento postural, reposo, miembros elevados y descargar de presión la zona ulcerosa tienen tanta importancia como una cura bien realizada. El médico responsable del paciente debe inspeccionar las curas de forma regular.
Consideramos fundamental y prioritario el desbridamiento quirúrgico del tejido necrótico o de fragmentos óseos infectados.
La infección debe ser diagnosticada precozmente. Es la clave para poder llevar a cabo un abordaje conservador y evitar las amputaciones. Todos los signos de infección han de ser tenidos en cuenta y valorados de forma evolutiva.
El paciente ha de ser enviado a la asistencia especializada ante las siguientes circunstancias:
INDICACIONES DE ASISTENCIA ESPECIALIZADA
-
Paciente no colaborador
-
Imposibilidad de proporcionar una asistencia domiciliaria adecuada
-
Mal estado general
-
Paciente séptico
-
Descomposición diabética
-
Falta de respuesta al tratamiento en 4-5 días si se ha a realizado de una manera correcta.
-
Gran tumefacción y edema de los pies.
-
Celulitis ascendente
-
Afectación de los espacios profundos del pie.
-
Osteomielitis
-
Infección en un paciente con circulación precaria por el peligro potencial de desarrollo de gangrena.
Desde un punto de vista práctico, podremos tratar de forma ambulatoria las úlceras tipos Wagner I y II.
La realización de una radiografía del pie resulta de suma importancia a la hora de enfocar el tratamiento del pie diabético. Debemos valorar la existencia de cuerpos extraños enclavados, gas en partes blandas debido a la existencia de infección por gérmenes productores de gas y la afectación ósea.
La úlcera neuropática plantar que no presenta sobreinfección, puede ser tratada perfectamente en asistencia primaria. Como hemos referido anteriormente, la úlcera se encuentra rodeada por un grueso borde de hiperqueratosis que debe ser extirpado para conseguir la cicatrización. Las curas locales se realizarán con los distintos medios de curas de que disponemos actualmente.
Antibioterapia oral.
-
Amoxicilina/ Acido Clavulánico
-
Ampicilina/ Sulbactam
-
Ciprofloxacino
-
Ciprofloxacino + Clindamicina
-
Ciprofloxaciono + Metronidazol
Cuando la infección está presente es necesario el uso de antibióticos. Debemos tener presente que la flora presente en estas lesiones es de tipo mixto con gérmenes aerobios y anaerobios. Puede tomarse muestras para cultivo, pero los frotis superficiales no son adecuados y el tratamiento es necesario iniciarlo de forma empírica Como tratamientos por vía oral podemos utilizar los fármacos antibióticos que exponemos en la tabla.
En otras ocasiones, el tratamiento es bastante más complejo y para el control de una infección de tipo necrotizante es necesario realizar grandes desbridamientos quirúrgicos en quirófano. Para alcanzar los objetivos de conservar el pie es necesario conservar el máximo tejido viable posible, pero esto exige un control exhaustivo de las heridas, ya que a veces son necesarios desbridamientos sucesivos con objeto de vencer a la infección.
Por supuesto, en estos pacientes ingresados la antibioterapia se coloca vía parenteral y resulta de suma importancia el control metabólico, hidroelectrolítico y de la patología asociada relacionada que presenta el paciente. .
La neuropatía.
Aparece aproximadamente en 1/3 de los pacientes con DM tipo I y en un porcentaje menor de pacientes con DM tipo II. En los primeros, la TFG puede aumentar inicialmente con la hiperglucemia. Tras unos 5 años de padecer una DM tipo I puede presentarse una albuminuria clínicamente detectable (³300 mg/l) que no tiene explicación por otra enfermedad del tracto urinario. La albúmina anuncia una disminución progresiva de la TFG con una alta probabilidad de desarrollar una nefropatía de fase terminal en 3 a 20 años (mediana, 10 años). La albuminuria es casi 2,5 veces más alta en los pacientes con DM tipo I con PA diastólica >90 mm Hg que en los que tienen PA diastólica <70 mm Hg. Por consiguiente, tanto la hiperglucemia como la hipertensión aceleran la evolución a la nefropatía en fase terminal. La nefropatía diabética suele ser asintomática hasta que se desarrolla la nefropatía en fase terminal, pero puede originar un síndrome nefrótico. La albuminuria y la nefropatía pueden prevenirse o retrasarse con el captopril, un inhibidor de la ECA. A la vez que un tratamiento enérgico de la hipertensión evita el deterioro de la función renal, los inhibidores de la ECA han demostrado sumar beneficios sobre otras clases de antihipertensivos. De hecho, los inhibidores de la ECA evitan la proteinuria en diabéticos hipertensos y no hipertensos. Datos recientes indican que esos fármacos también previenen la retinopatía.
La neuropatía diabética.
Se presenta frecuentemente como una polineuropatía distal, simétrica, de predominio sensitivo que causa déficit sensitivos que se inician y suelen caracterizarse por una distribución en "calcetines y guantes". La polineuropatía diabética puede causar entumecimiento, hormigueos y parestesias en las extremidades y, con menor frecuencia, dolor e hiperestesia intensa y debilitante de localización profunda. Los reflejos aquíleos suelen estar disminuidos o abolidos. Es preciso descartar otras causas de polineuropatía. Las mononeuropatías dolorosas y agudas que afectan a los pares craneales III, IV y VI, así como a otros nervios, como el femoral, pueden aumentar en semanas o meses, se presentan con mayor frecuencia en los diabéticos de edad avanzada y se atribuyen a infartos nerviosos. La Neuropatía del sistema autónomo se presenta principalmente en diabéticos con polineuropatía y puede causar hipotensión postural, trastornos de la sudación, impotencia y eyaculación retrógrada en los varones, deterioro de la función vesical, retardo del vaciamiento gástrico (a veces con un síndrome posgastrectomía), disfunción esofágica, estreñimiento o diarrea y diarrea nocturna. La disminución de la frecuencia cardíaca en respuesta a la Maniobra de Valsalva, o al pasar a la bipedestación, y la ausencia de variación de la frecuencia cardiaca durante la ventilación profunda son signos de neuropatía autonómica en los diabéticos.
Las úlceras de los pies y los problemas articulares
Son causas importantes de patología en la DM. La principal causa predisponente es la polineuropatía diabética; la denervación sensitiva dificulta la percepción de los traumatismos por causas tan comunes como los zapatos mal ajustados o las piedrecillas. Las alteraciones de la sensibilidad propioceptiva conducen a un modo anormal de soportar el peso y a veces al desarrollo de articulaciones de Charcot.
El riesgo de infección por hongos y bacterias.
Aumenta debido a la disminución de la inmunidad celular causada por la hiperglucemia y los déficit circulatorios originados por la hiperglucemia crónica. Son muy frecuentes las infecciones cutáneas periféricas y las aftas orales y vaginales. El proceso inicial puede ser una infección micótica que lleva a lesiones interdigitales, grietas, fisuras y ulceraciones exudativas que facilitan una invasión bacteriana secundaria. Muchas veces los pacientes con úlceras de pie infectadas no sienten dolor a causa de la neuropatía y no tienen síntomas sistémicos hasta una fase posterior con una evolución desatendida. Las úlceras profundas, y en especial las úlceras asociadas con algún grado detectable de celulitis, exigen hospitalización inmediata, dado que puede aparecer toxicidad sistémica e incapacidad permanente. Debe descartarse la osteomielitis mediante gammagrafía ósea. El desbridamiento quirúrgico temprano es una parte esencial del tratamiento, pero a veces es imprescindible la amputación.
Cetoacidosis diabética
Acidosis metabólica por acumulación de cuerpos cetónicos debida a niveles de insulina intensamente disminuidos.
La cetoacidosis diabética (CAD) se debe a una disponibilidad de insulina claramente deficiente, que causa una transición desde la oxidación y el metabolismo de la glucosa a la oxidación y el metabolismo de los lípidos . En los pacientes con DM tipo I, la CAD es desencadenada comúnmente por una omisión del tratamiento insulínico o una infección aguda, un traumatismo o un infarto que hacen insuficiente el tratamiento insulínico habitual. Aunque los pacientes con DM tipo II tienen raras veces CAD, muchos de ellos pueden tener formación de cuerpos cetónicos y acidosis (habitualmente leve) causados por una disminución de la ingesta de alimento y una notable disminución de la secreción de insulina debida a la hiperglucemia intensa y crónica (toxicidad de la glucosa). Estos pacientes no suelen necesitar insulina una vez corregido el episodio metabólico agudo.
En la CAD, la hiperglucemia intensa origina diuresis osmótica, pérdidas urinarias excesivas de agua, Na y K y contracción de volumen con acidosis que conducen a un aumento de la síntesis y la liberación de cuerpos cetónicos en el hígado. Los principales cuerpos cetónicos, ácido acetoacético y ácido b-hidroxibutírico, son ácidos orgánicos fuertes; la hipercetonemia induce una acidosis metabólica y una compensación respiratoria y los intensos aumentos en la excreción urinaria de los ácidos acetoacético y b-hidroxibutírico fuerzan pérdidas adicionales de Na y K. La acetona derivada de la descarboxilación espontánea del ácido acetoacético se acumula en el plasma y es lentamente eliminada por la respiración; la acetona es un anestésico para el SNC, pero la causa del coma en la CAD se desconoce.
La cetogénesis anormal en la CAD se debe a la pérdida del efecto modulador normal de la insulina sobre los ácidos grasos libres (AGL) liberados a partir del tejido adiposo y sobre la oxidación de los AGL y la cetogénesis en el hígado. Los niveles de AGL y la captación de éstos por el hígado están considerablemente aumentados. En el hígado, la insulina regula normalmente la oxidación de los AGL y la cetogénesis mediante la inhibición indirecta del transporte de los derivados de los AGL de cadena larga a través de la membrana mitocondrial interna hacia el interior de la matriz mitocondrial. El glucagón estimula en el hígado el transporte del éster del CoA con el ácido graso de cadena larga y la oxidación y la cetogénesis en las mitocondrias, y en la CAD desaparece el efecto antagónico normal de la insulina. La proporción plasmática entre el ácido b-hidroxibutírico y el ácido acetoacético es normalmente de 3:1 y suele estar aumentada en la CAD, alcanzando a veces la proporción de 8:1.
Las tiras y tabletas reactivas disponibles comercialmente reaccionan con el ácido acidoacético (y débilmente con la acetona), pero no reaccionan con el ácido b-hidroxibutírico. Por consiguiente, las tiras reactivas pueden subestimar considerablemente la cantidad de cuerpos cetónicos presentes.
Cetoacidosis alcohólica
Cetoacidosis que va acompañada con hiperglucemia leve y ausencia de un nivel de alcoholemia elevado.
Este síndrome se atribuye a los efectos combinados de la abstinencia alcohólica y la inanición sobre la secreción endógena de insulina y sobre los estímulos que aumentan la liberación de ácidos grasos libres (AGL) y a la cetogénesis en pacientes que tienen probablemente un deterioro subyacente de la secreción de insulina. Algunos alcohólicos crónicos están predispuestos a episodios de vómitos intensos y dolor abdominal.
La historia característica es la de una borrachera que termina en vómitos y está causada por la interrupción de la ingestión de alcohol o alimentos durante ³24 h. Durante este período de inanición los vómitos continúan y aparece dolor abdominal intenso, lo que induce al paciente a buscar asistencia médica. El grado de hiperglucemia (p. ej., glucosa plasmática <150 mg/dl [<8,33 mmol/l]) convierte claramente en improbable una CAD. Se encuentran signos de pancreatitis en la mayoría de los pacientes y muchos presentan un deterioro de la tolerancia a la glucosa o DM tipo II tras la recuperación del episodio agudo. El tratamiento se inicia con una infusión i.v. de glucosa al 5% en solución de cloruro sódico al 0,9% con adición de tiamina y otras vitaminas hidrosolubles y con reposición de K según las necesidades. La cetoacidosis y los síntomas GI suelen responder con rapidez. (El uso de insulina es adecuado en los pacientes en quienes existe cualquier duda de una CAD atípica.)
Coma hiperglucémico hiperosmolar no cetósico
Síndrome caracterizado por hiperglucemia, deshidratación extrema e hiperosmolaridad plasmática que conducen a un deterioro de la conciencia, acompañado a veces con convulsiones.
El coma hiperglucémico hiperosmolar no cetósico (CHHNC) es una complicación de la DM tipo II y tiene una tasa de mortalidad superior al 50%. Suele presentarse tras un período de hiperglucemia sintomática en el cual la ingesta de líquido es insuficiente para prevenir la deshidratación extrema producida por la diuresis osmótica inducida por la hiperglucemia. El factor desencadenante puede ser la coexistencia de una infección aguda o alguna otra circunstancia (p. ej. paciente anciano que vive solo).
En algunos pacientes el suceso desencadenante es una infección, en especial una neumonía o una sepsis por gramnegativos; pero el CHHNC también puede presentarse cuando los pacientes con una DM tipo II no diagnosticada o descuidada reciben fármacos que deterioran la tolerancia a la glucosa (p. ej., glucocorticoides) o tienen un aumento de pérdida de líquidos (p. ej., por diuréticos). También puede inducirse un CHHNC con la diálisis peritoneal o la hemodiálisis, la alimentación con sonda y con las grandes cargas de glucosa i.v.
Los rasgos constantes y diagnósticos del CHHNC son alteraciones del SNC, hiperglucemia extremada, deshidratación e hiperosmolaridad, acidosis metabólica leve sin hipercetonemia intensa y azoemia prerrenal (o insuficiencia renal crónica preexistente). El estado de la conciencia en el momento de la presentación varía desde la obnubilación mental al coma. En contraste con la CAD pueden producirse crisis convulsivas focales o generalizadas. Puede presentarse hemiplejía transitoria. La glucosa plasmática suele ser del orden de los 1.000 mg/dl (55,5 mmol/l) (muy superior a la mayoría de los casos de CAD). La osmolalidad sérica calculada al ingreso es de unos 385 mOsm/kg, mientras que el nivel normal está alrededor de 290 mOsm/kg Los niveles iniciales de bicarbonato plasmático están ligeramente disminuidos (17 a 22 mmol/l) y el plasma no suele ser muy positivo para los cuerpos cetónicos. Los niveles de Na y K séricos suelen ser normales, pero el BUN y los niveles de creatinina sérica están notablemente aumentados.
El déficit medio de líquido es de 10 litros y el colapso circulatorio agudo es el acontecimiento común terminal en el CHHNC. La trombosis in situ generalizada es un hallazgo frecuente en la autopsia y en algunos casos se ha observado hemorragia atribuida a coagulación intravascular diseminada o dedos aparentemente gangrenosos.
Retinopatía diabética
Es la segunda causa de ceguera y la primera en edad laboral. La prevalencia es muy variable entre el 15 y el 50%, esto es debido a la variabilidad en el tiempo de evolución de la diabetes de las personas incluidas en los estudios.
Nefropatía diabética
El 30-50% de las personas con diabetes con una evolución de la enfermedad de 10 a 20 años presenta algún grado de afectación renal. El porcentaje de pacientes cuya enfermedad renal primaria (ERP) es la diabetes era el 10.1% en él año 2001.
CAPITULO 4. DIAGNÓSTICO
El diagnóstico requiere confirmar la existencia de hiperglucemia, hipercetonemia y acidosis metabólica. Sin embargo, está justificado un diagnóstico de presunción a la cabecera del paciente si la orina o la sangre son fuertemente positivas para glucosa y cuerpos cetónicos. El nivel inicial de glucosa plasmática suele ser de 400 a 800 mg/dl (22,2 a 44,4 mmol/l), pero puede ser más bajo. El pH y el bicarbonato plasmáticos están disminuidos y el hiato aniónico calculado está aumentado. El Na sérico inicial suele estar ligeramente disminuido, mientras que el K sérico inicial habitualmente está elevado o en el límite superior de la normalidad. Los niveles de K £4,5 mEq/l indican una intensa depleción de K y se requiere asistencia rápida. El BUN inicial está con frecuencia aumentado hasta el grado esperado en la azoemia prerrenal. Es característica una elevación de la amilasa sérica, pero es raro que la CAD se asocie con pancreatitis. Es preciso realizar una búsqueda minuciosa de una posible infección susceptible de ser tratada.
Métodos diagnósticos
El diagnóstico se debe realizar mediante la determinación de glucemia basal (en ayunas de 12 h) en plasma venoso o mediante la glucemia a las 2 h de la sobrecarga oral de glucosa (SOG) con 75 g.
Los valores de glucemia obtenidos mediante tiras reactivas leídas en reflectómetro son útiles para el tratamiento clínico de la diabetes o en caso de sospecha clínica. Sin embargo, por su menor exactitud y precisión, no deben ser utilizadas para el diagnóstico.
En los pacientes asintomáticos, la DM se confirma cuando se cumple el criterio diagnóstico para la hiperglucemia en ayunas recomendado por el National Diabetes Data Group (NDDG): concentración de glucosa en plasma (o suero) ³140 mg/dl (³7,77 mmol/l) después de una noche en ayunas en dos ocasiones en un adulto o un niño. Recientemente, la American Diabetes Association recomienda que los niveles de glucosa plasmática en ayunas >126 mg/dl (>6,99 mmol/l) se consideren diagnósticos de DM.
Una prueba de tolerancia oral a la glucosa (PTOG) puede ser útil para diagnosticar la DM tipo II en pacientes cuya glucosa en ayunas está entre 115 y 140 mg/dl (6,38 y 7,77 mmol/l) y en los que están en una situación clínica que podría tener relación con una DM no diagnosticada (p. ej., polineuropatía, retinopatía). Por otra parte, diversos trastornos distintos de la DM, como el efecto de los fármacos, y el proceso de envejecimiento normal pueden causar anomalías en la PTOG.
El NDDG recomienda también criterios para el diagnóstico del deterioro de la tolerancia a la glucosa en los pacientes que no cumplen los criterios diagnósticos para la DM. Los pacientes con deterioro de la tolerancia a la glucosa pueden tener un mayor riesgo de hiperglucemia en ayunas o sintomática, pero en muchos casos el trastorno no progresa o remite.
La DM es un síndrome heterogéneo en el que existe una alteración común que la define: la elevación de la glucemia. Los síntomas clásicos de la DM se deben a la propia hiperglucemia: poliuria, polidipsia, polifagia, pérdida de peso, visión borrosa e infecciones recurrentes, aunque en la mayor parte de los casos, sobre todo en las fases iniciales de la DM2, el paciente se encuentra asintomático.
Detección de nuevos casos
La DM2 puede ser sintomática durante muchos años, por lo que muchos pacientes ya presentan complicaciones en el momento del diagnóstico. Este hecho, junto al beneficio demostrado del tratamiento en la reducción de las mismas, justifica la detección precoz de la enfermedad. Actualmente se recomienda el cribado de la diabetes en las embarazadas y en los individuos mayores de 45 años o con algún factor de riesgo para la diabetes tipo 2.
En todos los casos, excepto en las mujeres gestantes, se debe realizar una glucemia en ayunas (glucemiabasal) en plasma venoso. Como método de cribado, o ante la sospecha clínica, puede utilizarse una determinación en sangre capilar mediante tira reactiva y lectura en reflectómetro, debiendo estar el paciente en ayunas al menos 3 h. Sin embargo, por su variabilidad y menor precisión, siempre se ha de confirmar el diagnóstico mediante determinaciones de laboratorio. Ante una determinación de glucemia normal en un paciente de riesgo, debe repetirse el cribado cada 3 años o más frecuentemente si existen factores de riesgo para la diabetes DM2. En estos casos se propone la determinación anual de la glucemia .
En todas las mujeres embarazadas se debe realizar el cribado de la diabetes gestacional mediante el test de O' Sullivan entre las 24 y 28 semanas de gestacion (tederminación de la glucemia 1 h después de la ingesta de 50 gr de glucosa en cualquier momento del día, sin ayuno previo). Si es superior a 140 mg/dl se ha de realizar el test de tolerancia oral a la glucosa (TTOG) con 100 gr de glucosa para confirmar el diagnostico de diabetes gestacional.
Recomendaciones de la ADA para detección precoz de la diabetes mellitus tipo 2.
-
Cribado universal mediante glucemia basal a los mayores de 45 años cada 3 años
-
Se considerará la detección más frecuente* y en edades más jóvenes en las siguientes poblaciones de riesgo
-
Obesos (IMC > 27)
-
Historia de diabetes en un familiar de primer grado
-
Etnias de alto riesgo en los EE.UU. (afro americanos, hispanos, nativos Americanos, etc.)
-
Diabetes gestacional previa y/o antecedentes de microsomas cHDL ≤ 35 mg/dl y/o triglicéridos ≥ 250 mg/dl Hipertensión arterial (≥ 140/90)
-
Diagnóstico previo de intolerancia a la glucosa (IG) o glucemia basal alterada (GBA)
-
Glucemia basal anual, excepto en caso de IG o GBA previas, que será semestral.
Métodos y criterios diagnósticos
Los criterios diagnósticos son los propuestos por la Asociación Americana de Diabetes (ADA) en 1997 y que han sido aceptados por el comité asesor de la OMS y el Consenso Europeo:
-
Glucemia basal en plasma venoso ≥ 126 mg/dl (7 mmol/l). Debe realizarse una segunda determinación en un día diferente para confirmar el diagnóstico.
-
Síntomas típicos de diabetes y glucemia al azar ≥ 200 mg/dl (11,1 mmol/l). No es necesaria una segunda determinación
-
Glucemia a las 2 h de la SOG con 75 g de glucosa ≥ 200 mg/dl (11,1 mmol/l). La SOG se debería realizar en caso de glucemias basales entre 110-125 mg/dl, aunque actualmente no existe acuerdo respecto a su indicación. Mientras que la ADA la desaconseja para la práctica clínica, el Consenso Europeo y la OMS mantienen su vigencia, propone valorar su necesidad en casos seleccionados. En caso de practicarse deben respetarse escrupulosamente las condiciones para su realización y repetirse en otra ocasión para confirmar el diagnóstico de diabetes (OMS, 1985; ADA, 1997).
A pesar de que diferentes autores propugnan el valor de la HbA1c en el diagnóstico, ni la ADA ni la OMS la han aceptado, ya que se trata de una prueba poco estandarizada, más cara y no disponible en muchos países.
CAPITULO 5. TRATAMIENTO
La dieta para conseguir una reducción de peso es de gran importancia en pacientes con sobrepeso con DM tipo II. Si no se logra una mejoría de la hiperglucemia mediante la dieta, debe iniciarse una prueba con un fármaco oral.
La educación del paciente, junto con la dieta y el ejercicio, es esencial para asegurar la eficacia del tratamiento prescrito, para identificar los signos que exigen buscar atención médica inmediata y para cuidar adecuadamente los pies.
En cada visita médica debe valorarse al paciente en busca de síntomas o signos de complicaciones, incluyendo una revisión de los pies y los pulsos periféricos y la sensibilidad en pies y piernas, y una prueba de albuminuria. La evaluación periódica de laboratorio incluye un perfil lipídico, niveles de BUN y creatinina en suero, ECG y una evaluación oftalmológica completa anual .
Dado que los diabéticos tienen un aumento de riesgo de insuficiencia renal aguda, las exploraciones radiológicas que requieren la inyección i.v. de medios de contraste deben llevarse a cabo sólo si son absolutamente imprescindibles y sólo si el paciente está bien hidratado.
La hipercolesterolemia o la hipertensión aumentan los riesgos de complicaciones tardías específicas y requieren atención especial y un tratamiento adecuado. Aunque los bloqueantes b-adrenérgicos (p. ej., el propranolol) se pueden utilizar inocuamente en la mayoría de los diabéticos, estos fármacos pueden Enmascarar los síntomas b-adrenérgicos de la hipoglucemia inducida por la insulina y pueden dificultar la respuesta contrarreguladora normal. Por ello, los inhibidores de la ECA y los antagonistas del calcio suelen ser los fármacos de elección.
Para el tratamiento inicial.
Muchos especialistas prefieren las sulfonilureas de acción más corta, y la mayoría no recomiendan utilizar una combinación de sulfonilureas diferentes. El tratamiento se inicia a una dosis baja, que se ajusta después de varios días hasta que se obtiene una respuesta satisfactoria o se ha alcanzado la dosis máxima recomendada. Alrededor de un 10 a un 20% de los pacientes no responden a un ensayo de tratamiento (fracasos primarios), y es frecuente que los pacientes que no responden a una sulfonilurea no respondan tampoco a otras. De los pacientes que responden al principio, un 5 a un 10% al año experimentan fracasos secundarios. En estos casos puede añadirse insulina al tratamiento con sulfonilurea.
La hipoglucemia es la complicación más importante del tratamiento con sulfonilureas. La hipoglucemia puede aparecer en pacientes tratados con cualquiera de las sulfonilureas, pero se presenta con mayor frecuencia con las de acción prolongada (gliburida, clorpropamida). La hipoglucemia inducida por las sulfonilureas puede ser grave y persistir, o recurrir durante días después de interrumpir el tratamiento, incluso cuando aparece en pacientes tratados con tolbutamida, cuya duración de acción habitual es de 6 a 12 h. Recientemente se ha descrito una tasa de mortalidad del 4,3% en pacientes hospitalizados con hipoglucemia inducida por sulfonilureas. Por tanto, todos los pacientes tratados con sulfonilureas que presentan una hipoglucemia deben ser hospitalizados porque, incluso si responden rápidamente al tratamiento inicial de la hipoglucemia, tienen que ser estrictamente monitorizados durante 2 o 3 d. La mayoría de estos pacientes pueden no necesitar más el tratamiento con sulfonilureas.
Monitorización de la glucosa plasmática.
Todos los pacientes deben aprender a vigilar la glucosa por sí mismos, y a los pacientes en tratamiento insulínico se les debe enseñar a ajustar sus dosis de insulina en consecuencia. Los niveles de glucosa pueden explorarse con analizadores domésticos de uso fácil que utilizan una gota de sangre del pulpejo de un dedo. Para obtener la muestra de sangre del extremo del dedo se recomienda una lanceta accionada por un resorte. La frecuencia de la determinación se decide individualmente. Los pacientes diabéticos en tratamiento insulínico teóricamente deben medir su glucosa plasmática diariamente antes de las comidas, 1 o 2 h después de comer y al acostarse. Sin embargo, en la práctica pueden obtenerse de dos a cuatro medidas al día en momentos diferentes, de modo que pueda hacerse una valoración global aproximadamente tras una semana de tratamiento.
La mayoría de los médicos determinan periódicamente la hemoglobina glucosilada (HbA1C) para valorar el control de la glucosa plasmática durante el mes a los 3 meses precedentes. La HbA1C es el producto estable de la glucosilación no enzimática de la cadena b de la hemoglobina por la glucosa plasmática y se forma a velocidades que aumentan con los niveles crecientes de glucosa plasmática. En la mayoría de los laboratorios, el nivel normal de HbA1C está alrededor del 6%; en los diabéticos poco controlados el nivel oscila entre el 9 y el 12%. La HbA1C no es una prueba específica para diagnosticar la diabetes; sin embargo, una HbA1C elevada suele indicar la existencia de diabetes.
Otra prueba es el nivel de fructosamina. La fructosamina se forma mediante una reacción química de la glucosa con las proteínas plasmáticas y refleja el control de la glucosa en un período previo de 1 a 3 sem. Por consiguiente, esta determinación puede señalar un cambio en el control antes que la HbA1C y suele ser de utilidad cuando se aplica un tratamiento intensivo y en ensayos clínicos de corta duración.
A los pacientes con DM tipo I se les debe enseñar a realizar la prueba de cuerpos cetónicos en orina con las tiras reactivas disponibles en el mercado y recomendarles su empleo siempre que aparezcan síntomas de resfriado, gripe u otra afección intercurrente, náuseas, vómitos o dolor abdominal, poliuria o si encuentran un nivel de glucosa plasmática inesperadamente alto en la automonitorización. Se recomiendan las pruebas de cuerpos cetónicos en todas las muestras de orina de los pacientes con DM tipo I que presenten fluctuaciones intensas, rápidas y persistentes en su grado de hiperglucemia.
Insulina.
Se suele preferir la insulina humana al iniciar el tratamiento insulínico porque es menos antigénica que las variedades obtenidas de animales. No obstante, en la mayoría de los pacientes en tratamiento insulínico, incluidos los que reciben preparados de insulina humana, aparecen niveles detectables de anticuerpos a la insulina, por lo general muy bajos.
La insulina se suministra generalmente en preparados que contienen 100 U/ml (insulina 100 U) y se inyecta por vía s.c. con jeringas de insulina desechables.
Los pacientes que se inyectan dosis £50 U prefieren generalmente las jeringas de 1/2 ml porque su lectura es más fácil y facilitan la medida exacta de dosis más pequeñas. Un dispositivo para inyectar múltiples dosis de insulina, llamado comúnmente "pluma" o "bolígrafo" de insulina, está diseñado para utilizar un cartucho que contiene las dosis para varios días. La insulina debe conservarse refrigerada, pero nunca congelada; no obstante, la mayoría de los preparados de insulina son estables a temperatura ambiente durante meses, lo que facilita su uso en el trabajo y en los viajes.
Los preparados de insulina se clasifican como de acción corta (acción rápida), acción intermedia o acción prolongada. los datos habituales del comienzo de la acción, el momento de acción máxima y la duración de la acción de los preparados de uso corriente; estos datos deben utilizarse sólo como orientaciones aproximadas, porque existe una variación considerable entre las distintas personas y con diferentes dosis del mismo preparado en el mismo paciente. El factor esencial que determina el comienzo y la duración de la acción de un preparado de insulina es la velocidad de absorción de la insulina a partir del lugar de inyección.
Las insulinas de acción rápida son: la insulina regular, que es un preparado de cristales de insulina-cinc suspendidos en solución; la insulina regular es la única preparación de insulina que puede administrarse i.v. La insulina Lispro, una forma de insulina regular que está preparada mediante ingeniería genética con la sustitución de un aminoácido, proporciona una absorción más rápida de la insulina y por ello puede administrarse con el alimento. La insulina Semilente es una insulina de acción rápida ligeramente más lenta, que contiene microcristales de insulina-cinc en un tampón de acetato. Insulinas de acción intermedia son la neutra protamina Hagedorn, que contiene una mezcla estequiométrica de insulina regular e insulina protamina-cinc, y la insulina Lente, que contiene un 30% de insulina Semilente y un 70% de insulina Ultralente en un tampón de acetato. La insulina protamina-cinc contiene insulina que está cargada negativamente, combinada con un exceso de protamina de esperma de pescado cargada positivamente. La insulina Ultralente contiene grandes cristales de cinc e insulina en un tampón de acetato.
Las mezclas de preparados insulínicos con diferentes comienzos y duraciones de la acción se administran casi siempre en una sola inyección extrayendo dosis medidas de dos preparados en la misma jeringa inmediatamente antes del uso. Los fabricantes recomiendan que la Semilente se mezcle sólo con Lente o Ultralente para mantener la misma solución tampón. Sin embargo, con frecuencia se extraen dosis individuales de insulina regular e insulina neutra protamina Hagedorn o insulina Lente en la misma jeringa para combinar insulina de acción rápida y de acción intermedia en una sola inyección. También se dispone de un preparado que contiene una mezcla con un 70% de insulina neutra protamina Hagedorn y 30% de insulina regular humana semisintética (Novolin 70/30 o Humulina 70/30), pero su proporción fija de insulina de acción intermedia y de acción rápida puede limitar su uso. La insulina protamina-cinc debe inyectarse siempre por separado, ya que contiene un exceso de protamina.
Iniciación del tratamiento insulínico en los adultos.
En el ensayo clínico , los pacientes con DM tipo I recibieron una dosis total media de unas 40 U de insulina al día. Dado que los pacientes con DM tipo II son resistentes a la insulina, necesitan cantidades mayores. Así, los que tienen una intensa hiperglucemia y son obesos pueden empezar con unas 40 U de insulina al día. La dosis total diaria inicial puede dividirse de modo que 1/2 se administre antes del desayuno, 1/4 antes de cenar y 1/4 al acostarse. Debido a la intensa resistencia a la insulina, los pacientes con DM tipo II pueden necesitar el doble de esa dosis y a menudo más. Después de elegir la dosis inicial, los ajustes de las cantidades, tipos de insulina y ritmo temporal se hacen en función de las determinaciones de la glucosa plasmática. Se ajusta la dosis para mantener la glucosa plasmática preprandial entre 80 y 150 mg/dl (4,44 y 8,33 mmol/l). Los incrementos de la dosis de insulina se restringen generalmente a un 10% cada vez y los efectos se valoran a lo largo de unos 3 d antes de hacer cualquier nuevo incremento. Si existe amenaza de hipoglucemia están indicados ajustes más rápidos de la insulina regular.
Pautas de insulina.
El objetivo del tratamiento insulínico es controlar las oleadas hiperglucémicas después de las comidas y proporcionar los niveles basales que sostienen el metabolismo normal de la glucosa. Es preciso que las pautas sean siempre individualizadas, y algunos diabéticos llegarán a conseguir un control estricto con pautas sumamente personalizadas. El enfoque debe incluir en todo caso:
Insulina de acción intermedia al acostarse.
Esto ayuda a controlar la producción de glucosa hepática nocturna. Empezar el día con niveles matutinos de glucosa más bajos mejorará la tolerancia a la glucosa a lo largo de todo el día. La insulina al acostarse se asocia con una menor ganancia de peso que la insulina sola durante el día. La insulina al acostarse es también una forma razonable de iniciar el tratamiento insulínico en pacientes con DM tipo II que no están controlados sólo con fármacos orales.
Insulina mixta antes del desayuno.
Suele realizarse una mezcla aproximada de un 30% de insulina de acción rápida y un 70% de insulina de acción intermedia. La mayoría de los pacientes tendrán necesidad aproximadamente de la mitad de la dosis diaria de insulina antes de desayunar.
Insulina regular antes de comida y cena.
Para obtener un control estricto, la insulina suplementaria de acción rápida debe administrarse antes de las comidas. En el caso de la insulina regular o la Semilente, la dosis debe administrarse de 15 a 30 min antes de la comida, y con una comida en el caso de la Lispro.
Múltiples inyecciones subcutáneas de insulina.
Están destinadas para mantener niveles de glucosa plasmática normales o casi normales a lo largo de todo el día en pacientes con DM tipo II. Esta clase de tratamiento puede aumentar los riesgos de episodios frecuentes y graves de hipoglucemia. Los pacientes deben estar muy motivados, conocer la DM, estar informados de las dudas sobre riesgos y beneficios, ser capaces de automonitorizarse la glucosa y ser supervisados por un médico experto en su utilización. En una pauta típica de inyecciones de insulina subcutáneas múltiples, en torno al 25% de la dosis diaria total se administra en forma de insulina de acción intermedia al acostarse, con dosis adicionales de insulina de acción rápida administradas antes de cada comida (una pauta de 4 dosis). Los pacientes con DM tipo I pueden necesitar insulina de acción intermedia o prolongada por la mañana para dar cobertura a lo largo del día. El paciente ajusta la dosis diaria en función de la automonitorización de la glucosa antes de cada comida y al acostarse; el nivel de glucosa plasmática entre las 2 y las 4 de la madrugada se valora al menos una vez a la semana.
Infusión continua de insulina subcutánea.
Esta modalidad de tratamiento insulínico intensivo en pacientes con DM tipo I emplea una pequeña bomba de infusión alimentada con pilas que suministra una infusión subcutánea continua de insulina de acción rápida por medio de una pequeña aguja, introducida generalmente en la pared abdominal. La bomba se programa para infundir insulina a un ritmo basal seleccionado, suplementado por aumentos de infusión manuales o programados antes de cada comida. El paciente mide los niveles de glucosa varias veces al día para ajustar la dosis. El control alcanzable con este método es superior al que se obtiene con inyecciones múltiples. En el tratamiento con una bomba los episodios hipoglucémicos son frecuentes, especialmente mientras se establece el control metabólico. Sin embargo, una vez establecido éste, las bombas no se asocian con hipoglucemia más que las inyecciones múltiples. Los implantes de bombas y el suministro de insulina experimentales al sistema portal han demostrado ser superiores. Sin embargo, la aguja permanente aumenta el riesgo de infecciones en los lugares en que se coloca.
Tratamiento insulínico de la diabetes inestable.
Los diabéticos inestables son pacientes con una DM tipo I que presentan oscilaciones rápidas y frecuentes de los niveles de glucosa sin causa aparente.
La diabetes inestable
Es muy frecuente en pacientes sin capacidad de secreción de insulina residual. Los procesos metabólicos por medio de los cuales la insulina influye sobre los niveles plasmáticos de glucosa, ácidos grasos libres unidos a albúmina y cuerpos cetónicos están regulados normalmente por desplazamientos del equilibrio entre los efectos de la insulina y los efectos antagónicos del glucagón (en el hígado) y el sistema nervioso autónomo adrenérgico. Estos mecanismos contrarreguladores están regulados independientemente y se activan normalmente durante el ayuno, el ejercicio y otros estados que requieren protección contra la hipoglucemia. Las dosis de insulina tienen que ser suficientes para hacer frente a un súbito aumento de los mecanismos contrarreguladores y para evitar el rápido desarrollo de hiperglucemia e hipercetonemia sintomáticas, pero esto produce muchas veces excesos transitorios de la insulina plasmática.
Muchos de estos pacientes mejoran cuando cambian a una pauta modificada de insulina con inyecciones subcutáneas múltiples, que proporciona la mayor parte de la insulina diaria en forma de insulina de acción rápida en dosis diarias ajustadas antes de cada comida, con algo de insulina de acción intermedia por la mañana, antes de la cena o al acostarse. La finalidad no es mantener el nivel diurno de glucosa plasmática en el intervalo normal o casi normal, sino estabilizar las fluctuaciones en un intervalo que evite la hiperglucemia o la hipoglucemia sintomática.
Complicaciones del tratamiento insulínico.
La hipoglucemia (v. más adelante) puede presentarse por un error al dosificar la insulina, una comida ligera u omitida o un ejercicio no planeado (se enseña generalmente a los pacientes a reducir su dosis de insulina o a aumentar su ingesta de hidratos de carbono antes de un ejercicio programado). Se enseña a los pacientes a identificar los síntomas de hipoglucemia, que suelen responder con rapidez a la ingestión de azúcar. Todos los diabéticos deben llevar consigo caramelos, terrones de azúcar o tabletas de glucosa. Una tarjeta, un brazalete o un collar de identificación indicativos de que el paciente es un diabético tratado con insulina ayudan a identificar la hipoglucemia en las urgencias. Los familiares próximos deben saber cómo administrar glucagón con un dispositivo de inyección fácil de usar. El personal médico de urgencias, tras confirmar la hipoglucemia con un glucómetro, debe iniciar el tratamiento con una inyección única rápida (bolo) de 25 ml de solución de glucosa al 50% seguida de infusión IV continua de glucosa.
El fenómeno del alba
Describe la tendencia normal de la glucosa plasmática a aumentar en las primeras horas de la mañana, antes del desayuno; la tendencia suele ser exagerada en pacientes con DM tipo I y en algunos pacientes con DM tipo II. Los niveles de glucosa en ayunas se elevan por un aumento de la producción hepática de glucosa, el cual puede ser secundario a la oleada de hormona de crecimiento que se produce a medianoche. En algunos pacientes con DM tipo I, la hipoglucemia nocturna puede ir seguida por un notable aumento de la glucosa plasmática en ayunas con una elevación en plasma de los cuerpos cetónicos (fenómeno de Somogyi). Por tanto, el fenómeno del alba y el fenómeno de Somogyi se caracterizan por hipoglucemia matutina, pero el último se debe a una hiperglucemia de rebote (contrarregulación). La frecuencia con que ocurre realmente el fenómeno de Somogyi es objeto de discusión. Cuando se sospecha su existencia, el paciente debe despertarse entre las 2 y las 4 de la madrugada para monitorizar los niveles de glucemia. Si se administra insulina de acción intermedia al acostarse, suele ser posible evitar los fenómenos del alba y de Somogyi.
Las reacciones alérgicas locales
En el lugar de las inyecciones de insulina son menos frecuentes con las insulinas porcina y humana purificadas. Estas reacciones pueden producir dolor y quemazón inmediatos, seguidos tras varias horas de eritema, prurito e induración locales, persistiendo esta última a veces durante días. La mayoría de las reacciones desaparecen espontáneamente después de semanas de inyección continuada de insulina y no necesitan ningún tratamiento específico, aunque a veces se utilizan antihistamínicos.
La alergia generalizada a la insulina
Por lo general a la molécula de insulina es rara, pero puede presentarse cuando se interrumpe el tratamiento y se reinicia tras un plazo de meses o años. Estas reacciones pueden producirse con cualquier tipo de insulina, incluso con la insulina humana biosintética. Los síntomas suelen aparecer poco después de una inyección y pueden consistir en urticaria, angioedema, prurito, broncospasmo y, en algunos casos, colapso circulatorio. Puede bastar un tratamiento con antihistamínicos, aunque a veces se necesita utilizar adrenalina y corticosteroides por vía i.v. Si es preciso continuar con el tratamiento insulínico después de estabilizarse la situación del paciente, deben llevarse a cabo pruebas cutáneas con un conjunto de preparados de insulina purificados y una desensibilización realizada por un médico experimentado.
La resistencia a la insulina
Es un aumento de las necesidades de insulina ³200 U/d y se asocia con aumentos notables de la capacidad de unión de la insulina plasmática. La mayoría de los pacientes tratados con insulina durante ³6 meses desarrollan anticuerpos a la insulina. La antigenicidad relativa de los preparados de insulina purificados es bovina > porcina > humana, pero los factores genéticos influyen también sobre la respuesta individual. Los anticuerpos fijadores de insulina circulantes pueden modificar la farmacocinética de la insulina libre, pero el tratamiento no suele verse afectado desfavorablemente. En los pacientes con resistencia a la insulina, el cambio a una insulina purificada porcina o humana puede reducir las necesidades. La remisión puede ser espontánea, o puede ser inducida en algunos pacientes con DM tipo II que pueden interrumpir el tratamiento insulínico durante 1 a 3 meses. La prednisona puede reducir las necesidades de insulina en el plazo de 2 semanas; el tratamiento suele iniciarse con unos 30 mg 2 veces al día y se reduce progresivamente a medida que disminuyen las necesidades.
La atrofia o la hipertrofia de la grasa local
En los lugares de inyección es relativamente rara y suele mejorar al cambiar a insulina humana e inyectarla directamente en el área afectada. No se necesita ningún tratamiento específico de la hipertrofia grasa local, pero los lugares de inyección deben cambiarse en forma rotatoria.
Fármacos antidiabéticos orales.
Estos fármacos se utilizan en la DM tipo II, pero no en la DM tipo I, porque en ese tipo de pacientes no pueden prevenir la hiperglucemia sintomática ni la CAD. Los fármacos hipoglucemiantes orales son las sulfonilureas. Los fármacos antihiperglucémicos son las biguanidas, los inhibidores de la a-glucosidasa y los sensibilizadores a insulina (tiazolidindionas ["glitazonas"]).
Sulfonilureas.
Las sulfonilureas reducen la glucosa plasmática fundamentalmente estimulando la secreción de insulina. Los efectos secundarios al potenciar la sensibilidad a la insulina periférica y hepática pueden ser debidos a una disminución de la toxicidad de la glucosa y también del aclaramiento de la insulina. Las sulfonilureas difieren en la potencia y la duración de su acción. Todas las sulfonilureas son metabolizadas en el hígado, pero sólo la tolbutamida y la tolazamida son inactivadas exclusivamente por el hígado. Alrededor del 30% de la clorpropamida se excreta normalmente en la orina, y el principal metabolito hepático de acetohexamida es sumamente activo y se excreta en la orina; ambos fármacos conllevan un aumento de riesgo de hipoglucemia prolongada en pacientes con deterioro de la función renal y en los ancianos. Las sulfonilureas de 2.ª; generación (como glipizida y gliburida) son unas 100 veces más potentes que las de 1.ª; generación, se absorben con rapidez y se metabolizan sobre todo en el hígado. Clínicamente, las sulfonilureas de 2.ª; generación son similares en eficacia.
Las reacciones alérgicas y otros efectos secundarios (p. ej., ictericia colestática) son relativamente infrecuentes.
La acetohexamida puede utilizarse en los pacientes alérgicos a otras sulfonilureas. La clorpropamida y la acetohexamida no deben utilizarse en pacientes con deterioro de la función renal. Además, la clorpropamida no debe utilizarse en pacientes ancianos, porque puede potenciar la acción de la hormona antidiurética, llevando a menudo a un deterioro del estado mental, el cual, en un paciente anciano, no suele identificarse como un efecto inducido por fármacos.
La hipoglucemia es la complicación más importante del tratamiento con sulfonilureas. La hipoglucemia puede aparecer en pacientes tratados con cualquiera de las sulfonilureas, pero se presenta con mayor frecuencia con las de acción prolongada (gliburida, clorpropamida). La hipoglucemia inducida por las sulfonilureas puede ser grave y persistir, o recurrir durante días después de interrumpir el tratamiento, incluso cuando aparece en pacientes tratados con tolbutamida, cuya duración de acción habitual es de 6 a 12 h. Recientemente se ha descrito una tasa de mortalidad del 4,3% en pacientes hospitalizados con hipoglucemia inducida por sulfonilureas. Por tanto, todos los pacientes tratados con sulfonilureas que presentan una hipoglucemia deben ser hospitalizados porque, incluso si responden rápidamente al tratamiento inicial de la hipoglucemia, tienen que ser estrictamente monitorizados durante 2 o 3 d. La mayoría de estos pacientes pueden no necesitar más el tratamiento con sulfonilureas.
Fármacos antihiperglucémicos.
La metformina (una biguanida) se ha utilizado como tratamiento principal en pacientes con DM tipo II durante más de 30 años en la mayor parte del mundo. Ha sido aprobada recientemente para su uso en Estados Unidos. Actúa reduciendo la producción de insulina por el hígado y puede incrementar la sensibilidad a la insulina en los pacientes que pierden peso. Es igualmente eficaz que una sulfonilurea como monoterapia (cuando se emplea sola rara vez causa hipoglucemia) y se comporta sinérgicamente en el tratamiento combinado con sulfonilureas. La metformina estimula también la pérdida de peso y reduce los niveles de lípidos. A diferencia de la fenformina, la metformina rara vez causa una acidosis láctica grave. Los efectos secundarios GI son frecuentes, pero a menudo pasajeros, y pueden prevenirse si el fármaco se toma con las comidas y si la dosis se aumenta gradualmente (en 500 mg/sem hasta 2,5 g). La metformina está contraindicada en los pacientes con nefropatías y hepatopatías o alcoholismo. También está contraindicada para los pacientes con acidosis láctica, y en la mayoría de los casos debe restringirse durante la hospitalización de los casos agudos.
La acarbosa es un inhibidor de la a-glucosidasa que inhibe competitivamente la hidrólisis de los oligosacáridos y monosacáridos. Esto retarda la digestión de los hidratos de carbono y la subsiguiente absorción en el intestino delgado, produciéndose una menor elevación posprandial de los niveles de glucemia. Dado que este mecanismo de acción difiere del de otros hipoglucemiantes orales, puede emplearse en el tratamiento combinado con otros agentes orales. Los efectos secundarios GI son muy frecuentes, pero suelen ser pasajeros. Hay que tomar el fármaco con las comidas, y la dosis debe aumentarse gradualmente desde 25 mg hasta 50 a 100 mg en cada comida.
Las tiazolidindionas son fármacos sensibilizadores a la insulina que mejoran la sensibilidad a la insulina en el músculo esquelético e inhiben la producción de la glucosa hepática. El único fármaco de esta clase disponible en Estados Unidos es la troglitazona. Ha sido aprobada recientemente para su empleo en el tratamiento de pacientes con DM tipo II que precisan insulina y tiene efectos moderados en la reducción de los niveles plasmáticos de glucosa y triglicéridos. Este fármaco se administra una vez al día y tiene una hepatotoxicidad posiblemente intrínseca. Se debe informar a los pacientes que disminuyan su dosis diaria de insulina al iniciar el tratamiento.
Tratamiento dietético.
En los diabéticos tratados con insulina, el tratamiento dietético se dirige a limitar las variaciones en el ritmo temporal, las cantidades y la composición de las comidas que podrían hacer inadecuada la pauta de insulina y dar lugar a hipoglucemia o a una hiperglucemia posprandial intensa. Todos los pacientes tratados con insulina necesitan un tratamiento dietético detallado que incluya la prescripción de la ingesta calórica diaria total, orientación sobre las proporciones de hidratos de carbono, grasas y proteínas en sus dietas e instrucciones sobre cómo distribuir las calorías entre las distintas comidas y refrigerios. Un dietista profesional puede dar forma al plan dietético y enseñar al paciente a cubrir sus necesidades individuales. La flexibilidad, no obstante, ayuda a mantener la motivación del paciente.
Existen publicaciones de la American Diabetes Association y de otras fuentes para la planificación de la dieta y la educación de los pacientes. Las listas intercambiables que proporcionan información sobre el contenido de hidratos de carbono, grasas, proteínas y calorías de las raciones individuales se emplean para traducir la prescripción dietética en un plan de alimentación, el cual debe contener alimentos que gusten al paciente, siempre que no exista un motivo específico para excluir un alimento concreto. Los alimentos con valores de intercambio similares (es decir, calorías y contenidos similares de hidratos de carbono, proteínas y grasas) pueden tener efectos diferentes sobre la hiperglucemia posprandial en todos los diabéticos. No obstante, las listas de intercambio son útiles para reducir la variación en la cantidad y la composición de los desayunos, almuerzos, cenas y refrigerios habituales del paciente.
En los pacientes con DM tipo II obesos
Los objetivos del tratamiento dietético son perder peso y controlar la hiperglucemia. La dieta debe satisfacer las necesidades mínimas diarias de proteínas (0,9 g/kg) y estar diseñada para inducir una pérdida de peso gradual y sostenida (alrededor de 1 kg/sem) hasta alcanzar y mantener el peso corporal ideal. Un dietista puede colaborar en el desarrollo de una dieta que vaya a seguir el paciente. Aumentar la actividad física en los pacientes con DM tipo II obesos y sedentarios es deseable y puede reducir con el tiempo la resistencia a la insulina. Los diabéticos con hipertensión deben tratarse con inhibidores de la ECA, los cuales han demostrado ser más protectores frente a la arteriopatía coronaria que los bloqueantes del canal de Ca.
Tratamiento de la diabetes durante la hospitalización.
Los pacientes diabéticos ingresados en hospitales tienen comúnmente enfermedades que agravan la hiperglucemia, por ejemplo una infección o una arteriopatía coronaria. El reposo en cama y una dieta regular también pueden agravar la hiperglucemia. A la inversa, si el paciente padece anorexia o tiene vómitos, o si la ingesta de alimento es reducida, la continuación de los fármacos puede producir hipoglucemia. El cálculo tradicional de las necesidades de insulina con una regla deslizante no debe ser la única intervención, porque es más bien reactiva que proactiva en la corrección de la hiperglucemia. También puede ser empleado incorrectamente cuando la hiperglucemia refleja la gluconeogénesis hepática en respuesta a una hipoglucemia no corregida previamente.
Los pacientes con DM tipo II que están hospitalizados suelen encontrarse bien sin ningún cambio en los fármacos. Los fármacos hipoglucemiantes pueden interrumpirse durante una afección aguda asociada con disminución de la ingesta de alimento o una que tenga tendencia a causar hipoglucemia. Puede añadirse insulina si los niveles plasmáticos de glucosa continúan siendo altos.
En los pacientes con DM tipo I, la insulina (NPH o Lente) debe seguir administrándose a un 50 a 70% de la dosis diaria fraccionada en dos o tres veces. La insulina regular suplementaria puede administrarse con arreglo a la escala deslizante. En pacientes que reciben nutrición parenteral total o parcial, la hiperglucemia se debe tratar con una infusión de insulina i.v. continua o con dosis fraccionadas de insulina de acción intermedia. La glucemia debe medirse cuatro veces al día antes de las comidas.
Control de los diabéticos durante las intervenciones quirúrgicas.
Las intervenciones quirúrgicas (incluidos el estrés emocional previo, los efectos de la anestesia general y el traumatismo de la intervención) pueden aumentar notablemente la glucosa plasmática en los diabéticos e inducir CAD en los pacientes con DM tipo I. En los pacientes que reciben normalmente una o dos inyecciones diarias de insulina, puede administrarse 1/3 a 1/2 de la dosis matutina habitual en la mañana anterior a la operación e iniciar una infusión i.v. de glucosa al 5%, ya sea en solución de cloruro sódico al 0,9% o bien en agua a un ritmo de 1 litro (50 g de glucosa) a lo largo de 6 a 8 h. Tras la operación se comprueban la glucosa y los cuerpos cetónicos en el plasma. A no ser que esté indicado un cambio en la dosis, se repite la dosis preoperatoria de insulina cuando el paciente se haya recuperado de la anestesia y se continúa con la infusión de glucosa. La glucosa y los cuerpos cetónicos plasmáticos se monitorizan a intervalos de 2 a 4 h y se administra insulina regular cada 4 a 6 h según las necesidades para mantener un nivel de glucosa plasmática entre 100 y 250 mg/dl (5,55 y 13,88 mmol/l). Esta pauta se mantiene hasta que el paciente pueda reanudar las tomas orales y una pauta de 1 o 2 dosis de insulina.
Algunos médicos prefieren no administrar la insulina subcutánea el día de la operación y añadir de 6 a 10 U de insulina regular a 1 litro de glucosa al 5% en solución de cloruro sódico al 0,9% o en agua e infundirla inicialmente a un ritmo de 150 ml/h en la mañana de la operación según el nivel de glucosa plasmática. Esta pauta se mantiene a lo largo de la recuperación, ajustando la insulina en función de los niveles plasmáticos de glucosa obtenidos posteriormente en la sala de recuperación a intervalos de 2 a 4 h.
La insulina no es necesaria en los diabéticos que han mantenido un nivel de glucosa plasmática satisfactorio con la dieta sola o en combinación con una sulfonilurea antes de la operación. Las sulfonilureas deben suspenderse de 2 a 4 d antes de la operación, y debe medirse la glucosa plasmática antes y después de la operación y cada 6 h mientras los pacientes reciban líquidos por vía i.v.
El tratamiento con insulina no debe exagerarse y puede ser innecesario, porque una hidratación suficiente reducirá generalmente los niveles de glucosa plasmática. Los pacientes con CHHNC suelen ser muy sensibles a la insulina y las dosis grandes pueden desencadenar descensos bruscos de la glucosa plasmática. Una reducción demasiado rápida de la osmolalidad puede originar un edema cerebral. Sin embargo, muchos pacientes obesos con DM tipo II con un CHHNC necesitan dosis de insulina mayores para reducir su intensa hiperglucemia. Si se administra insulina, debe añadirse glucosa al 5% a los líquidos i.v. cuando la glucosa plasmática llegue aproximadamente a 250 mg/dl (13,88 mmol/l) para evitar la hipoglucemia. Tras la recuperación del episodio agudo, los pacientes pasan generalmente a las dosis ajustadas de insulina regular s.c. a intervalos de 4 a 6 h. Muchos pacientes que son tratados eficazmente del CHHNC con insulina al principio pueden mantener el control de la glucosa con la dieta o con hipoglucemiantes orales.
Condiciones para la realización del Test de Tolerancia Oral a la Glucosa o sobre carga oral de glucosa (OMS)
Administración oral de 75 mg de glucosa en 250 cm³ de agua (en la embarazada: 100g, en el niño : 175 g/Kg. ).
Se ha de realizar entre las 8 y 10 de la mañana, en ayunas de 12 hrs., en ausencia de cualquier medicación y después de 3 días de dieta rica en hidratos de carbono (>150g).
El paciente debe permanecer en reposo y sin fumar durante la realización de la prueba.
En el adulto (a, excepción de las mujeres embarazadas) es suficiente con la determinación a las 2 hrs.
Valoración inicial y seguimiento del paciente
Se relacionan los diferentes datos de anamnesis, exploración física y pruebas complementarias a registrar en el momento del diagnóstico y la periodicidad con que deben realizarse.
Datos a registrar en la valoración inicial y el seguimiento anual
Antecedentes familiares, diabetes y enfermedades cardiovasculares
Antecedentes personales, enfermedades cardiovasculares, factores de riesgo cardiovascular: tabaco, hipertensión arterial, obesidad, hiperlipemia, consumo de alcohol .Complicaciones específicas de la diabetes.
Evolución y grado de control de la diabetes ,motivo de diagnostico y circunstancia concomitantes. Caracteristicas y cumplimiento de la dieta, control metabólico previo, tipo y frecuencia de autoanalisis, ingresos hospitalarios ,episodios hipoglucemicos, tratamientos previos y actual,Cumplimiento
Exploración física: peso, talla, índice de masa corporal (kg/talla en m²), índice de cintura/cadera, presión arterial en decúbito y ortostatismo; Exploración neurológica: si existe clínica sugestiva de neuropatía, pulsos pedíos, femorales y carotídeos, índice tobillo/brazo [ITB] si se dispone de Doppler; Examen de los pies: sensibilidad vibratoria y monofilamentos; Palpación tiroidea; Exploración oftalmológica: agudeza visual, tonometría y Fondo de ojo dilatado) a realizar por el oftalmólogo; Examen dental y Periodental (odontólogo).
Analítica y exploraciones complementarias: sangre, hemograma, glucemia, creatinina, colesterol total, HDL y LDL, triglicéridos y HbAc
Orina: albumina en orina matinal, sedimento, glucosoria y cetonuria.
Algunos consideran que se realice el fondo de ojo cada 2 años en pacientes con buen control glucémico y anuncia de proteinuria o retinopatía en controles previos.
Visitas de seguimiento
Las visitas se programarán en función del tiempo de evolución, las necesidades del proceso educativo y el grado de control metabólico, inicialmente cada dos semanas, hasta ajustar el tratamiento y haber desarrollado el programa básico de educación. La insulinización requiere una frecuencia diaria de visitas de enfermería durante la primera semana. Cuando el paciente mantenga un grado de control bueno o aceptable puede ser controlado cada 2-3 meses por el personal de enfermería, y cada 4-6 meses por el médico. Si el control metabólico es deficiente o existen complicaciones, las visitas serán más frecuentes, alternando las visitas médicas y de enfermería.
Todo diabético debería recibir al menos 3 o 4 visitas de enfermería anuales con contenidos educativos diferentes y al menos 2 visitas médicas con el fin de valorar el grado de consecución de los objetivos pactados con el paciente y el control metabólico. En una de ellas debe efectuarse una revisión anual que incluya el interrogatorio y exploración completa para la detección precoz de complicaciones. Deberían establecerse mecanismos de recapción del diabético son: proporcionar un buen estado nutricional y contribuir a prevenir y tratar las complicaciones, tanto agudas como crónicas. Una alimentación correcta conseguirá estos objetivos al ayudar a:
-
Alcanzar la normalidad bioquímica (glucemia y lípidos plasmáticos).
-
Minimizar las fluctuaciones de glucemia posprandiales
-
Conseguir y mantener el normopeso.
Contenido de las visitas de control de enfermería
-
Anamnesis.
Síntomas de Hipoglucemia o hiperglucemia y complicaciones, consumo de alcohol y tabaco.
-
Evolución de la libreta de autocontrol del paciente.
Resultados de autoanalisis, registro de peso
Registro de hipoglucemias
Cirugía Metabólica
Hasta ahora el tratamiento médico no ha cambiado el curso natural de la enfermedad, siendo la principal causa de ceguera, amputación y diálisis .
Por primera vez el Centro de Cirugía Bariátrica y Metabólica de Clínica Las Condes realiza una nueva técnica llamada BYPASS DUODENO-YEYUNAL, la que consiste en saltarse la primera porción del intestino delgado, permitiendo que el alimento llegue rápidamente al intestino más lejano (distal), produciendo así liberación de hormonas intestinales (incretinas) que ayudarán a la regulación de la insulina y con ello, a la mejoría o incluso remisión completa de la diabetes.
Por primera vez, las cirugías de obesidad no tendrán como fin principal la baja de peso, sino será la cura de enfermedades metabólicas crónicas como la diabetes tipo II.
No hay más de 200 pacientes operados en el mundo con esta técnica y en ellos se ha demostrado remisión completa o incluso cura de la diabetes en más de un 90%. La cirugía metabólica es una exclusión del duodeno (primera parte del intestino) que deriva del switch duodenal. Ésta intervención ha demostrado, desde hace muchos años, mejorar o incluso curar la diabetes en obesos. La cirugía consiste en la exclusión del duodeno realizada con un, cirugía que se prolonga entre 1 a 2 horas.
La cirugía metabólica está indicada para pacientes diabéticos tipo II, no obesos con IMC (índice de masa corporal) entre 22 a 30, entre 18 a 65 años, y en caso de contar con tratamiento para la insulina, ésta debe haberse prolongado por menos de 10 años.
La cirugía metabólica es la próxima gran revolución en cirugía digestiva. Y, a pesar de que existe más de una técnica, todas apuntan a la mejoría de la diabetes a través de algún tipo de bypass del tubo digestivo. Hoy la diabetes puede ser bien controlada con el tratamiento médico y dietético; sin embargo, el curso natural de la enfermedad no ha cambiado significativamente en los el último tiempo, siendo ésta una enfermedad crónica que al cabo de 20 años comienza a producir efectos indeseados en el sistema renal, vascular y la retinopatía.
Para los cirujanos de obesidad es un hito poder observar cómo un paciente que se maneja con 30 unidades de insulina al día y 3 medicamentos orales, al tercer día normaliza sus glicemias y queda sin medicamentos, si bien se sabe que a corto y mediano plazo esta cirugía pionera ha demostrado excelentes resultados, se requiere un seguimiento a más largo plazo para determinar su efectividad al igual que ocurrió con los obesos. Los resultados actuales son muy alentadores y se ve como una técnica muy promisoria.
Actualmente, existen 200 pacientes operados en el mundo, siendo Brasil el país líder en estas intervenciones. También se han realizado en Estados Unidos, India y algunos países de Europa.
Para poder implementar esta cirugía, se requirió evidencia científica con estudios en animales. El Dr. Francesco Rubino del Hospital Presbiteriano de Nueva York/ Centro Médico Weill Cornell -desde el 2005- fue pionero en demostrar la efectividad de la exclusión duodenal para tratar la diabetes. Gracias a este procedimiento, se abre una gran esperanza para tratar la diabetes, enfermedad crónica que hasta ahora era incurable y que en los últimos 100 años se ha tratado sólo con el manejo médico y diabético. En estos 200 pacientes mencionados, la remisión completa de la diabetes (es decir, sin uso de ningún medicamento, ni dieta ni insulina) ha sido de un 90%, lo que abre las puertas a lo que sea una revolución. No sólo dejan los medicamentos, sino que también evitan la aparición a futuro de las complicaciones habituales de la diabetes. El fin último es controlar la enfermedad y alterar su curso natural ominoso, En nuestro país, la tasa de diabetes, se estima llegará a un 15% en los próximos años.
CAPITULO 6. CUIDADOS DE ENFERMERIA
Cuando la enfermera(o) nos encontramos frente a una persona que tiene diabetes, tenemos que tener en cuenta ¿Qué actitud tiene y que respuestas está desarrollando esa persona ante la enfermedad?, ¿Tiene esa persona y su familia los conocimientos, la fuerza y la voluntad para satisfacer las necesidades que su situación les plantea?
Una enfermedad crónica puede ser definida como “aquel trastorno orgánico funcional que obliga a su modificación del estilo de vida de la persona es probable que persista durante largo tiempo”
Algoritmo de actuación
Valoración necesidades/patrones:
-
Extracción sangre
-
Peso/talla
-
Toma de T/A realización ECG (Adultos)
-
Revisión y exploración de los pies (Adultos)
-
¿Fuma? Si : Consejo Antitabaco
-
Apoyo para afrontamiento y adaptación
-
Inicio programa educativo educativo básico según plan terapéutico
pactado (Dieta/ADO/Insulina)
-
Dispensación material para administración plan terapéutico
(Insulina): Agujas, jeringas, lancetas….
(Deberá realizarse la primera semana tras diagnostico).
Fase de compensación:
Se citará según plan terapéutico y objetivos de control hasta terminar programa educativo básico cada 2-3 días.
Seguimiento:
-
Evaluar si se consiguen objetivos pactados
-
Evaluaremos los posibles efectos secundarios (hipoglucemias).
-
Revisamos zonas de inyección.
-
Inspección y detección pie de riesgo una vez al año tras el diagnóstico
-
Valorar cumplimiento y afrontamiento del proceso.
-
Refuerzos educativos cada 3/6 meses una vez terminado programa.
-
Extracción sangre cada 3/6 meses según grado de control.
-
Citas entre 15 días y 3 meses según grado y objetivo de control.
Mantener la TA
Situaciones de (Descompensaciones de glucemia).
Higiene corporal
Estado de zonas de inyección de insulina.
Integridad de la piel
-
Exploración sistematizada de los pies.
-
Lleva hidratos de carbono de absorción rápida
Seguridad
-
Presencia de hipoglucemias- hiperglucemias.
-
Resuelve correctamente las hipo-hiperglucemia
-
Prepara y se administra correctamente la insulina
-
Tiene sentimientos de desvalorización hacia si mismo
-
Sentimientos-emociones hacia la diabetes (Ansiedad, temor, impotencia)
-
Capacidad de afrontamiento/adaptación a la situación actual
-
Se observa o manifiesta incumplimiento del plan terapéutico
Comunicación
-
Capacidad para expresar emociones - miedos.
-
Relaciones familiares sociales.
-
Disfunción sexual.
Valores y creencias
-
Concepto Salud/enfermedad
-
Falsas creencias sobre la insulina, diabetes y sus complicaciones.
-
Barreras que impiden alcanzar la Salud.
Realización personal
-
Alteración de los roles de la persona o familia cansado en el cuidador principal
-
Trabajo/actividad Modificación de actividades recreativas.
Capacidad de aprender
-
Conocimiento sobre Diabetes (Concepto, criterios de control de alimentación equilibrada).
-
Tratamiento farmacológico
-
Complicaciones agudas y crónicas
-
Utilización de los servicios sanitarios
-
Dificultades en el aprendizaje
-
Limitaciones en el aprendizaje
Conocimiento del sistema sanitario.
Además de estas consideraciones especiales debe reflejarse en la historia cualquier respuesta en el individuo para satisfacer sus necesidades que no sea adecuada o suficiente y que pueda generarle un problema que podamos resolver o bien orientar a otro profesional a la resolución del mismo.
Aunque los parámetros bioquímicos, no son en ningún caso respuestas del usuario hacia una necesidad y compete su resolución a otro colectivo profesional, es imprescindible que aparezcan no reflejados en su historia clínica, independientemente del profesional que los trate.
CAPITULO 7. GUÍA DE ATENCIÓN ENFERMERA A PERSONAS CON DIABETES
Según la Organización Mundial de la salud, la diabetes Mellitus es un proceso crónico compuesto por un grupo de enfermedades metabólicas caracterizadas por la hiperglucemia resultante de defectos en la secreción y/o acción de la insulina.
La diabetes constituye un problema personal y de salud pública de enormes proporciones. Siendo una de las principales causas de invalidez y muerte prematura en la mayoría de los países desarrollados y es motivo de un importante deterioro en la calidad de vida de las personas afectadas. Existe una gran variabilidad en la prevalencia de la diabetes en los distintos países del mundo, del 1 al 50%, dependiendo de los factores de riesgo en cada población y de la metodología empleada para su determinación. En los estudios epidemiológicos de calidad que ponen de manifiesto la prevalencia real de la DM1. Prácticamente todos estos estudios están realizados con los criterios de diabetes existentes antes de 1997. En este año, la American Diabetes Association (ADA) propuso unos nuevos criterios diagnósticos, descendiendo el nivel de glucemia basal para el diagnóstico de diabetes de 140 a 126 mg/dl. Estos mismos criterios son los recomendados por la OMS en 1992. En España existen 2 estudios realizados según estos últimos criterios diagnósticos que establecen la prevalencia de la diabetes en el 15'9% y el 14'7%, sin embargo el tamaño de la muestra es pequeño lo que plantea dificultades para su extrapolación a población general. En España la diabetes ocupa el sexto lugar en causa de muerte junto con la enfermedad cerebrovascular, tiene la peculiaridad de provocar una mayor mortalidad en las mujeres que en los hombres, siendo la tercera causa de muerte.
La distribución de los costos directos producidos por la diabetes tipo 2 en está presidida por los gastos de hospitalización (32%), cuya duración media es de 8,1 días; la atención ambulatoria (25,6%), el uso de antidiabéticos orales (4,6%) y el uso de otros fármacos como la insulina y los dedicados a tratar las complicaciones, como los cardioprotectores, gastrointestinales o antiinfecciosos (25,6%). La mayoría de estudios sobre costes económicos en el ámbito de la DM parecen coincidir en que la mayor parte de los recursos directos se emplean en el tratamiento de las complicaciones crónicas en régimen hospitalario, sobrepasando el 50% del total del gasto de la enfermedad.
Cuando las enfermeras nos encontramos frente a una persona que tiene diabetes, tenemos que tener en cuenta.
-
¿Qué actitudes tiene y que respuestas está desarrollando esa persona ante la enfermedad?
-
¿Tiene esa persona y su familia los conocimientos, la fuerza y la voluntad para satisfacer las necesidades que su situación les plantea?
Una enfermedad crónica puede ser definida como “aquel trastorno orgánicofuncional que obliga a una modificación del estilo de vida de la persona y es probable que persista durante largo tiempo”
La visión enfermera
Fase de compensación
Se citará según plan terapéutico y objetivos de control hasta terminar programa educativo básico cada 2-3 días.
Seguimiento:
-
Evaluar si se consiguen objetivos pactados
-
Evaluaremos los posibles efectos secundarios (Hipoglucemias)
-
Revisamos zonas de inyección.
-
Inspección y detección pie de riesgo una vez al año.
-
Programa educativo avanzado durante el primer año tras el diagnóstico.
-
Valorar cumplimiento y afrontamiento del proceso.
-
Refuerzos educativos cada 3-6 meses una vez terminado programa.
-
Extracción sangre cada 3/6 meses según grado de control.
-
Citas entre 15 días y 3 meses según grado y objetivos de control
-
Valoración necesidades/ patrones:
-
Extracción sangre
-
Peso/talla
-
Toma de T/A realización ECG (Adultos)
-
Revisión y exploración de los pies (Adultos)
-
¿Fuma? Si : Consejo antitabaco
-
Apoyo para afrontamiento y adaptación
-
Inicio programa educativo básico según plan terapéutico pactado(Dieta/ADO/Insulina)
-
Dispensación material para administración plan terapéutico (insulina): Agujas, jeringas, lancetas (Deberá de realizarse la primera semana tras diagnóstico)
Valoración
La valoración no solo es el registro de datos sino la puesta en marcha de un proceso sistematizado y completo que debe de constar de:
Recogida de datos a través de la entrevista, la observación y el examen físico.
Validación y organización de los mismos, según el modelo enfermero adoptado.
Registro en un instrumento de valoración estandarizado en el cual los datos tanto objetivos como subjetivos, queden recogidos, organizados y clasificados de forma que nos orienten hacia la obtención de diagnósticos de una forma integradora y no lineal, indicándonos a su vez problemas que deban de ser tratados en colaboración o por otro profesional.
CONCLUSIONES
La investigación realizada sobre Diabetes Mellitus fue muy rica en información, pues, como mencione en un principio, hay muchos sujetos de atención afectados por esta patología. Es muy importante hacerse estudios para desacartar algún tipo de Diabetes y controlarla de manera eficaz.
El diagnóstico de la enfermedad produce una grave distorsión en la vida de la persona, por la amenaza implícita o explícita que supone a su integridad, así como por los múltiples cambios en el estilo de vida a los que deberá hacer frente desde el inicio. Los problemas afectan a 3 áreas:
1-Área personal: pérdida del estado de salud anterior, modificaciones o pérdidas en la escala de valores y filosofía de la vida, sentimientos de impotencia o desesperanza, miedo a lo desconocido, miedo a la pérdida del control propio y del medio y respuestas depresivas, de negación o de agresividad.
2- Área familiar: los problemas más relevantes están vinculados a la pérdida de la homeostasis familiar anterior. Pérdida del rol y los cambios en el rol que deben asumir los demás miembros de la familia.
3- Área social: los problemas más relevantes están centrados en la pérdida de relaciones y lazos afectivos, cambios en la utilización del tiempo libre y modificaciones en la calidad o cantidad de interacciones sociales.
PROPUESTAS EDUCATIVAS Y DE INVESTIGACIÓN
PROPUESTAS EDUCATIVAS
1.- Que se realicen cursos para diabéticos en los cuales se les enseñe la importancia de llevar la dieta y como prevenir el pie diabético.
2.- Que cada trabajador de la salud sea un orientador sobre prevención de la diabetes y medidas de prevención de pie diabético.
3.- Crear espacios de discusión y capacitación con estrategias que permitan generar un frente común contra la diabetes.
4.- Crear conciencia para entender que los factores de riesgo (antecedentes familiares, obesidad, intolerancia a la glucosa y sedentarismo, entre otros), son modificables y constituyen la base para prevenir la diabetes y sus complicaciones.
PROPUESTAS DE INVESTIGACIÓN
1.- Que se realicen trabajos de investigación en el cual se evalúe el nivel de conocimientos y práctica del autocuidado dirigido al paciente diabético y sus familiares.
2.- Evaluar el nivel de conocimientos de todo el personal de la salud en cuanto a la etiología, diagnostico y tratamiento, así como todas las posibles complicaciones derivadas de la diabetes.
BIBLIOGRAFIA
American Diabetes Association. Implication of the Diabetes Control and Complications Trial. Clinical. Practice Recomendations.Diabetes care 2000
American Diabetes Association. Implications of the United Kingdom Prospective Diabetes Study.Clinical Practice. Recomendations.Diabetes care 2000
American Diabetes Association. Report of the Expert comité on the diagnosis and classification of Diabetes Mellitus Diabetes Care 1997
Americam Diabetes Association.Standards of Medical Care For Patients with Diabetes Mellitus. Clinical Practice Recommendations. Diabetes Care 2000
Europa Diabetes Policy Group 1999. A destop guide for the management of type 2 diabetes mellitus. Diabet Med 1999
Gaster B, Hirsch b. The effet of improved Glycemic control on complications on type 2 Diabetes. Arch Intern Med 1998
Grupo de estudio de la diabetes en atención primaria de salud (GEDAPS) Guía de tratamiento de la diabetes Tipo 2 en atención primaria. Madrid: Ediciones Harcourt S. A; 1999
Klein R, BEK, Moss Se of glicemia control to diabetic microvascular complications in diabetes mellitus. Ann Internet Med. 1996
Manual Merck Décima Edición ( Edicion del centenario )
Mosby's Medical,Nursing and Allied Health Dicionary.
Conceptos Actuales acerca de la Diabetes. Joslin EP. 10ª ed. México: Editorial Interamericana.
Guía para el manejo integral del paciente diabético. Dr. Melchor Alpizar Salazar.
Educación, base primordial del tratamiento en atención integral del paciente diabético. Ovalle Berumen JF. 2ª ed. Lerman 1 Editorial McGraw-Hill Interamericana, 1988
Citas de internet:
www.anatomia.tripod.com/pancreas.htm.
www.nlm.nih.gov/medlineplus/spanish/ency/article/001214.htm.
http://piediabetico.net.
Figura 2.- Proceso de regulación del azúcar en la sangre.
Figura 9.- Bypass duodeno-yeyunal laparoscópico.
Figura 8.- Clasificación de Wagner.
Figura 7.- Prueba de 10 puntos.
Figura 5.- Pie de Charcot.
Figura 4.- Atrofia del pie diabético.
Figura 3.- Lesión del pie
Figura 6.- Infección del pie diabético.
Descargar
| Enviado por: | Jesus |
| Idioma: | castellano |
| País: | México |
