Ecología y Medio Ambiente
Detergentes y jabones
Tema: Detergentes y jabones.
Introducción
¿Cómo limpia un jabón?
El agua sola no es capaz de disolver la grasa que compone y contiene la suciedad. Un jabón limpia debido a la capacidad que tiene para formar emulsiones con los materiales solubles en grasas; las moléculas de jabón rodean a la suciedad hasta incluirla en una envoltura denominada micela, la parte apolar de la molécula de jabón se disuelve en la gotita de grasa mientras que los grupos carboxilato, polares, se orientan hacia la capa de agua que los rodea. La repulsión entre cargas iguales evita que las gotas de grasa se unan de nuevo. Se forma así una emulsión que se puede separar de la superficie que se está lavando.
Muchas veces hemos visto maravillados cómo en una fría mañana invernal los patos nadan en el estanque sin una aparente preocupación por ser mojados por las frías aguas; cuando por fin dejan el estanque, simplemente se sacuden de las gotas superficiales y su plumaje queda tan seco como antes de su contacto con el agua. Al observar las aguas estancadas es frecuente ver insectos que con gran seguridad van y vienen corriendo sobre la superficie del agua. Ambos fenómenos tienen que ver con el hecho muy conocido de que el agua y el aceite no se mezclan. Tanto el cuerpo del insecto como el plumaje de los patos se encuentran cubiertos por una capa de grasa que los hace impermeables.
Cuando la ropa u otros objetos se manchan con grasa y tratamos de lavarlos con agua sucederá lo mismo que con el plumaje de los patos: el agua no moja a la mancha de aceite. El agua, por lo tanto, no sirve para limpiar objetos sucios con aceites o grasas; sin embargo, con la ayuda de jabón o detergente sí podemos eliminar la mancha de grasa. El efecto limpiador de jabones y detergentes se debe a que en su molécula existe una parte lipofílica por medio de la cual se unen a la grasa o aceite, mientras que la otra parte de la molécula es hidrofílica, tiene afinidad por el agua, por lo que se une con ella; así, el jabón toma la grasa y la lleva al agua formando una emulsión
Saponinas.
Antes de que el hombre creara la gran industria del jabón se usaban jabones naturales llamados saponinas (nombre derivado del latín sapo, jabón) y conocidos por los mexicanos como amole. Muchas raíces y follaje de plantas tienen la propiedad de hacer espuma con el agua, por lo que se han utilizado desde la Antigüedad para lavar ropa. Los pueblos prehispánicos del centro de México llamaban amole a estas plantas y eran sus jabones. Aun en la actualidad en muchas comunidades rurales se emplea el amole tanto para lavar ropa fina, como para evitar que se deteriore, ya que es un detergente neutro perfectamente degradable.
Las saponinas se han usado también como veneno de peces, macerando en agua un poco del órgano vegetal que lo contiene, con la ventaja de que los peces muertos por este procedimiento no son tóxicos.
Las saponinas producen hemólisis a grandes diluciones y están constituidas por grandes moléculas orgánicas, como esteroides o triterpenos, unidas a una o varias azúcares, por lo que contienen los elementos necesarios para emulsionar la grasa: una parte lipofílica, que es el esteroide o triterpeno, por medio del cual se unirá a la grasa, y una parte hidrofílica, que es el azúcar, por medio de la cual se unirá al agua.
Entre las saponinas de naturaleza esteroidal son muy importantes los glicósidos cardiacos, obtenidos de la semilla de la dedalera o Digitalis purpurea. El extracto obtenido de estas semillas, que contienen una mezcla de saponinas, es muy útil en el tratamiento de enfermedades del corazón. Sin embargo, un exceso de estas sustancias es peligroso y puede causar incluso la muerte. Debido a esto, las infusiones de dedalera se utilizaron en la Edad Media en los juicios de Dios.
Los glucósidos cardiacos se encuentran no sólo en la dedalera, sino que hay otras plantas que también las contienen, tales como las distintas especies de la familia Asclepidacea.
Esta familia de plantas es rica en ellos, y su principal característica es la producción de un jugo lechoso cuando se le cortan hojas o tallos. Ha adquirido notoriedad por ser las plantas que alimentan a la mariposa monarca en su estado larvario. De esta planta las mariposas toman los glicósidos cardiacos que la volverán tóxica y por consiguiente desaniman a las aves a que las consuman como alimento.
Enzimas
Estos materiales adquirieron gran popularidad en Estados Unidos y Europa en la década de los sesenta debido a su facultad de eliminar manchas proteicas o carbohidratos, aun en el remojo. Los detergentes con esta formulación son capaces de eliminar manchas de sangre, huevo, frutas, etcétera.
Con todo, estos detergentes han producido problemas de salud en los obreros que trabajan en su elaboración. Por suerte, hasta ahora no los han provocado en las amas de casa.
El problema con los obreros se debió principalmente a que los detergentes producen polvo que, al ser aspirado, pasa a los pulmones. Esto se ha resuelto fabricando detergentes con gránulos mayores, para que no produzcan polvo.
Los fabricantes de detergentes de Europa y Japón están poniendo enzimas en la mayor parte de sus productos.
Entre las sustancias que se agregan a los detergentes para mejorar sus características se encuentran ciertas sustancias que protegen a las telas contra la fijación del polvo del suelo o el atmosférico. Estas sustancias, que mantienen a las telas limpias por más tiempo al evitar la reimplantación del polvo, son sin duda de gran utilidad, pues evitan trabajo y deterioro de la tela.
Una sustancia con esas propiedades es la carboxi-metilcelulosa, que es eficiente en algodón y otras telas celulósicas, pero falla con telas sintéticas.
Para estas últimas es útil el uso de 1 a 6% de ácido poliacrílico o de poliacrilatos.
Los ácidos carboxílicos secuestran la dureza del agua reaccionando con las sales metálicas presentes en esas aguas.
El tripolifosfato de sodio es un excelente secuestrante y por muchos años se ha usado con óptimos resultados. Por desgracia en los Estados Unidos se empezaron a observar efectos de eutrofisación de las aguas, por lo que su uso está siendo severamente restringido.
Lo mismo está sucediendo en Europa, donde también se han descubierto daños por eutrofisación, fenómeno que consiste en el aumento de nutrientes a un ritmo excesivo, por lo que al descomponerse la materia prima orgánica que ingresa (detergentes), disminuye el oxígeno disuelto, alterando la vida en las aguas.
Saponificación
Los jabones se preparan por medio de una de las reacciones químicas más conocidas: la llamada saponificación de aceites y grasas.
Los aceites vegetales, como el aceite de coco o de olivo, y las grasas animales, como el sebo, son ésteres de glicerina con ácidos grasos. Por eso cuando son tratados con una base fuerte como sosa o potasa se saponifican, es decir producen la sal del ácido graso conocida como jabón y liberan glicerina. En el caso de que la saponificación se efectúe con sosa, se obtendrán los jabones de sodio, que son sólidos y ampliamente usados en el hogar. En caso de hacerlo con potasa, se obtendrán jabones de potasio, que tienen consistencia líquida.
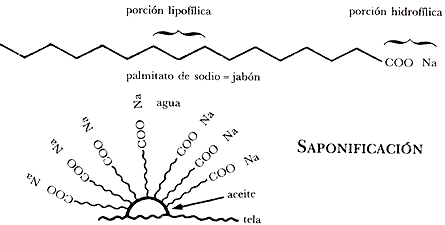
Con frecuencia se agrega brea en el proceso de saponificación obteniéndose así jabones en los que, junto con las sales de sodio de ácidos grasos, se tendrá la sal de sodio de ácidos resínicos, lo que los hace más solubles y más apropiados para lavar ropa. Evidentemente se podrán obtener sales de ácidos grasos con otros metales, especialmente con calcio, ya que el hidróxido más abundante y barato es la cal, Ca(OH)2. Ahora bien, si la saponificación se hace con cal, el producto será el jabón de calcio, Ca(OCOR)2. El problema es que este jabón es un sólido duro e insoluble, por lo que no sirve para los fines domésticos a los que se destinan los jabones de sodio.
Los jabones de sodio tienen un amplio uso en nuestra civilización, por lo que la industria jabonera es una de las más extensamente distribuidas en el mundo entero.
Fabricación del jabón
El proceso de fabricación de jabón es, a grandes rasgos, el siguiente: se coloca el aceite o grasa en un recipiente de acero inoxidable, llamado paila, que puede ser calentado mediante un serpentín perforado por el que se hace circular vapor. Cuando la grasa se ha fundido ±8Oº, o el aceite se ha calentado, se agrega lentamente y con agitación una solución acuosa de sosa. La agitación se continúa hasta obtener la saponificación total. Se agrega una solución de sal común (NaCl) para que el jabón se separe y quede flotando sobre la solución acuosa.
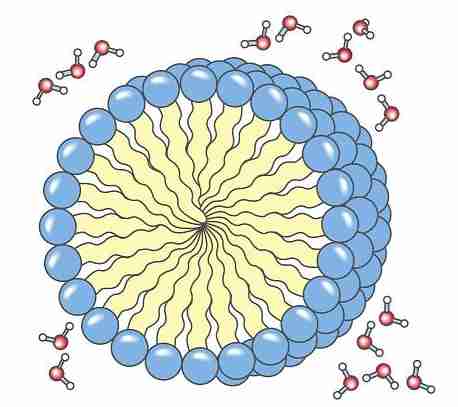
Se recoge el jabón y se le agregan colorantes, perfumes, medicinas u otros ingredientes, dependiendo del uso que se le quiera dar. El jabón se enfría y se corta en porciones, las que enseguida se secan y prensan, dejando un material con un contenido de agua superior al 25%.
Los jabones son inefectivos para la limpieza en agua dura ( agua que contiene sales de metales pesados, especialmente hierro y calcio), éstos precipitan en forma de sales insolubles (costra de las bañeras). En cambio, las sales de hierro y calcio de los sulfatos ácidos de alquilo son solubles en agua y las sales sódicas de estos materiales, conocidas como detergentes (agentes limpiadores), son efectivas incluso en aguas duras.
Tales detergentes contienen cadenas carbonadas rectas, análogas a las de las grasas naturales. Se metabolizan mediante bacterias en plantas de tratamiento de aguas residuales y se conocen con el nombre de “detergentes biodegradables”.
Jabón R-COO- Na+ Detergente R-OSO3- Na+
Aunque los detergentes sintéticos varían considerablemente en cuanto a sus estructuras, sus moléculas tienen una característica común que comparten con el jabón ordinario: tienen una cadena apolar muy larga, soluble en grasas, y un extremo polar, soluble en agua.
Los detergentes actuales contienen diferentes aditivos, fosfatos que exaltan la limpieza, agentes espumantes, blanqueantes, etc. siempre intentando satisfacer la demanda de los consumidores.
Detergentes
Los primeros detergentes sintéticos fueron descubiertos en Alemania en 1936, en lugares donde el agua es muy dura y por lo tanto el jabón formaba natas y no daba espuma. Los primeros detergentes fueron sulfatos de alcoholes y después alquilbencenos sulfonados, más tarde sustituidos por una larga cadena alifática, generalmente muy ramificada.
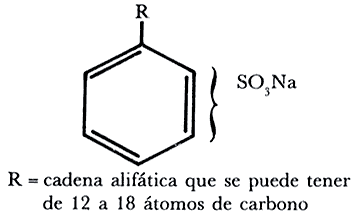
Los resultados fueron positivos, pues al usarse en agua muy dura siguieron dando abundante espuma por no formar sales insolubles con calcio y otros constituyentes de las aguas duras.
Dado que los detergentes han resultado ser tan útiles por emulsionar grasas con mayor eficiencia que los jabones, su uso se ha popularizado, pero, contradictoriamente, han creado un gran problema de contaminación, ya que muchos de ellos no son degradables. Basta con ver los ríos rápidos que llevan las aguas municipales para darse cuenta de cómo se elevan en ellos verdaderas montañas de espuma. Para evitar esto, se han hecho esfuerzos por sustituir la cadena lateral (R) ramificada por una cadena lineal, la que sí sería biodegradable. Los detergentes son muy variados, y los hay para muy diversos usos; simplemente, para ser efectivos en las condiciones de temperatura que se acostumbran en el lavado industrial de los distintos pueblos de la Tierra, tiene que variar su formulación.
El lavado industrial en Europa se acostumbra hacer a alta temperatura, entre 90 y 95° Por su parte, en los Estados Unidos se hace entre 50 y 60°, mientras que en México se realiza a temperatura ambiente.
Las diferentes condiciones de temperatura en las que se realiza el lavado trae problemas a los fabricantes de detergentes. Éstos deben estar seguros de que el detergente se disuelve en agua a la temperatura adecuada. Los detergentes más comunes en los Estados Unidos no son fácilmente solubles en frío. Los agentes blanqueadores como el perborato, que funciona bien en caliente, cuando se utiliza en frío tiene que ser reforzado con activadores, pues en agua tibia los blanqueadores pierden eficiencia.
¿Debido a que limpia un jabón?
Un jabón limpia debido a la capacidad que tiene para formar emulsiones con los materiales solubles en grasas
¿A que se le denomina micela?
A las moléculas de jabón que rodean a la suciedad hasta incluirla en una envoltura
¿A que se debe el efecto limpiador de jabones y detergentes?
Se debe a que en su molécula existe una parte lipofílica por medio de la cual se unen a la grasa o aceite, mientras que la otra parte de la molécula es hidrofílica, tiene afinidad por el agua, por lo que se une con ella; así, el jabón toma la grasa y la lleva al agua formando una emulsión.
¿Qué son las saponinas?
Antes de que el hombre creara la gran industria del jabón se usaban jabones naturales llamados saponinas (nombre derivado del latín sapo, jabón)
¿Por que nombre conoce el mexicano a las saponinas?
Conocidos por los mexicanos como amole
¿Qué son las enzimas?
Son materiales que adquirieron gran popularidad en Estados Unidos y Europa en la década de los sesenta debido a su facultad de eliminar manchas proteicas o carbohidratos, aun en el remojo.
¿Qué es el carboxil - meticelulosa?
Sustancia, que mantienen a las telas limpias por más tiempo al evitar la reimplantación del polvo, son sin duda de gran utilidad, pues evitan trabajo y deterioro de la tela.
¿Qué es la saponificación?
Una de las reacciones químicas más conocidas para preparar jabones a base de aceites y grasas
¿Cuándo se obtienen jabones de sodio?
En el caso de que la saponificación se efectúe con sosa, se obtendrán los jabones de sodio, que son sólidos y ampliamente usados en el hogar.
¿Cuándo se obtienen jabones de potasio?
En caso de hacerlo con potasa, se obtendrán jabones de potasio, que tienen consistencia líquida.
¿Cuáles con las dos bases fuertes con que son tratados los esteres de glicerina con ácidos grasos para formar jabón?
Potasa y sosa
¿A que se le considera agua dura?
Agua que contiene sales de metales pesados, especialmente hierro y calcio
¿Cuál es la característica que comparten los detergentes y los jabones?
Tienen una cadena apolar muy larga, soluble en grasas, y un extremo polar, soluble en agua.
¿Dónde fueron descubiertos los primeros detergentes sintéticos?
Los primeros detergentes sintéticos fueron descubiertos en Alemania en 1936, en lugares donde el agua es muy dura y por lo tanto el jabón formaba natas y no daba espuma
¿Cuales fueron los primeros detergentes sintéticos?
Los primeros detergentes fueron sulfatos de alcoholes y después alquilbencenos sulfonados, más tarde sustituidos por una larga cadena alifática, generalmente muy ramificada.
Descargar
| Enviado por: | Dagon |
| Idioma: | castellano |
| País: | México |
