Biología, Botánica, Genética y Zoología
Angiogénesis
Concepto
El proceso de formación de nuevos vasos a partir de los capilares preexistentes es lo que se denomina angiogénesis. La angiogénesis es un proceso complejo que involucra a distintas células, componentes solubles y factores de la matriz extracelular y tiene gran importancia en una gran variedad de procesos fisiológicos y patológicos del organismo. La regulación de la angiogénesis se lleva a cabo mediante un perfecto equilibrio entre la producción y la liberación de diversos factores estimulantes e inhibidores, que varían en función de las necesidades y el tipo de tejido. Un número elevado de enfermedades se caracteriza por alteraciones del proceso angiogénico, tanto por insuficiencia como por exceso de angiogénesis. Hace ya más de un siglo que se observó que la proliferación de los vasos sanguíneos era necesaria para el crecimiento tumoral. El tratamiento antiangiogénico realizaría una acción antitumoral de forma indirecta mediante la inhibición de la vascularización del tumor e impidiendo que se le aporten los nutrientes necesarios para su crecimiento y desarrollo.
Normalmente, las inhibidoras predominan, bloqueando el crecimiento. Si surge la necesidad de desarrollar nuevos vasos sanguíneos, las activadoras de la angiogénesis se incrementan en número y las inhibidoras disminuyen. Esto provoca el crecimiento y la división de células vasculares endoteliales y, finalmente, la formación de nuevos vasos sanguíneos.
Este mecanismo requiere de eventos complejos que incluyen moléculas proangiogénicas y antiangiogénicas. Dentro de los principales factores angiogénicos estudiados en la actualidad están el factor de crecimiento fibroblástico (FGF) y el factor de crecimiento del endotelio vascular (VEGF). De manera reciente se han hecho grandes esfuerzos por aplicar estos factores en el tratamiento de la cardiopatía isquémica avanzada y crónica, así como en la enfermedad arterial periférica.
Mecanismos
La angiogénesis requiere de una serie procesada de eventos que incluye: la migración y proliferación de células endoteliales dentro y fuera de la microvasculatura original, el rompimiento de membranas basales, y finalmente la expresión controlada de enzimas proteolíticas que pueden degradar matriz extracelular, reensamblar nueva matriz extracelular, y formar tubos endoteliales.
Se ha observado que bajo ciertas circunstancias, un proceso angiogénico insuficiente puede ser causa por ejemplo de úlceras que no cicatrizan, o mayor extensión del infarto del miocardio, y por otro lado, muchas patologías pudieran estar complicadas por una angiogénesis no regulada como el cáncer, la retinopatía diabética, y la misma aterosclerosis. El proceso normal de angiogénesis incluye moléculas proangiogénicas y antiangiogénicas. Dentro de las moléculas angiogénicas principales que se conocen en la actualidad están: Factor de crecimiento fibroblástico (FGF), factor de crecimiento endotelial vascular (VEGF), factor alfa de necrosis tumoral, factor beta de transformación del crecimiento, factor de crecimiento derivado de plaquetas y la angiogenina. También es importante señalar, que la hipoxia tisular es una de las mayores fuerzas que estimulan la angiogénesis.
El factor de crecimiento fibroblástico ácido (aFGF o FGF-1) y FGF básico (bFGF, o FGF-2) son polipéptidos de 18 kilodaltones que actúan como mitógenos potentes para las células endoteliales y las del músculo liso. Se ha observado que estos factores tienen gran afinidad por la heparina y el sulfato de heparán.
El VEGF es miembro de una familia de proteínas relacionadas estructuralmente que actúan como ligandos de la familia de receptores del VEGF (VEGFR). El VEGF ejerce sus efectos sobre el desarrollo de nuevos vasos sanguíneos (angiogénesis) y la supervivencia de los vasos sanguíneos inmaduros (mantenimiento vascular) al unirse y activar dos receptores de membrana tirosin-kinasa relacionados estructuralmente, el VEGFR-1 y el VEGFR-2, que son expresados por las células endoteliales de la pared vascular (Tabla 1). La unión del VEGF a estos receptores inicia una cascada de señales que finalmente estimula el crecimiento, la supervivencia y la proliferación de las células del endotelio vascular. Las células desempeñan funciones en procesos tan variados como la vasoconstricción/vasodilatación y la presentación de antígenos y son componentes esenciales de los vasos sanguíneos, ya sean capilares, venas o arterias. Por lo tanto, al estimular las células endoteliales, el VEGF desempeña un papel central en la angiogénesis.
Tabla 1. Especificidad del receptor de los ligandos de VEGF y efectos biológicos.
|
|
|
|
| Miembro de la familia | Receptor | Función |
|
|
|
|
|
|
|
|
| VEGF (VEGF-A) | VEGFR-1, VEGFR-2, | Angiogénesis, |
| VEGF-B | VEGFR-1 | No establecida |
| VEGF-C | VEGFR-2, VEGFR-3 | Linfangiogénesis |
| VEGF-D | VEGFR-2, VEGFR-3 | Linfangiogénesis |
| VEGF-E (factor virico) | VEGFR-2 | Angiogénesis |
| PIGF | VEGFR-1, | Angiogénesis |
El VEGF es crítico para el desarrollo
El VEGF es esencial para establecer un sistema vascular funcional durante la embriogénesis y al comienzo del desarrollo postnatal, pero tiene una actividad fisiológica limitada en los adultos. Estudios en ratones han demostrado que:
-
La alteración dirigida de una de las dos copias del gen del VEGF conlleva la muerte del embrión.
-
La inactivación del VEGF durante el comienzo del desarrollo postnatal también es letal.
-
La alteración del VEGF en ratones adultos no se ha asociado a ninguna anomalía aparente porque su papel se limita al desarrollo folicular, la cicatrización de heridas y el ciclo reproductivo femenino.
-
La angiogénesis limitada en los adultos implica que la inhibición del VEGF es una estrategia terapéutica factible.
El VEGF es el mediador clave de la angiogénesis
La expresión del VEGF es estimulada por múltiples factores proangiogénicos, incluidos el factor de crecimiento epidérmico, el factor de crecimiento fibroblástico básico, el factor de crecimiento derivado de las plaquetas y la interleuquina-1a. Los niveles de VEGF también están regulados directamente por condiciones ambientales como el pH, la presión y los niveles de oxígeno. El impacto global de estos diferentes factores es la estimulación, mediada por el VEGF, de la expresión de factores importantes para la angiogénesis, incluidas las proteínas anti-apoptóticas, las moléculas de adhesión celular y las metaloproteinasas de la matriz (MMP).
El VEGF y el crecimiento tumoral
El VEGF ha sido un centro de atención para la investigación de la angiogénesis tumoral, que es esencial para el crecimiento del tumor por encima de un diámetro de 2 mm. Se ha comprobado que muchos tumores expresan VEGF, y que este factor tiene una función crítica en el desarrollo y mantenimiento de una red vascular tumoral, que a su vez promueve su crecimiento y la formación de metástasis. El VEGF contribuye al crecimiento tumoral de varias formas:
-
El VEGF estimula la angiogénesis tumoral, permitiendo que los tumores tengan acceso al oxígeno y los nutrientes que necesitan para crecer y metastatizar.
-
El VEGF desempeña una importante función en el mantenimiento del sistema vascular del tumor al evitar la apoptosis de las células inmaduras del endotelio.
-
El VEGF tiene un papel en la formación de vasos linfáticos nuevos que son una vía de metastatización tumoral.
-
El VEGF evita la respuesta inmunitaria normal frente a los tumores al inhibir la maduración de las células dendríticas
En ausencia de un sistema vascular, los tumores se mantienen pequeños (1-2 mm). Los tumores malignos experimentan “una activación angiogénica”, que altera el equilibrio entre los factores proangiogénicos y antiangiogénicos, normalmente aumentando la segregación de factores de crecimiento.
Muchos factores de crecimiento, además del pH bajo y los niveles bajos de oxígeno que se encuentran en los tumores, estimulan la expresión del VEGF, que luego puede activar la expresión de otros factores involucrados en la angiogénesis como las MMPs y las moléculas de adhesión celular. De esta forma el VEGF actúa como el mediador clave de la angiogénesis tumoral, estimulando el crecimiento de nuevos vasos sanguíneos desde los capilares adyacentes, permitiendo que los tumores tengan acceso al oxígeno y a los nutrientes que necesitan para crecer y metastatizar.
Los científicos han estado trabajando durante años para entender los mecanismos que controlan la angiogénesis. Han descubierto que tanto los tejidos sanos como los tumores producen naturalmente proteínas y moléculas que promueven o inhiben la angiogénesis. Se han realizado experimentos en ratones para determinar si la angiogénesis es desencadenada por el tumor o por el tejido huésped que lo rodea. Los hallazgos probaron que los tumores inician la angiogénesis al liberar factores de crecimiento en los tejidos circundantes, en un sentido ordenando al tejido a comenzar a formar vasos sanguíneos. Para que un tumor crezca, tiene que liberar más factores proangiogénicos que factores inhibidores en el tejido circundante.
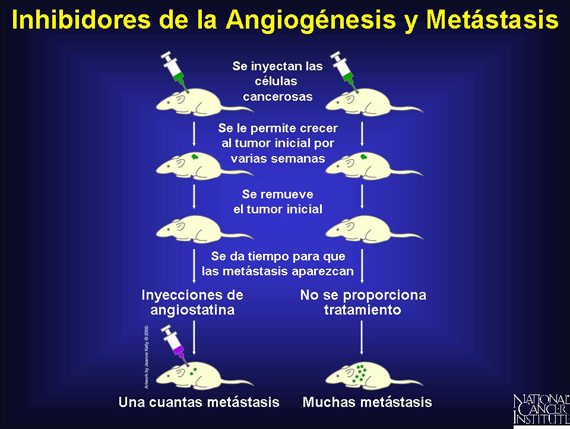
El hecho que los tumores también produzcan inhibidores angiogénicos resulta ser muy importante para explicar la metástasis, que es la propagación del cáncer a otras partes del cuerpo y la principal razón de las muertes relacionadas con esta enfermedad. Frecuentemente, metástasis pequeñas, microscópicas, en áreas del cuerpo alejadas del tumor primario, permanecen inactivas durante años y empiezan a crecer solo después que el tumor primario es extirpado. Esto sucede porque el tumor primario ha estado liberando inhibidores angiogénicos en el torrente sanguíneo y cuando estos inhibidores desaparecen los tumores microscópicos empiezan a crecer. Los investigadores esperan que evitando la angiogénesis ellos puedan evitar que estas metástasis microscópicas crezcan. Además, si un tumor no se ha propagado a otras áreas y ha sido tratado efectivamente con agentes antiangiogénicos es menos probable que ocurra la metástasis, debido a que hay menos vasos sanguíneos disponibles para que las células cancerosas se diseminen desde el tumor.
Aplicaciones clínicas
Las aplicaciones clínicas de la angiogénesis han tomado en la actualidad 3 direcciones:
Diagnóstico y pronóstico de procesos patológicos.
Aceleración terapéutica durante la reparación tisular.
Inhibición terapéutica.
La cuantificación de la angiogénesis puede:
-
Predecir la ocurrencia de metástasis.
-
Predecir la recurrencia de un tumor.
-
Diferenciar procesos neoformativos.
-
Predecir la involución de las lesiones.
Aceleración terapéutica
Se han realizado estudios preclínicos en los cuales la aceleración de la angiogénesis, en pacientes con úlcera gástrica o duodenal, causada por drogas (antiinflamatorias no esteroideos) refractarias al tratamiento convencional, acelera el proceso de curación tras la administración de FGF b por vía oral.
Principios generales de la terapia antiangiogénica
Los inhibidores de la angiogénesis no deben causar supresión medular, síntomas gastrointestinales o pérdida del cabello.
El efecto terapéutico aparece en meses, 1 año o más.
La resistencia a la drogas antian-giogénesis no produce efectos adversos (angiogénesis).
La combinación con citotóxicos es más efectiva.
Es principalmente dirigida a pequeños grupos de células endoteliales vasculares, emigrantes o proliferantes.
La mayoría de los tumores teóricamente pueden regresar después del tratamiento antiangiogénico. Sin embargo, este ofrece mayor seguridad si el tumor es menor que 2 mm y su crecimiento es aún angiogénesis independiente.
El tumor permanecerá inalterable el tiempo que dure el tratamiento, de ser este interrumpido, las células tumorales reiniciarán su expansión, pues la terapia antiangiogénica no crea poblaciones resistentes.
Se concluye que el análisis histológico de muchos tumores revela la presencia de numerosos vasos de neoformación, íntimamente asociados con el tejido tumoral. Estos vasos constituyen un elemento esencial del estroma tumoral y por lo tanto la densidad vascular puede constituir un factor pronóstico importante para la evolución de la enfermedad neoplásica, independientemente de otros factores. Por estas razones, la angiogénesis es considerada una etapa esencial de la diferenciación y organización tumoral.
Para entender mejor::
Inhibición VEGF y angiogénesis contra cáncer: http://www.youtube.com/watch?v=S8mpYCC5zJA
Angiogénesis y su papel en el desarrollo del cáncer: http://www.youtube.com/watch?v=Hk5vg8eloiI
FUENTES:
Arch Cardiol Mex. 2003 Apr-Jun;73 Suppl 1:S109-11.
OncoLog, junio 2004, Vol. 49, No. 6,
Tratado de fisiología médica, décima edición,Mc Graw- Hill Guyton- Hall
http://www.cancer.gov/espanol/cancer/entendiendo/angiogenesis/Slide6
http://www.doyma.es/revistas/ctl_servlet?_f=7014&articuloid=13076512&revistaid=36
http://bvs.sld.cu/revistas/ibi/vol20_3_01/ibi10301.htm
http://fundacionannavazquez.wordpress.com/2007/10/16/angiogenesis-2/
http://youtube.com
Descargar
| Enviado por: | ANIMSAY |
| Idioma: | castellano |
| País: | España |
