Química
Aminoácidos y proteinas
INTRODUCCION
Los aminoácidos son sustancias cristalinas, casi siempre de sabor dulce; tienen carácter ácido como propiedad básica y actividad óptica; químicamente son ácidos carbónicos con, por lo menos, un grupo amino por molécula, 20 aminoácidos diferentes son los componentes esenciales de las proteínas. Aparte de éstos, se conocen otros que son componentes de las paredes celulares. Las plantas pueden sintetizar todos los aminoácidos, nuestro cuerpo solo sintetiza 16, aminoácidos, éstos, que el cuerpo sintetiza reciclando las células muertas a partir del conducto intestinal y catabolizando las proteínas dentro del propio cuerpo.
Los aminoácidos son las unidades elementales constitutivas de las moléculas denominadas proteínas. Son pues, y en un muy elemental símil, los "ladrillos" con los cuales el organismo reconstituye permanentemente sus proteínas específicas consumidas por la sola acción de vivir.
Las proteínas que son los compuestos nitrogenados más abundantes del organismo, a la vez que fundamento mismo de la vida. En efecto, debido a la gran variedad de proteínas existentes y como consecuencia de su estructura, las proteínas cumplen funciones sumamente diversas, participando en todos los procesos biológicos y constituyendo estructuras fundamentales en los seres vivos. De este modo, actúan acelerando reacciones químicas que de otro modo no podrían producirse en los tiempos necesarios para la vida (enzimas), transportando sustancias (como la hemoglobina de la sangre, que transporta oxígeno a los tejidos), cumpliendo funciones estructurales (como la queratina del pelo), sirviendo como reserva (albúmina de huevo), etc.
Los alimentos que ingerimos nos proveen proteínas. Pero tales proteínas no se absorben normalmente en tal constitución sino que, luego de su desdoblamiento ("hidrólisis" o rotura), causado por el proceso de digestión, atraviesan la pared intestinal en forma de aminoácidos y cadenas cortas de péptidos, según lo que se denomina " circulación entero hepática".
OBJETIVOS
1. Reconocer la presencia de algunos aminoácidos en las proteínas.
2. Adquirir información sobre algunas propiedades físicas y químicas de aminoácidos
3. Conocer algunas propiedades de las proteínas.
MARCO TEORICO
Los grupos R de los aminoácidos son diversos, por lo que pueden reaccionar de varias maneras. Así, aminoácidos como al ácido aspártico y el ácido glutámico poseen un segundo ácido carboxílico, la lisina, posee un segundo grupo amino. Además, otros aminoácidos con grupos laterales reactivos son: la cisteína (-SH), la arginina (guanidio), la histidina (imidazol), la serina, la treonina y la tirosina (alcoholes), la asparagina y la glutamina (amidas), la metionina (un tioeter) y el triptofano (indol).
La reactividad de estos grupos funcionales ha sido aprovechada de diversas maneras en el estudio y análisis de las proteínas. Como un ejemplo, se menciona el caso de las lisinas, que reaccionan con aldehídos (carbonilo) para formar bases de shift, esto se ha aprovechado para producir un papel aldehídico, al que las proteínas se unen covalentemente , lo que permite fijarlas para su estudio.
También es posible hacer reaccionar las cisteínas o las lisinas con diversos grupos químicos reactivos presentes en resinas, con lo que es posible unir proteínas a materiales para columnas de cromatografía y fabricar columnas con enzimas inmovilizadas, anticuerpos y receptores estere o selectivos para ligandos específicos.
Una tercera aplicación de la reactividad de los restos laterales de los aminoácidos está en identificar el tipo de aminoácidos involucrados directamente en cierta función de unas proteínas. Así. Por ejemplo, si un residuo de cisteína participa en el reconocimiento de un ligando específico, al modificar este residuo con metil-metano-tiosulfonato, la proteína pierde su actividad biológica. En cambio, si el metil-metano-tiosulfonato se añade cuando el ligando está presente, la presencia del ligando protege a la cisteína con la que interactúa y evita la pérdida de la función.
Además, las propiedades químicas de los aminoácidos ciertamente son aprovechadas por los sistemas vivos para realizar diferentes funciones.
PRESENTACION
En animales superiores, las proteínas son los compuestos orgánicos más abundantes, pues representan alrededor del 50% del peso seco de los tejidos. Desde el punto de vista funcional, su papel es fundamental. No existe proceso biológico alguno que no dependa de la presencia y/o actividad de este tipo de sustancias; las proteínas cumplen diferentes funciones: enzimas, hormonas, trasportadores, los anticuerpos, receptores de muchas células, etc.
Todas las proteínas contienen carbono, hidrógeno, oxígeno y nitrógeno y casi todas poseen también azufre. Si bien hay ligeras variaciones en diferentes proteínas, el contenido de nitrógeno representa, término medio, el 16% de la masa total de la molécula, lo cual permite calcular la cantidad de proteína existente en una muestra, por medición del N de la misma.
Debido a su gran tamaño, cuando se dispersa a estas moléculas en un solvente adecuado, forman obligadamente soluciones coloidales, con características especiales que las distinguen de las soluciones de moléculas pequeñas.
Por medio de la hidrólisis, las moléculas proteínicas son escindidas en sus monómeros, los aminoácidos. Y cientos o miles de estos aminoácidos pueden participar en la formación de la gran molécula polimérica de una proteína.
Los aminoácidos, como ya hemos comentado, son materia prima de proteínas y péptidos que cumplen diferentes funciones en nuestro organismo. No obstante, también pueden utilizarse como materia prima del metabolismo energético, de hecho, alrededor del 30% de los aminoácidos, pasan a una ruta metabólica que, después de eliminar el nitrógeno de la molécula, envía los productos desaminados al ciclo de Krebs.
REACCIONES DE LOS AMINOACIDOS
1. Reacción de la ninhidrina
ALBÚMINA:
Al agregarle 5 gotas de solución de ninhidrina calentado a ebullición durante 2-3 minutos se obtuvo un color púrpura, el cual significa prueba positiva para cualquier aminoácido.
Lisina + NaOH
El color fue mas intenso en la segunda experiencia ya que en la primera la estructura no se rompe y por lo tanto no se alcanza a percibir la coloración.
2. Reacción de millón
ALBÚMINA:
Al agregarle 5 gotas de reactivo de millón la solución obtuvo un precipitado con una coloración de amarillo claro.
Al calentar la solución no se obtuvo un cambio a simple vista, solo se observo que el reactivo de millón no actuó sobre la albúmina esto demuestra que es prueba negativa
La Albúmina, es un tipo de proteína simple, compuesta de carbono, hidrógeno, oxígeno, nitrógeno y un pequeño porcentaje de azufre.
La albúmina es coagulable por el calor, los ácidos minerales, el alcohol y el éter, y es soluble en agua y en disoluciones diluidas de sal. Es parte importante de la alimentación, y está presente en la clara de huevo, la leche, el músculo y el plasma sanguíneo; también se produce en las plantas, especialmente en las semillas. Puesto que la albúmina se coagula cuando se calienta a 71 °C, es útil para separar precipitados que enturbian disoluciones; así se aclaran disoluciones en el refinado del azúcar y otros procesos. La albúmina forma compuestos insolubles con muchas sales metálicas, como el cloruro de mercurio, el sulfato de cobre y el nitrato de plata.
TIROSINA:
Al agregarle 5 gotas de reactivo de millón la solución obtuvo un precipitado con una coloración de rojo ladrillo.
Al calentar la solución se no obtuvo un cambio en la coloración rojo ladrillo ya que las 2 sustancias se disolvieron dejando como resultado prueba positiva para reacción de aminoácidos.
La tirosina pertenece al grupo de aminoácidos con grupos polares sin carga. Participa como promedio en un 3,5% (en relación con todos los aminoácidos) de la composición de las proteínas. Los mamíferos pueden sintetizar la tirosina, un aminoácido no esencial, a partir de la fenilalanina, un aminoácido esencial que debe obtenerse a través de la alimentación.
FENILANINA:
Al agregarle 5 gotas de reactivo de millón la solución no presento un cambio notable en la coloración.
Al calentar la solución no se obtuvo un cambio a simple vista, solo se observo que el reactivo de millón no actuó sobre la fenilanina esto demuestra que es prueba negativa para reacción de aminoácidos.
La fenilanina forma parte del grupo de aminoácidos con grupos no polares (hidrófobos). Este aminoácido participa como promedio en un 3,5% (en relación con todos los aminoácidos) de la composición de las proteínas. El precursor para su biosíntesis es el corismato, una molécula en forma de anillo que se obtiene, entre otros, a partir de productos intermedios de la glicólisis. No puede ser sintetizado por los mamíferos, por lo que constituye uno de los aminoácidos esenciales. La ausencia de una enzima, la fenilalanina hidroxilasa, que cataliza la degradación de fenilalanina a tirosina, provoca una enfermedad denominada fenilcetonuria.
3. Reacción xantoproteica
ALBÚMINA:
Al agregarle 1ml de ácido nítrico concentrado
TIROSINA:
GLICINA:
4. Reacción sakaguchi
ALBÚMINA:
Al agregarle 1ml de NaOH y de 2 a 5 gotas de alfa-naftol la solución obtuvo un color blanco.
Al agregarle 4 a 5 gotas de agua de bromo, tomo una coloración roja en la parte superior y en la parte inferior un color blanco.
GLICINA:
Al agregarle 1ml de NaOH y de 2 a 5 gotas de alfa-naftol la solución obtuvo un color blanco.
Al agregarle 4 a 5 gotas de agua de bromo, tomo una coloración verde en la parte superior y en la parte inferior un color blanco.
ARGININA:
Al agregarle 1ml de NaOH y de 2 a 5 gotas de alfa-naftol la solución obtuvo un color blanco.
Al agregarle 4 a 5 gotas de agua de bromo, tomo una coloración roja en la parte superior y en la parte inferior un color blanco.
CREATINA:
Al agregarle 1ml de NaOH y de 2 a 5 gotas de alfa-naftol la solución obtuvo un color blanco.
Al agregarle 4 a 5 gotas de agua de bromo, tomo una coloración roja en la parte superior y en la parte inferior un color blanco.
REACCIONES GENERALES DE LAS PROTEÍNAS
1. Prueba del biuret para enlaces peptídicos
UREA:
A medida que fuimos calentando la urea hasta que se solidifico el papel tornasol presento un cambio de coloración de roja a azul, esto se debe a que la urea es básica y pasa a ser del grupo acido.
Al agregarle 2ml de NaOH lo que observamos fue los siguientes cambios:
Tubo 1. La solucion presento un cambio de incoloro a un color moradito.
Tubo 2. La solucion presento un cambio en la parte de arriba rojo y abajo incoloro.
Tubo 3. La solucion presento un cambio ya que quedo todo de color naranja
Al agregarle las 5 gotas de CUSO4
Tubo 1. La solucion presento un cambio a morado oscuro.
Tubo 2. La solucion presento un cambio a un morado mas oscuro.
Tubo 3. La solución presento un cambio a un morado un poco mas oscuro.
Todas las muestras dieron como resultado positivo
DISCUSION DE RESULTADOS:
La producen los péptidos y las proteínas, pero no los aminoácidos, ya que se debe a la presencia del enlace peptídico (- CO- NH -) que se destruye al liberarse los aminoácidos.
Cuando una proteína se pone en contacto con un álcali concentrado, se forma una sustancia compleja denominada biuret, de fórmula:
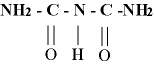
Que en contacto con una solución de sulfato cúprico diluida, da una coloración violeta característica. Entre las reacciones coloreadas específicas de las proteínas, que sirven por tanto para su identificación, destaca la reacción del Biuret.
2. Desnaturalización de proteínas
ALBUMINA
Amarillo, al agregar 0.5 ml de HCL se formo una estructura con forma de telaraña.
Al calentarse presento una precipitación de espuma y se solidifico, al ponerle el papel tornasol se puso de color rojo.
Al agregarle NaOH fue cambiando hasta llevarlo al PH mas cercano a la neutralidad es decir hasta que el papel tornasol cambio a azul.
CASEINA
Amarillo, al agregar 0.5 ml de NaOH no presento ningún cambio en la coloración ni en su estructura solo se presento un poco de burbujas.
Al calentar no paso nada pero al agregar el papel se puso azul.
Al agregar HCl 10 gotas cambio su PH a la neutralidad es decir el papel tornasol se puso de color rojo.
GELATINA
Polvito, se volvió una mezcla al agregársele agua.
DISCUSION DE RESULATADOS:
Se pudo observar que todas las muestras se coagularon, debido al gran tamaño de sus moléculas forman con el agua soluciones coloidales que pueden precipitar formándose coágulos al ser calentadas a temperaturas superiores a 70ºC o al ser tratadas con soluciones salinas, ácidos, alcohol, etc. La coagulación de las proteínas es un proceso irreversible y se debe a su desnaturalización por los agentes indicados que al actuar sobre la proteína la desordenan por destrucción de sus estructuras secundaria y terciaria.
CONCLUSIONES
*Las proteínas constituyen una de las moléculas más importantes en el organismo, ya que cumple muchas funciones.
*Las reacciones se utiliza en trabajos analíticos, así como en la visualización de las bandas de los aminoácidos después de su separación por electroforesis o por cromatografía.
*Las proteínas están constituidos por aminoácidos, por los cuales los métodos se basan en el reconocimiento de los aminácidos.
Descargar
| Enviado por: | Goyis |
| Idioma: | castellano |
| País: | Colombia |
