Industria y Materiales
Aguas residuales
4. INFORMACIÓN GENERAL
4.1. DEFINICIONES
4.1.1. AGUAS RESIDUALES INDUSTRIALES
Son las aguas residuales que provienen de las actividades de lavado de contenedores, lavado de piezas menores y del sistema de agua desionizada
4.1.2. Fosa de recolección de aguas RESIDUALES industriales.
Se llama fosa de recolección de aguas residuales industriales al recipiente ubicado entre los edificios de producción, identificación y almacén que tiene como objetivo recolectar las aguas residuales industriales que provienen de la Planta
4.1.3. pH
Es la medida de la concentración de los iones hidrógeno, que se expresa por el logaritmo común de la recíproca de la concentración de iones hidrógeno. (7.2)
pH = - log [H+]
4.2. ABREVIATURAS
4.2.1. pH: Potencial Hidrógeno
4.2.2. N: Normalidad
4.3. ASPECTOS GENERALES
Los procesos industriales, tales como lavados de equipos y accesorios generan aguas residuales. Estas deben ser analizadas para evitar que se realicen descargas a la red municipal que estén fuera de los parámetros permitidos.
5. MATERIALES Y EQUIPO
5.1. 2 buretas de 15 ml
5.2. 4 matraces Erlenmeyer de 250 ml
5.3. 2 vasos de precipitado de 500 ml
5.4. 2 probetas graduadas de 100 ml
5.5. 1 piseta de 250 ml
5.6. 2 embudos
5.7. Papel indicador de pH rango amplio (0-14)
5.8. Solución de NaOH 0.1 N
5.9. Solución de NaOH 50 %
5.10. Solución de HCl 0.1 N
5.11. Solución de HCl 30 %
5.12. Solución indicadora de azul de bromotimol
5.13. Agua Desionizada
5.14. Equipo de seguridad (Guantes, lentes de protección o careta y peto u overol y botas a prueba de ácidos o bases fuertes )
6. DESCRIPCIÓN
Las sustancias a emplear deben ser manejadas con la mayor de las precauciones con el objeto de evitar accidentes.
Antes de realizar cualquier actividad, el personal involucrado debe contar con el equipo de seguridad adecuado. El personal que realice las actividades de adición de sustancias a la cisterna, una vez determinada la cantidad a adicionar, debe contar con el equipo de protección requerido mencionado en el punto 5.14.
Las soluciones de HCl 0.1N y NaOH 0.1N se deberán solicitar al Laboratorio de Control de Calidad, y serán preparadas de acuerdo a sus procedimientos.
Las soluciones de NaOH 50% y HCl 30% son proporcionadas directamente por el proveedor.
6.1. REVISIÓN DIARIA
Revisar el nivel de la fosa por lo menos 2 veces al día (la frecuencia de la revisión depende de las actividades desarrolladas en la Planta).
Si el nivel ocupado en la fosa no rebasa 2/3 partes del volumen de la fosa (aproximadamente 10, 000 l) no realizar labor alguna.
6.1.3. Si el nivel rebasa 2/3 partes del volumen de la fosa, proceder de acuerdo al punto 6.2.
6.2. VACIADO DE LA FOSA
Abrir válvula de recirculación.
6.2.2. Cerrar válvula de descarga a la red de drenaje.
Arrancar bomba de recirculación y recircular 3 min.
Con el vaso de precipitados de 500 ml tomar muestra de agua residual en el punto de muestreo.
6.2.5. Determinar el pH con las tiras reactivas de pH (registrar en bitácora, ANEXO A).
6.2.6. Si los valores están dentro del rango de 6.0 a 9.0 de pH proceder de acuerdo al punto 6.2.9.
Si los valores de pH están por debajo de 6.0 proceder de acuerdo al punto 6.3.
6.2.8. Si los valores de pH están por arriba del 9.0 proceder de acuerdo al punto 6.4.
6.2.9. Abrir la válvula de descarga a la red de drenaje.
Cerrar la válvula de recirculación a la fosa.
6.2.11. Accionar el botón la bomba para descargar la fosa y pararla cuando la fosa este vacía.
6.3. NEUTRALIZACIÓN PARTIENDO DE UNA SOLUCIÓN ÁCIDA
Cuando el pH resulte menor a 6.0, se deberá proceder a determinar la cantidad de Hidróxido de Sodio a adicionar.
Preparar mesa de trabajo, soluciones y materiales.
6.3.2. Medir 100 ml de agua residual en una probeta y vertirla a un matraz Erlenmeyer.
Ajuste a “0” la bureta que contenga una solución de Hidróxido de Sodio (NaOH) 0.1 N.
6.3.4. Adicionar 5 gotas de azul de bromotimol al matraz Erlenmeyer y agite. La muestra presentará una coloración amarilla lo que indica que se encuentra en una fase ácida.
Proceder a neutralizar la muestra mediante la adición de NaOH 0.1N. La neutralización se detectará cuando exista un vire de color de amarillo a azul claro.
Nota:
La adición de NaOH 0.1 N debe ser gota a gota y agitando suavemente el matraz para detectar el momento exacto del vire de color. Si se adiciona rápidamente, el vire será a un azul intenso lo cuál indicará que la cantidad de NaOH 0.1N es mayor a la necesaria para la neutralización.
Una vez terminada la neutralización anotar los mililitros consumidos de solución en la bitácora (ANEXO A). En caso de no detectar el vire de color, se debe repetir la prueba. Los desechos de la titulación se deberán vaciar a la fosa de agua residual.
6.3.7. Registrar en bitácora (ANEXO A) el volumen total de agua residual presente en la fosa.
6.3.8. Aplicar la formula resultante del siguiente razonamiento:
Solución a emplear NaOH 50%
Densidad NaOH 50%=1.53
PM=39.998
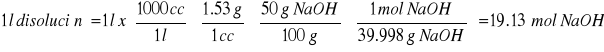
1 l disolución = 19.13 M
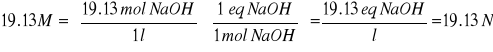
" 1 l disolución de NaOH 50%= 1l disolución NaOH 19.13 N
N1V1 = N2V2
(0.1)(w) = (19.13)(x)
![]()
Donde x= Volumen de NaOH al 50% en ml
w=Volumen de NaOH 0.1N en ml
100 ml ---- x
y ---- z
Z = ___y x____
100 ml
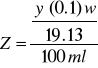
![]()
Donde:
Z = Son los litros de solución de NaOH al 50% necesarias para neutralizar el volumen total de agua residual presente en la cisterna
y = Es el volumen total de agua residual presente en la cisterna en litros
w= Son los mililitros de solución de NaOH 0.1 N resultantes de neutralizar una muestra de 100 ml de agua residual.
6.3.9. Añadir a la fosa la cantidad resultante del cálculo anterior (Z) y recircular durante 10 minutos (registrar en bitácora, ANEXO A).
Suspender la recirculación y tomar muestra.
6.3.11. Determinar pH y registrar en bitácora (ANEXO A).
Si el pH está entre 6.0 y 9.0 descargar el agua a la fosa (punto 6.2.9).
6.3.13. Si el pH no está entre 6.0 y 9.0 se debe neutralizar.
En caso de que el Hidróxido de Sodio (NaOH) entre en contacto con la piel, deberá enjuagar abundantemente con agua. En caso de quemaduras se deberá dar aviso inmediatamente al Servicio Médico de la Planta. En caso de un derrame de NaOH, se deberá avisar de inmediato al Departamento de Seguridad Industrial.
6.4. NEUTRALIZACIÓN PARTIENDO DE UNA SOLUCIÓN ALCALINA
Cuando el pH resulte mayor a 9.0, se deberá proceder a determinar la cantidad de Acido Clorhídrico a adicionar.
Preparar mesa de trabajo, soluciones y materiales.
6.4.2. Medir 100 ml de agua residual en una probeta y vertirla a un matraz Erlenmeyer.
Ajuste a “0” la bureta que contenga una solución de Ácido Clorhídrico (HCl) 0.1 N.
6.4.4. Adicionar 5 gotas de azul de bromotimol al matraz Erlenmeyer y agite. La muestra presentará una coloración azul lo que indica que se encuentra en una fase alcalina.
Proceder a neutralizar la muestra mediante la adición de HCl 0.1N. La neutralización se detectará cuando exista un vire de color de azul a amarillo claro.
Nota:
La adición de HCl 0.1 N debe ser gota a gota y agitando suavemente el matraz para detectar el momento exacto del vire de color. Si se adiciona rápidamente, el vire será a un amarillo intenso lo cuál indicará que la cantidad de HCl 0.1N es mayor a la necesaria para la neutralización.
Una vez terminada la neutralización anotar los mililitros consumidos de solución en la bitácora (ANEXO A). En caso de no detectar el vire de color, se debe repetir la prueba. Los desechos de la titulación se deberán vaciar a la fosa de agua residual.
6.4.7. Registrar en bitácora (ANEXO A) el volumen total de agua residual presente en la fosa.
6.4.8. Aplicar la formula resultante del siguiente razonamiento:
Solución a emplear: HCl 30 %
Densidad de HCl 29.57% = 1.15
PM = 36.461
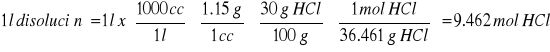
1 l disolución = 9.46 M
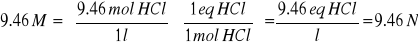
" 1 l disolución de HCl 30%= 1l disolución HCl 9.46 N
N1V1 = N2V2
(0.1)(w) = (9.46)(x)
![]()
Donde x= Volumen de HCl al 30% en ml
w=Volumen de HCl 0.1N en ml
100 ml ---- x
y ---- z
![]()
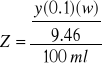
![]()
Donde:
Z = Son los litros de solución de HCl al 30% necesarios para neutralizar el volumen total de agua residual presente en la cisterna
y = Es el volumen total de agua residual presente en la cisterna en litros
w = Son los mililitros de solución de HCl 0.1 N resultantes de neutralizar una muestra de 100 ml de agua residual
6.4.9. Añadir a la fosa la cantidad resultante del cálculo anterior (Z) y recircular durante 10 minutos (registrar en bitácora, ANEXO A).
Suspender la recirculación y tomar muestra.
6.4.11. Determinar pH y registrar en bitácora (ANEXO A).
Si el pH está entre 6.0 y 9.0 descargar el agua a la fosa (punto 6.2.9).
Si el pH no está entre 6.0 y 9.0 se debe neutralizar.
Lo embaces vacíos del HCl y los de NaOH se deberán entregar a confinamiento
En caso de que el ácido Clorhídrico (HCl) entre en contacto con la piel, deberá enjuagar abundantemente con agua. En caso de quemaduras se deberá dar aviso inmediatamente al Servicio Médico de la Planta. En caso de un derrame de HCl, se deberá avisar de inmediato al Departamento de Seguridad Industrial.
7. REFERENCIAS
7.1. Norma Oficial Mexicana, NOM-002-ECOL-1996, que establece los límites máximos permisibles de contaminantes en las descargas de aguas residuales a los sistemas de alcantarillado urbano y municipal, publicada en el Diario Oficial de la Federación el 3 de junio de 1998.
7.2. Fernando Orozco D., “Análisis Químico Cuantitativo”, Edit. Porrua S.A., 1985 págs. 183-202
8. ANEXOS
ANEXO A monitoreo de AGUAS RESIDUALES INDUSTRIALES PROVENIENTES DE LA PLANTA CC LERMA
Descargar
| Enviado por: | Cristina Arellano |
| Idioma: | castellano |
| País: | España |
